Дорогие коллеги, дорогие друзья!
Миновала очередная зима нашей жизни, унося с собой новогодние праздники, ожидание снегопадов и холодов и некую замороженность в душе. Вступая в весну, мы прислушиваемся к пению птиц за

Марк Шагал.
Влюбленные. 1929 г.
Тонино Гуэрра
За два дня до смерти Федерико Феллини сказал: «Как хочется влюбиться еще раз!» Я был потрясен! На самом краю человек хотел еще раз пережить любовь, парить над землей, подчиняться тому...

НОВОСТИ ОНКОЛОГИИ / 4 ФЕВРАЛЯ – МЕЖДУНАРОДНЫЙ ДЕНЬ БОРЬБЫ С ОНКОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ
4 февраля ежегодно отмечается Всемирный день борьбы с онкологическими заболеваниями. Дата была провозглашена Международным противораковым союзом (UICC).

НОВОСТИ ОНКОЛОГИИ / ОПРЕДЕЛЕНЫ ПОБЕДИТЕЛИ ИНТЕНСИВА RUSSCO ПО РАКУ МОЛОЧНОЙ ЖЕЛЕЗЫ
2 февраля завершил свою работу интенсив RUSSCO, посвященный раку молочной железы, который проходил в онлайн-формате 28 января и 1-2 февраля и объединил специалистов из различных регионов нашей страны и соседних стран...

НОВОСТИ ОНКОЛОГИИ / ЕЩЕ РАЗ ОБ АДЪЮВАНТНОЙ ХИМИОТЕРАПИИ КОЛОРЕКТАЛЬНОГО РАКА II СТАДИИ
Начиная с 2004 года, после публикации исследования MOSAIC, а затем NSABP С-07, стандартным режимом для проведения адъювантной химиотерапии больным операбельным колоректальным раком III стадии стала комбинация FOLFOX [1, 2]...
НОВОСТИ ОНКОЛОГИИ / АСПИРИН ЭФФЕКТИВЕН В ПРЕДОТВРАЩЕНИИ РЕЦИДИВОВ У ОПЕРИРОВАННЫХ БОЛЬНЫХ КОЛОРЕКТАЛЬНЫМ РАКОМ
Несмотря на значительные достижения системной терапии колоректального рака (КРР) за последние два десятилетия, остается актуальной разработка эффективной адъювантной терапии с целью снижения рецидива заболевания у больных...
НОВОСТИ ОНКОЛОГИИ / ИЗМЕНЕНИЕ ВЕСА И РИСК СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ ОПЕРАБЕЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Все большее число пациенток с операбельным раком молочной железы не без основания рассчитывают на продолжительную жизнь после окончания лечения. Возможные осложнения операционного лечения и облучения (например, лимфостаз руки...
ЛОКАЛЬНОЕ ЛЕЧЕНИЕ МЕТАСТАЗОВ КОЛОРЕКТАЛЬНОГО РАКА В ЛЕГКИЕ: ЧТО ПРЕДПОЧЕСТЬ?
Легкие – одна из излюбленных локализаций метастазов колоректального рака. Хирургическое удаление очагов всегда считалось стандартом локального лечения, однако стереотаксическая лучевая терапия уже не раз посягала на пальму первенства...
УГОЛОК РАДИОТЕРАПЕВТА / SBRT ПРИ ЛОКАЛИЗОВАННОМ РАКЕ ПОЧКИ: ЕЩЕ РЫВОК, ПОБЕДА БЛИЗКА!
Эта тема выглядит уже не новой – но, тем не менее, в национальных рекомендациях лучевая терапия первичного локализованного рака почки до сих пор отсутствует (в рекомендациях NCCN метод упоминается вкупе с другими аблативными

УГОЛОК РАДИОТЕРАПЕВТА / КОММЕНТАРИЙ ЭКСПЕРТА
Какой же вариант аблативной терапии можно считать наилучшим для локализованной почечноклеточной карциномы? Безусловно, хирургический метод остается золотым стандартом, однако немалое количество пациентов не являются кандидатами...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ПРОГНОСТИЧЕСКОЕ И ПРЕДИКТИВНОЕ ЗНАЧЕНИЕ ЛЮМИНАЛЬНЫХ ТИПОВ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ: АНАЛИЗ ИССЛЕДОВАНИЯ DATA
Исследование DATA III фазы (NCT00301457) оценивало эффективность длительной гормональной терапии у женщин в постменопаузе с люминальным раком молочной железы на ранних стадиях. Исследователи проанализировали его результаты...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ФАКТОРЫ ПРОГНОЗА, ВЛИЯЮЩИЕ НА ВЫЖИВАЕМОСТЬ, У ПАЦИЕНТОВ С ОСТЕОГЕННЫМИ САРКОМАМИ
Индийское исследование прогностических моделей у пациентов с остеогенными саркомами (остеосаркомами и саркомой Юинга), опубликованное в JCO, обозначает несколько факторов, связанных с низкой безрецидивной выживаемостью пациентов...

ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / MORPHEUS-LIVER: ТИРАГОЛУМАБ В КОМБИНАЦИИ С АТЕЗОЛИЗУМАБОМ И БЕВАЦИЗУМАБОМ У ПАЦИЕНТОВ С МГЦР
Режим атезолизумаб/бевацизумаб стал стандартом 1-й линии при метастатическом ГЦР, продемонстрировав выигрыш в общей выживаемости в сравнении с сорафенибом. Тем не менее, медиана ОВ не превышает 2 лет. Сможет ли эскалация терапии...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / TROPiCS-04: ФИНАЛЬНЫЕ РЕЗУЛЬТАТЫ
Не всегда ADC одинаково хорошо работают при разных нозологиях. И если сацитузумаб говитекан первым показал обнадеживающие результаты в РМЖ, то в случае уротелиальной карциноме все складывается иначе...

ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / KEYLINK-006: ЭФФЕКТИВНА ЛИ ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ ОЛАПАРИБОМ И ПЕМБРОЛИЗУМАБОМ ПРИ ДИССЕМИНИРОВАННОМ НЕПЛОСКОКЛЕТОЧНОМ НМРЛ?
Более чем у половины пациентов с немелкоклеточным раком легкого заболевание клинически манифестирует и впервые выявляется уже на стадии опухолевой диссеминации, когда потенциальные лечебные опции преимущественно ограничены...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НОВАЯ РОЛЬ СА-125
Медуллярная карцинома почки (RMC) — это высокоагрессивная злокачественная опухоль, одна из типичных характеристик которой - потеря супрессора опухоли SMARCB1. Она в основном поражает молодых людей, преимущественно африканского...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / РАК МОЧЕВОГО ПУЗЫРЯ: ДВОЙНАЯ ИММУНОТЕРАПИЯ В КОМБИНАЦИИ С ЛТ В КАЧЕСТВЕ СЕЛЕКТИВНОГО ОРГАНОСОХРАНЯЮЩЕГО ПОДХОДА
Отдельной категории пациентов с локализованным раком мочевого пузыря (РМП) ввиду различных причин невозможно провести неоадъювантную терапию, альтернативным подходом в такой ситуации является химиолучевая или лучевая терапия в...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НОВЫЙ ЦВЕТ ТЕРАПИИ РАКА ПРОСТАТЫ: ФИОЛЕТОВЫЙ. VIOLET STUDY ДЛЯ ТЕРБИЯ-161-PSMA
Австралийские авторы недавно анонсировали важное событие: первое клиническое исследование "VIOLET" с тербием-161 PSMA для лечения рака простаты. «Мы не только не наблюдали дозолимитирующей токсичности в течение 6 циклов до 7,4...
НОВОСТИ ASCO GI 2025 / РАК ЖЕЛУДКА
EORTC-1203 GITC «INNOVATION»: сравнение эффективности комбинации химиотерапии и трастузумаба с или без пертузумаба в периоперационной химиотерапии рака желудка
НОВОСТИ ASCO GI 2025 / КОЛОРЕКТАЛЬНЫЙ РАК
Комбинированная иммунотерапия в лечении КРР с MSI/dMMR в исследовании CheckMate 8HW...
НОВОСТИ ASCO GU 2025 / РАК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
С 13 по 15 февраля в Сан-Франциско прошел очередной конгресс ASCО Genitourinary 2025. Давайте рассмотрим последние новости с конгресса и решим, позволят ли новые данные изменить нашу реальную практику уже сейчас...
НОВОСТИ ASCO GU 2025 / РАК МОЧЕВОГО ПУЗЫРЯ
NIAGARA trial: влияние pCR на отдаленные результаты лечения...
НОВОСТИ ASCO GU 2025 / РАК ПОЧКИ
Финальные данные CheckMate 9ER: ниволумаб + кабозантиниб vs сунитиниб в 1й линии терапии диссеминированного почечно-клеточного рака (ПКР)

ЭТО ИНТЕРЕСНО / КОФЕ УТРОМ – НИЖЕ РИСКИ
Кофе является одним из наиболее любимых и часто употребляемых напитков в мире. Большинство проспективных исследований показали, что умеренное потребление кофе связано с более низким риском развития диабета 2 типа...
Анонс
-

4 февраля 2025
ВСЕМИРНЫЙ ДЕНЬ БОРЬБЫ С ОНКОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ
ТЕЛЕМОСТ RUSSCO
-

20 - 21 МАРТА 2025
VII КОНФЕРЕНЦИЯ RUSSCO ОНКОУРОЛОГИЯ
КРАСНОЯРСК
-

27-28 МАРТА 2025
XII КОНФЕРЕНЦИЯ RUSSCO РАК МОЛОЧНОЙ ЖЕЛЕЗЫ
МОСКВА
-

24-25 АПРЕЛЯ 2025
XI КОНФЕРЕНЦИЯ RUSSCO РАК ЛЕГКОГО И ДРУГИЕ ОПУХОЛИ ГРУДНОЙ КЛЕТКИ
CАНКТ-ПЕТЕРБУРГ
Дорогие коллеги, дорогие друзья!
Миновала очередная зима нашей жизни, унося с собой новогодние праздники, ожидание снегопадов и холодов и некую замороженность в душе. Вступая в весну, мы прислушиваемся к пению птиц за окнами наших ординаторских, ощущаем тепло солнечных лучей, падающих на щеку. Весна не может не радовать - как надежда на лучшее, как предвкушение нового чувства. «С возрастом я всё более ясно ощущаю, как смешно то, что не имеет собственного смысла, собственной души, то, что не пронизано любовью,» — сказал Марк Шагал, который немалое количество своих работ посвятил теме любви, его парящих над обыденностью влюбленных знает весь мир.
Любви, душевности и смысла не бывает много, и порой человек ищет их всю жизнь. Уверены, многие онкологи согласятся, что наша любимая работа составляет немалую часть нашей жизни, придавая ей смысл. Российское общество клинической онкологии начало новый 2025 год, уже проведя несколько вебинаров и Большую конференцию RUSSCO «Опухоли ЖКТ», впереди нас ждут еще несколько крупных тематических конференций, а это значит, что весной нам точно не придется скучать, тем более что многие мероприятия меняют геолокацию и перемещаются из Москвы и Санкт-Петербурга в регионы, чтобы большее количество коллег смогли принять очное участие в них. Программы большинства из них уже на сайте, и мы приглашаем всех коллег присоединиться лично или онлайн. Но, погрузившись в работу, не забывайте о себе и о том, что на пороге Весна!
Доброй весны, нежной оттепели и много солнца каждому из вас!
Ваша команда RUSSCO
Марк Шагал.
Влюбленные. 1929 г.

Тонино Гуэрра
***
За два дня до смерти Федерико Феллини сказал: «Как хочется влюбиться еще раз!»
Я был потрясен! На самом краю человек хотел еще раз пережить любовь, парить над землей, подчиняться тому, кому хочется подчиняться, слышать музыку оркестра в душе… Когда ты любишь, ты перестаешь быть просто человеком, а становишься ароматом. Ты не ходишь по земле, а паришь над ней. Вот это состояние влюбленности и есть главное в жизни. И неважно, во что ты влюблен – в женщину, в работу, в мир или в жизнь…
НОВОСТИ ОНКОЛОГИИ / 4 ФЕВРАЛЯ – МЕЖДУНАРОДНЫЙ ДЕНЬ БОРЬБЫ С ОНКОЛОГИЧЕСКИМИ ЗАБОЛЕВАНИЯМИ

4 февраля ежегодно отмечается Всемирный день борьбы с онкологическими заболеваниями. Дата была провозглашена Международным противораковым союзом (UICC).
Цель этого масштабного мероприятия – акцентировать внимание общественности на распространенности, важности своевременного выявления и профилактики онкологических заболеваний. Рак является одной из ведущих причин смерти как во всем мире, так и в нашей стране. Поэтому в число приоритетных задач входит создание эффективной системы противораковой просветительной и воспитательной работы, чтобы в дальнейшем достичь уровня информированности населения, позволяющего изменить его отношение к онкологическим заболеваниям.
В течение всего февраля в каждом онкологическом учреждении страны, будь то крупный центр или ЦАОП, проводятся различные мероприятия и акции, позволяющие сделать двери онкоцентров открытыми для большого числа людей, даже тех, кто боялся думать об обследовании и гнал мысль о возможной закравшейся опухоли. Сделать шаг в сторону врача, инициировать обследование и в итоге развеять сомнения или выявить опухоль на ранней стадии и начать радикальное лечение до появления негативных симптомов – не это ли могло быть отличным результатом подобных акций?
4 февраля 2025 года в 10:00 по московскому времени состоялся ежегодный телемост Российского общества клинической онкологии RUSSCO. Это важное событие объединило специалистов в области онкологии. Мероприятие прошло в формате онлайн-вебинара и было доступно для участников, подключавшихся из разных регионов России. Председателями и модераторами телемоста выступили председатель RUSSCO профессор Дмитрий Александрович Носов, главный онколог РФ академик РАН Андрей Дмитриевич Каприн, главный внештатный онколог ДЗ Москвы академик РАН Игорь Евгеньевич Хатьков.
Программа телемоста включала в себя обсуждение ключевых тем, связанных с современными подходами к диагностике и лечению онкологических заболеваний. Участники смогли узнать о результатах последних исследований и лучших практиках в области онкологии в РФ. В этом году для докладов подключались коллеги из Новосибирска, Перми, Тюмени, Казани, Тулы и Москвы.
НОВОСТИ ОНКОЛОГИИ / ОПРЕДЕЛЕНЫ ПОБЕДИТЕЛИ ИНТЕНСИВА RUSSCO ПО РАКУ МОЛОЧНОЙ ЖЕЛЕЗЫ
Старостин Никита Максимович
врач-онколог химиотерапевтического отделения №3
Онкоцентра №1 ГКБ им. С.С. Юдина ДЗМ (г. Москва)
Сиз Наталья Андреевна
врач-онколог кабинета амбулаторной химиотерапии
Гомельского областного онкологического диспансера
(г. Гомель, Республика Беларусь)
2 февраля завершил свою работу интенсив RUSSCO, посвященный раку молочной железы, который проходил в онлайн-формате 28 января и 1-2 февраля и объединил специалистов из различных регионов нашей страны и соседних стран.
В рамках интенсива участники имели возможность прослушать лекции членов комитета RUSSCO junior, которые подняли такие важные вопросы, как рак и беременность, а также онкофертильность, и поделились последними достижениями в области научных исследований и клинической практики. После лекционного курса основной упор был сделан на разбор сложных клинических случаев, что позволило участникам получить практические рекомендации и советы от опытных коллег, а также поучаствовать в дискуссиях и интерактивном консилиуме с экспертами: д.м.н., в.н.с. отделения противоопухолевой лекарственной терапии №1 отдела противоопухолевого лекарственного лечения НИИ онкологии им. Н.Н. Трапезникова Фроловой Моной Александровной и к.м.н., заведующей онкологическим отделением противоопухолевой лекарственной терапии ГБУЗ «ММКЦ «Коммунарка» ДЗМ» Глазковой Еленой Владимировной.
Во время обучающего курса традиционно участники активно зарабатывали баллы в свой личный рейтинг, который оценивался экспертами и наставниками курса. Как и заявлялось ранее, главным призом для одного из участников интенсива станет поездка на XII конференцию RUSSCO «Рак молочной железы», которая состоится 28-29 марта в Москве.
Сегодня мы готовы подвести итоги мероприятия и с большим удовольствием поздравляем победителей, разделивших между собой первое место: Старостин Никита Максимович (г. Москва) и Сиз Наталья Андреевна (г. Гомель, Республика Беларусь). Второе место по количеству набранных баллов досталось Кобец Дарье Петровне (г. Москва). А третье – Юлдашевой Наталье Олеговне (г. Уфа). Кроме того, хочется дополнительно отметить лучшего ординатора курса – Вычегжанину Елену Павловну, ординатора НМИЦ онкологии им. Н.Н. Петрова, которая продемонстрировала высокий уровень знаний, наравне с практикующими врачами. А лучший результат за итоговый тест принадлежит Грибову Вадиму Валентиновичу (г. Макеевка).
НОВОСТИ ОНКОЛОГИИ / ЕЩЕ РАЗ ОБ АДЪЮВАНТНОЙ ХИМИОТЕРАПИИ КОЛОРЕКТАЛЬНОГО РАКА II СТАДИИ
Автор: Тюляндин Сергей Алексеевич
Заслуженный деятель науки РФ, главный научный сотрудник отделения
противоопухолевой лекарственной терапии №2
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
член правления RUSSCO, профессор, доктор медицинских наук, Москва
Начиная с 2004 года, после публикации исследования MOSAIC, а затем NSABP С-07, стандартным режимом для проведения адъювантной химиотерапии больным операбельным колоректальным раком III стадии стала комбинация FOLFOX [1, 2]. В исследовании MOSAIC добавление оксалиплатина к комбинации 5-фторурацила и лейковорина (FP) в сравнении с только PF уменьшило риск прогрессирования на 20% (5-летняя безрецидивная выживаемость – 73% и 67% соответственно) и на 16 % риск смерти (6-летняя общая выживаемость – 78,5% и 76%) [1]. Оба эти исследования включали больных с II (Т3-4N0) стадией, но в обоих случаях не было получено достоверных данных о пользе добавления оксалиплатина в этой популяции. В декабрьском номере Journal of Clinical Oncology опубликована статья, посвященная объединенному анализу результатов адъювантной терапии больных II стадией колоректального рака исследований MOSAIC и NSABP С-07. В этой работе также анализируются критерии высокого риска для этой стадии колоректального рака, как те, что были использованы для селекции больных в эти исследования, так и появившиеся позднее (например, локализация первичной опухоли, возраст, менее 12 исследованных лимфоузлов и индекс массы тела – BMI).
В совместный анализ вошли 1595 больных (797 получали FOLFOX и 798 PF) со II стадией колоректального рака, из них 689 были отнесены к группе высокого риска (345 получали FOLFOX и 344 PF), поскольку имели хотя бы один из следующих критериев: T4, перфорация опухоли, кишечная непроходимость, низкодифференцированный рак, венозная инвазия или менее 10 изученных лимфатических узлов. Было показано, что добавление оксалиплатина не привело к увеличению общей выживаемости как для всех больных со II стадией (HR=1,03; p=0,83), так и для больных с высоким риском (HR=0,86; p=0,349). При однофакторном анализе возраст, наличие перфорации или обструкции, сторона возникновения первичной опухоли, пол и стадия T имели прогностическое значение. При многофакторном анализе не было получено данных о влиянии добавления оксалиплатина на общую выживаемость в подгруппах Т3 и Т4, у больных моложе 50 лет и при меньшем чем 12 изученных лимфоузлов. Отдельно был проведен анализ у больных со следующими факторами высокого риска: T4, наличие перфорации или обструкции, левая сторона локализации первичной опухоли, возраст старше 70 лет и мужской пол. Не было показано, что добавление оксалиплатина улучшает общую выживаемость при наличии каждого из этих критериев в отдельности или в комбинации. Также не было получено данных о пользе добавления оксалиплатина при использовании критериев плохого прогноза ESMO (опухоль Т4 и менее 12 исследованных лимфоузлов).
В объединенном анализе исследований MOSAIC и NSABP C-07 проведена оценка влияния добавления оксалиплатина к комбинации PF в качестве адъювантной химиотерапии у больных колоректальным раком II стадии высокого риска. Показано, что добавление оксалиплатина к адъювантной терапии не улучшает результаты общей выживаемости больных со II стадией колоректального рака независимого от наличия критериев высокого риска прогрессирования. Авторы делают категоричный вывод, что оксалиплатин-содержащие комбинации не должны быть стандартом лечения при адъювантной терапии колоректального рака II стадии даже у пациентов с высоким риском. Одновременно авторы подчеркивают важность интеграции определения наличия или отсутствия циркулирующей опухолевой ДНК (ctDNA) при селекции больных II стадией для проведения адъювантной химиотерапии. Уровни ctDNA могут быть более точными в сравнении с традиционными клинико-патологическими критериями высокого риска прогрессирования для выявления пациентов с риском рецидивирования, которые с большей вероятностью получат потенциальную пользу от адъювантной терапии.
Категоричный вывод авторов объединенного анализа, в числе которых был родоначальник использования оксалиплатина при колоректальном раке Аймери де Грамонт, несколько противоречит Практическим рекомендациям RUSSCO версии от 2024 года. Согласно нашим рекомендациям, только для больных с T3N0 и одним из критериев высокого риска рекомендовано адъювантное назначение PF в течение 6 месяцев или комбинация XELOX в течение 3 месяцев. При одинаковой эффективности разница в 3 месяца по продолжительности может быть более предпочтительней для молодых сохранных пациентов, что делает уместной сохранение этой опции. Для больных T3N0 c двумя и более критериями высокого риска и для Т4N0 рекомендуются только комбинации с включением оксалиплатина: XELOX 3 месяца или FOLFOX 6 месяцев. Основываясь на результатах объединенного анализа, кажется уместным хотя бы добавление PF в качестве еще одной опции. При равной противоопухолевой эффективности отсутствие периферической нейротоксичности представляется важным преимуществом PF.
Источники:
- André T, Boni C, Mounedji-Boudiaf L, et al. Oxaliplatin, fluorouracil, and leucovorin as adjuvant treatment for colon cancer. N. Engl. J Med. 2004; 350: 2343-2351.
- Kuebler JP, Wieand HS, O’Connell MJ, et al. Oxaliplatin combined with weekly bolus fluorouracil and leucovorin as surgical adjuvant chemotherapy for stage II and III colon cancer: results from NSABP C-07. J. Clin. Oncol. 2007; 25: 2198-2204.
- Chibaudel B, Raeisi M, Cohen R, et al. Assessment of the addition of oxaliplatin to fluoropyrimidine-based adjuvant chemotherapy in patients with highrisk stage II colon cancer: an ACCENT pooled analysis. J. Clin. Oncol. 2024; 42: 4187-4195.
НОВОСТИ ОНКОЛОГИИ / АСПИРИН ЭФФЕКТИВЕН В ПРЕДОТВРАЩЕНИИ РЕЦИДИВОВ У ОПЕРИРОВАННЫХ БОЛЬНЫХ КОЛОРЕКТАЛЬНЫМ РАКОМ
Несмотря на значительные достижения системной терапии колоректального рака (КРР) за последние два десятилетия, остается актуальной разработка эффективной адъювантной терапии с целью снижения рецидива заболевания у больных, перенесших хирургическую резекцию с лечебной целью. Наши все возрастающие знания о биологии колоректального рака открыли и открывают новые мишени для противоопухолевой терапии. Одной из привлекательных терапевтических мишеней является фермент циклооксигеназа-2 (COX-2) – член семейства ферментов циклооксигеназы, которые действуют как посредники воспаления путем преобразования арахидоновой кислоты в простагландины. COX-2 часто гиперэкспрессирована при КРР, что сочетается с высокой пролиферативной активностью, инвазией и метастазированием. Доклинические модели показали, что ингибирование COX-2 ослабляет рост опухоли. В связи с этим использование аспирина или других нестероидных противовоспалительных препаратов является рациональной стратегией профилактики и лечения КРР. Исследования показали, что регулярное использование аспирина в низких дозах снижает риск развития КРР, снижает частоту аденом после резекции аденомы или рака и связано с уменьшением частоты метастазов при приеме после постановки диагноза КРР. Хотя регулярное прием аспирина, как правило, хорошо переносится, препарат не рекомендуют в профилактических целях из-за возможных побочных эффектов, таких как желудочнокишечные язвы и кровотечения, а также геморрагический инсульт. Поиск биомаркеров, которые предсказывают пользу от ингибирования COX-2, является актуальной задачей. В последние годы появляется все больше свидетельств, что противоопухолевый эффект аспирина при КРР сочетается с наличием в клетках опухоли больного соматических мутаций в гене PIK3CA. Поэтому статус мутации PIK3CA был предложен в качестве предиктора эффективности лечения аспирином при колоректальном раке. Однако механизмы, лежащие в основе этого клинического явления, пока неясны.
Ген PIK3CA кодирует каталитическую субъединицу p110α класса IA фосфатидилинозитол 3-киназы (PI3K). Исследования in vivo и in vitro показали, что мутации в этом гене связаны с плохим прогнозом для онкологических больных и устойчивостью к стандартным методам лечения, таким как химиотерапия и терапия моноклональными антителами. Мутации в пути PI3K/Akt/mTOR являются одними из самых распространенных при различных типах рака, включая не только КРР, но и рак легких, молочной железы и простаты, которые в общей сложности ответственны за смерть более трех миллионов человек во всем мире ежегодно. Этот сигнальный путь имеет решающее значение в регуляции клеточного цикла, что делает его перспективной мишенью для противораковой лекарственной терапии.
Одним из последствий активации пути PI3K/Akt/mTOR является повышенная экспрессия COX-2, однако не было выявлено никакой корреляции между мутацией PIK3CA и экспрессией COX2. Хотя ингибирующее влияние аспирина на простагландиновый путь является одним из доказанных механизмов, остается неясным, как аспирин связан с благоприятным воздействием на пациентов, имеющих соматические мутации PIK3CA. Возможной потенциальной мишенью для аспирина может быть NF-κB вследствие активации сигнального пути PIK3/AKT/mTOR. NF-κB является важнейшим медиатором воспаления, который индуцирует экспрессию провоспалительных генов, кодирующих цитокины и хемокины. NF-κB также участвует в экспрессии COX-2. Другой возможной точкой приложения аспирина является кишечная микробиота, которая участвует в воспалительных процессах и поддержании кишечного гомеостаза. В этом контексте было отмечено, что аспирин может влиять на рост кишечных бактерий, что может приводить к сдвигу кишечной микрофлоры в сторону более благоприятного состава.
Все вышеизложенной послужило основанием для проведения в скандинавских странах исследования ALASCCA, в котором изучалось целесообразность назначения аспирина с целью уменьшения частоты развития рецидива у оперированных больных КРР с наличием активации сигнального пути PI3K. В исследование включались пациенты, оперированные по поводу КРР I-III стадии с наличием активирующей мутации в 9 или 20 экзонах PIK3CA или с активацией сигнального пути вследствие мутации PTEN или любой другой мутации PIK3CA. Эти две группы в отдельности были рандомизированы на получение аспирина в дозе 160 мг ежедневно в течение 3 лет или плацебо. Из 3508 скринированных больных по данным генетического анализа мутации в 9 или 20 экзонах PIK3CA (группа А) выявлены у 515 (14,7%) и мутации PTEN и другие мутации PIK3CA (группа В) – у 588 (16,7%) больных. В исследование из этих групп было включено 314 и 312 больных соответственно. Основным критерием эффективности активирующих мутаций составили частота и время рецидива заболевания в группе А. Медиана возраста пациентов – 62 года, 52% были женщинами, у 67% был диагностирован рак ободочной кишки (II стадия – 53%, III – 47%), у 33% – рак прямой кишки (I стадия – 24%, II – 40%, III – 47%). У 50% больных раком прямой кишки проведена неоадъювантная терапия, 50% больных раком ободочной кишки получали адъювантную терапию.
Оценен 3-летний период наблюдения. В группе А прием аспирина сочеталcя со снижением частоты рецидивов по сравнению с плацебо с 14,1% до 7,7% (HR=0,49; p=0,044), в группе В – с 16,8% до 7,7% (HR=0,42; p=0,013). Польза от приема аспирина отмечается в обеих группах и при их объединении свидетельствует о 55% снижении относительного риска прогрессирования. Польза от аспирина нашла свое отражение в показателях 3-летней безрецидивной выживаемости (DFS), которые выросли на 7,1% и 10,4% в группах А и В соответственно (см. табл.1.).
Таблица 1.
Результаты 3-летнего наблюдения оперированных
больных КРР, получавших адъювантно аспирин или плацебо.
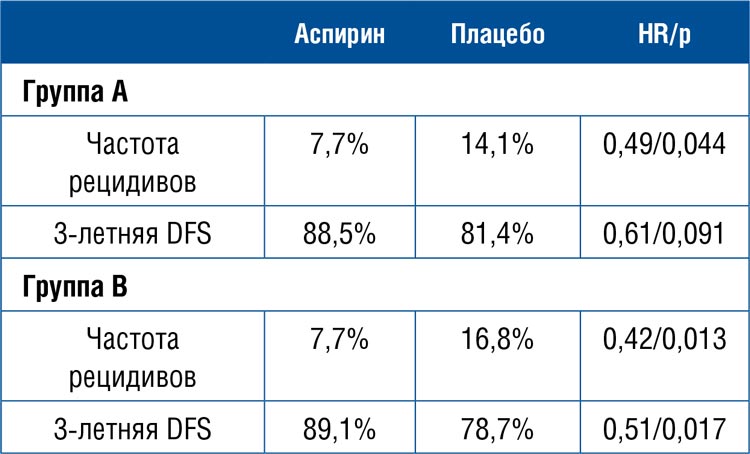
При наблюдении за ходом исследования побочные эффекты были зарегистрированы у 301 и 228 больных в группах аспирина и плацебо, из которых у 57 и 38 соответственно отнесены к серьезным. По причине токсичности умерли 3 больных в группе аспирина и 1 больной в группе плацебо. У 4 больных, принимавших аспирин, зарегистрированы желудочно-кишечные кровотечения. Авторы исследования делают вывод об убедительной пользе назначения аспирина для снижения риска прогрессирования оперированных больных КРР с наличием мутации PIK3CA или PTEN. Аспирин в дозе 160 мг внутрь ежедневно в течение 3 лет примерно в 2 раза снижает риск прогрессирования у 20-30% больных КРР, имеющих эти соматические мутации. Полученные результаты служат основанием для включения адъювантного назначения аспирина в клинические рекомендации. Также требуется внести в клинические рекомендации необходимость проведения тестирования операбельных больных КРР на выявление мутаций в генах, кодирующих белки сигнального пути PIK3 (PIK3CA и PTEN).
Источники:
- Hall DCN, Benndorf RA. Aspirin sensitivity of PIK3CA-mutated сcolorectal сancer: potential mechanisms revisited. Cell. Mol. Life Sci. 2022; 79: 393.
- Domingo E, Church DN, Sieber O, et al. Evaluation of PIK3CA mutation as a predictor of benefit from nonsteroidal anti-inflammatory therapy in colorectal cancer. J. Clin. Oncol. 2013; 31: 4297-4305.
- Martling А, Lindberg J, Myrberg IH, et al. Low-dose aspirin to reduce recurrence rate in colorectal cancer patients with PI3K pathway alterations: 3-year results from a randomized placebo-controlled trial. J. Clin. Oncol. 2025; 43 (suppl 4; abstr. LBA125). This research was presented at the 2025 ASCO Gastrointestinal Cancers Symposium in San Francisco.
Тюляндин Сергей Алексеевич
НОВОСТИ ОНКОЛОГИИ / ИЗМЕНЕНИЕ ВЕСА И РИСК СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ У БОЛЬНЫХ ОПЕРАБЕЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Все большее число пациенток с операбельным раком молочной железы не без основания рассчитывают на продолжительную жизнь после окончания лечения. Возможные осложнения операционного лечения и облучения (например, лимфостаз руки на стороне поражения) и химиотерапии (например, периферическая нейропатия после таксанов), депрессия могут быть причиной снижения физической активности. Наступление ранней менопаузы у молодых пациенток и полное длительное ингибирование эстрогенов при проведении гормональной адъювантной терапии изменяет гормональный профиль больных. А все это вместе взятое способствует увеличению веса пациенток в ходе адъювантной терапии и после ее окончания, что может сопровождаться повышенным риском развития сердечной недостаточности. Именно оценке влияния изменения веса больных операбельным раком молочной железы после оперативного лечения и его влияния на частоту сердечной недостаточности было посвящено общенациональное исследование, проведенное в Южной Корее.
В исследовании использовалась база данных Национальной службы медицинского страхования Республики Кореи для выявления женщин с диагнозом инвазивного рака молочной железы в период с января 2010 года по декабрь 2016 года без диагноза сердечной недостаточности до или в течение 1 года после диагностики рака. Изменение веса определялось по результатам двухгодичных медицинских осмотров до (0-2 года) и после (0,5-2,5 года) диагностики рака.
В исследование было включено 43717 женщин с медианой возраста 53,7 года, со средним индексом массы тела (BMI) до постановки диагноза 23,5 кг/м2 и после постановки диагноза 23,3 кг/м2. В течение 2 лет после постановки диагноза у 6,1% пациентов зафиксирована потеря веса более 10%, у 15,7% потеря составила от 5% до 10% веса, 63,9% сохранили вес, у 10,7% отмечена прибавка в весе от 5% до 10% и у 3,5% прибавка составила более 10%. Среди пациентов с ожирением до постановки диагноза 77% сохранили ожирение, несмотря на рекомендации снижения веса. Частота использования антрациклинов при проведении адъювантной химиотерапии была самой высокой (58,5%) среди пациентов с потерей веса >10%.
Медиана наблюдения за больными составила 4,7 года. При многофакторном анализе с учетом возраста, стадии, проведенного лечения, менопаузального статуса и с поправкой на сердечно-сосудистые факторы риска у пациентов с прибавкой веса от 5% до 10% зарегистрировали достоверное увеличение частоты развития сердечной недостаточности в 1,59 раза по сравнению с пациентами со стабильным весом (HR=1,59; 95% доверительный интервал [ДИ] 1,16-2,17). У пациенток с прибавкой веса >10% риск сердечной недостаточности повышался в 1,85 раза (HR 1,85; 95% ДИ 1,15-2,98). Не отмечено значимого влияния на частоту сердечной недостаточности у больных с потерей веса от 5% до 10% (HR 0,97; 95% ДИ 0,72- 1,32) или потерей более >10% (HR 1,00; 95% ДИ 0,64-1,56) по сравнению с пациентами с сохраненным весом. Пациенты с ожирением до и после постановки диагноза имели численный, но статистически незначимый повышенный риск сердечной недостаточности по сравнению с пациентами с отсутствием ожирения (HR 1,37; 95% ДИ 0,91-2,07). Исследователи пришли к выводу, что увеличение веса после постановки диагноза рака молочной железы было связано с повышенным риском сердечной недостаточности, причем этот риск возрастал по мере увеличения веса.
Эти результаты еще раз подчеркивают важность информирования больных операбельным раком молочной железы о необходимости поддержания здорового веса, особенно в течение первых нескольких лет после постановки диагноза, для профилактики возникновения или осложнения заболеваний сердечно-сосудистой системы. Не менее важно для больных получить консультации по правильному питанию и адекватной физической нагрузке и контролировать их выполнение, хотя бы измеряя вес больных при обязательном ежегодном осмотре в первые 5 лет после постановки диагноза. Кроме снижения риска сердечно-сосудистых и других хронических заболеваний, поддержание правильного веса в соответствии с возрастом, здоровое питание и адекватная физическая активность снижают риск прогрессирования рака молочной железы. Это исследование имеет важное значение и для нашей страны, где пациентки, страдающие раком молочной железы, чаще, чем в Южной Корее, имеют избыточный для своего возраста вес.
Источник:
Jung W, Park YM, Yu J, et al. Weight changes and heart failure risk after breast cancer development. JAMA Oncol. Published online: January 09, 2025.
Тюляндин Сергей Алексеевич
ЛОКАЛЬНОЕ ЛЕЧЕНИЕ МЕТАСТАЗОВ КОЛОРЕКТАЛЬНОГО РАКА В ЛЕГКИЕ: ЧТО ПРЕДПОЧЕСТЬ?
Легкие – одна из излюбленных локализаций метастазов колоректального рака. Хирургическое удаление очагов всегда считалось стандартом локального лечения, однако стереотаксическая лучевая терапия уже не раз посягала на пальму первенства как наиболее оптимальный, неинвазивный и эффективный метод локального воздействия. Правда, пока это не касалось именно метастазов КРР, поскольку они считаются наименее чувствительными к облучению, поэтому роль ЛТ в их лечении до конца не ясна.
Южнокорейские авторы в своем ретроспективном анализе демонстрируют интересные данные. В период с 2010 по 2017 гг в медицинском центре университета Yonsei было пролечено 404 больных колоректальным раком, которые получили локальное воздействие всего на 528 очагов в легких (хирургическое удаление или SBRT). При этом к операции прибегали чаще всего в случае солитарного поражения небольшого объема без признаков метастазов в других органах, тогда как к облучению – при очагах большего размера, множественных и сочетающихся с метастатическим поражением других зон помимо легких. Наиболее часто использовались схемы 50 Гр за 5 фракций, 48 Гр за 4 фракции и 45 Гр за 3 фракции. Средняя БЭД составляла 112 Гр ± 11 Гр. Первичной конечной точкой исследования был выбран локальный контроль, вторичными – ВБП, ОВ и токсичность.
В итоге в группе операции оказали 334 пациента с 367 очагами, в группе SBRT – 70 больных со 161 очагом.
Средний период наблюдения был 31,7 мес. Локальный контроль за 1 и 3 года составил 97,1% и 88,6% в группе операции, что мало отличалось от результатов в группе SBRT: 95,7% и 86,7%, p=0.174 (рис.1), причем эти различия оставались незначительными и в мультивариантном анализе.
Рисунок 1.
Локальный контроль в группах.
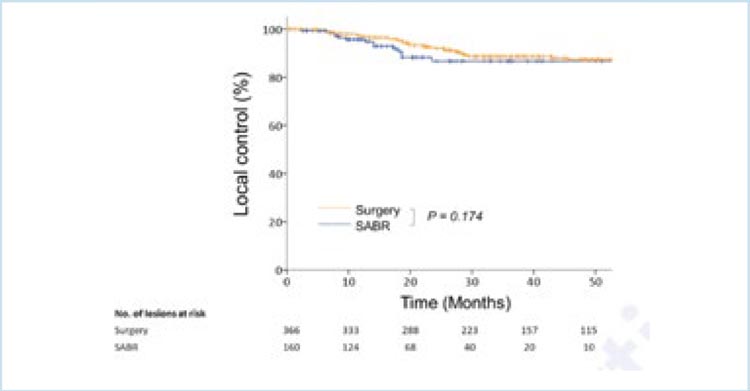
Среди пациентов группы хирургического лечения 8,1% имели серьезные послеоперационные осложнения; в группе SBRT у 4,2% отмечен лучевой пневмонит 3-4 степени. Показатели ВБП и ОВ нумерически были лучше в группе операции: 1-годичная ВБП 71,1% против 40,8%, 3-летняя ОВ – 45,3% против 27,9%; во многом это связано с тем, что прогноз у подавляющего большинства пациентов группы SBRT был изначально хуже. Тем не менее, данные исследования демонстрируют, что адекватные биологически эквивалентные дозы излучения позволяют реализовать эффект оптимальным образом, что делает результаты локального контроля после SBRT абсолютно сопоставимыми с таковыми после операции. Без сомнения, SBRT является методом выбора для многих пациентов, и требуются проспективные исследования, чтобы подтвердить адекватность этого лечебного подхода.
Источник:
Byung min Lee et al. Stereotactic Ablative Radiotherapy Versus Surgery in Patients with Pulmonary Metastases from Colorectal Cancer. Cancer Research and Treatment, Published online: February 6, 2025. DOI: https://doi. org/10.4143/crt.2024.1040
УГОЛОК РАДИОТЕРАПЕВТА / SBRT ПРИ ЛОКАЛИЗОВАННОМ РАКЕ ПОЧКИ: ЕЩЕ РЫВОК, ПОБЕДА БЛИЗКА!
Эта тема выглядит уже не новой – но, тем не менее, в национальных рекомендациях лучевая терапия первичного локализованного рака почки до сих пор отсутствует (в рекомендациях NCCN метод упоминается вкупе с другими аблативными методиками, которые являют собой инвазивные процедуры, и лишь в примечаниях конкретизировано, что SBRT предпочтительна для пациентов, не подходящих для оперативного вмешательства, имеющих I-III стадии процесса, преимущественно с опухолями до 7 см в дм). Меж тем, уже немалое количество исследований демонстрирует адекватность и сопоставимость SBRT при первичном раке почки.
Февральский номер журнала Lancet Oncology предоставляет нам еще одно такое доказательство в виде систематического обзора и метаанализа по применению аблативных методик в лечении локализованного первичного рака почки.
Авторы предприняли поиск публикаций с 2000 по 2024 гг., включив наблюдательные и проспективные рандомизированные исследования по применению SBRT, радиочастотной абляции (РЧА), микроволновой и криоабляции в лечении первичного локализованного ПКР, и в итоге включили 133 работы (8910 пациентов) для метаанализа. Первичной конечной точкой стал локальный контроль за 1, 2 и 5 лет с момента старта проведенного лечения. Частота и выраженность осложнений также регистрировалась авторами.
Локальные показатели контроля составили:
- для SBRT – 99% (95% ДИ 97-100; I2=6%) в течение 1 года, 97% (95- 99; I2=0%) в течение 2 лет и 95% (89-98; I2=42%) в течение 5 лет;
- для радиочастотной абляции – 96% (94-98; I2=73%) в течение 1 года, 95% (92-98; I2=77%) в течение 2 лет и 92% (88-96; I2=78%) в течение 5 лет;
- для микроволновой абляции – 97% (95-99; I2=74%) в течение 1 года, 95% (92-98; I2=77%) в течение 2 лет и 86% (75-94; I2=66%) в течение 5 лет; • для криоабляции – 95% (93-96; I2=61%) в течение 1 года, 94% (91- 96; I2=69%) в течение 2 лет и 90% (87-93; I2=74%) в течение 5 лет.
Доля пациентов с побочными эффектами 3-4 степени составила 3% (121 из 3726) после криоабляции, 2% (39 из 2503) после радиочастотной абляции, 1% (22 из 2069) после микроволновой абляции и 2% (11 из 612) после SBRT.
Этот крупный метаанализ на данный момент является первым, в котором сравниваются клинические результаты SBRT с другими общепринятыми (и внесенными в рекомендации) абляционными методами лечения локализованного почечноклеточного рака, включая радиочастотную абляцию, микроволновую абляцию и криоабляцию, и, помимо этого, авторы затрагивают пробелы, касающиеся отсутствия сравнительных данных об эффективности SBRT и вышеупомянутых методов.
Результаты метаанализа показывают, что SBRT может быть особенно выгодным вариантом для лечения более крупных опухолей почки (нежели те, что доступны для других методов), обеспечивая самые высокие показатели локального контроля среди всех абляционных вариантов со сравнительно низкими показателями тяжелых осложнений. При этом для периферических опухолей меньшего объема все методы продолжают представлять собой эффективный выбор с надежными профилями безопасности. Будущие работы должны быть направлены на проведение рандомизированных контролируемых исследований среди большего числа пациентов для дальнейшего определения наиболее оптимальных долгосрочных результатов при использовании тех или иных локальных методов. А составителям отечественных рекомендаций пора перестать рассматривать SBRT только как экспериментальный метод лечения, приемлемый лишь в рамках клинических исследований, тем более что во многих центрах России метод освоен и применяется достаточно широко у пациентов, не подходящих или отказавшихся от хирургического вмешательства.
Источник:
Ryan S Huang, Ronald Chow, Ali Benour, David Chen, Gabriel Boldt, Christopher J D Wallis, Anand Swaminath, Charles B Simone, Michael Lock, Srinivas Raman. Comparative efficacy and safety of ablative therapies in the management of primary localised renal cell carcinoma: a systematic review and meta-analysis. The Lancet Oncology. 2025. ISSN 1470- 2045. https://doi.org/10.1016/S1470- 2045(24)00731-9.
УГОЛОК РАДИОТЕРАПЕВТА / КОММЕНТАРИЙ ЭКСПЕРТА
Автор: Деньгина Наталья Владимировна
Заведующая радиологическим отделением
ГУЗ «Областной клинический онкологический диспансер»,
директор Центра лучевой терапии «R-Spei», член правления RUSSCO,
главный редактор Газеты RUSSCO и сайта RosOncoWeb,
кандидат медицинских наук, Ульяновск
Какой же вариант аблативной терапии можно считать наилучшим для локализованной почечноклеточной карциномы? Безусловно, хирургический метод остается золотым стандартом, однако немалое количество пациентов не являются кандидатами для операции по различным причинам, поэтому определиться с оптитмальным неинвазивным (или малоинвазивным) аблативным методом чрезвычайно важно. Недавний мета-анализ, включающий 133 исследования и 8910 пациентов, пожалуй, демонстрирует наиболее глубокий анализ этой проблемы.
- Пациенты в группах SBRT,
РЧА, МВА и криоаблации несколько различались между собой, причем группе лучевой терапии достались более сложные
больные (как всегда): более возрастные (средний возраст 73,5
года, в отличие от, например,
группы РЧА – 65,6 лет), с большим размером опухолей (3,9 см
против 2,8 в группе РЧА), с худшей функцией почек (eGFR 63,9
против 71,9 в группе МВА), рис.1;
Рисунок 1. Характеристики пациентов в группах
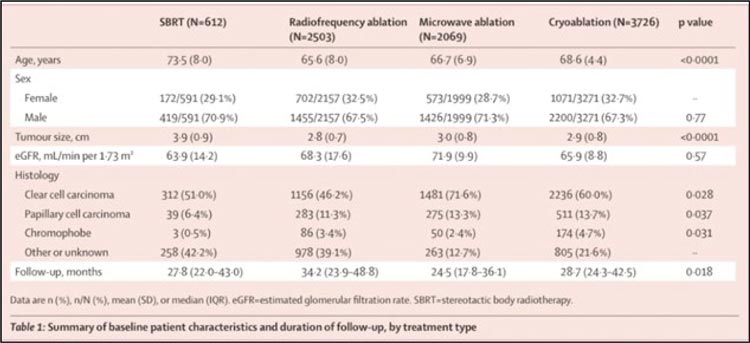
- Основные результаты метаанализа: локальный контроль. На
отрезке 5 лет ЛК был лучшим для
пациентов группы SBRT – 95%, в
сравнении с другими методами
(РЧА – 92%, МВА – 86%, криоабляция – 90%). При этом размер
опухоли имеет значение: при опухолях менее 4 см все методы демонстрировали хорошие результаты ЛК, тогда как в случае 4 и
более см именно лучевая терапия
показывала лучший ЛК – 93% (в
сравнении с РЧА – 79%), рис.2;
Рисунок 2. Основные результаты мета-анализа – локальный контроль и ОВ
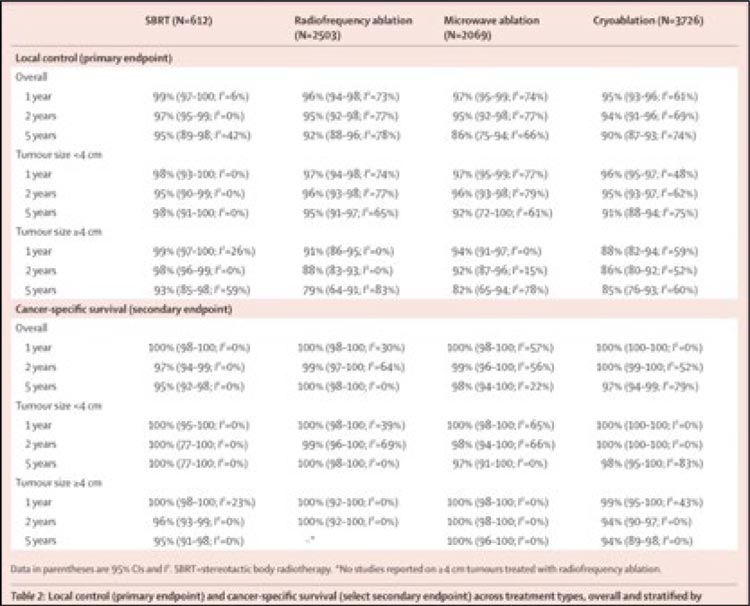
- Основные результаты: выживаемость. На отрезке 1 год все методы продемонстрировали практически 100% ОВ, тогда как через 5 лет показатель уже различался между группами: SBRT – 95%, РЧА – 100%, МВА – 98%, криоабляция – 97% (рис.2). При этом отбор в лечебные группы имел значение – мы помним, что на лучевую терапию шли более возрастные пациенты с более высоким риском и большим размером опухолей;
- Процент нежелательных явлений 3-4 в целом был невысок (SBRT – 2%, РЧА – 2%, МВА – 1%, криоабляция – 3%);
- Изменение функциональной
способности почек варьировало на
различных временных отрезках, с
тенденцией ухудшения к пятому
году наблюдения, и в сравнении
с другими методами SBRT демонстрировала явно не самые худшие
результаты (рис.3).
Рисунок 3. Показатели функции почек в группах с течением времени
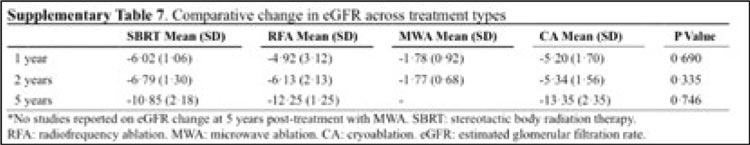
Что могут значить данные этого мета-анализа для клиницистов?
Во-первых, то, что все методы весьма эффективны в лечении локализованного ПКР. При этом SBRT более предпочтительна для опухолей большего размера (4 см и более), а в целом выбор метода должен быть персонализированным. Во-вторых, мета-анализ четко демонстрирует: SBRT продолжает уверенно завоевывать позиции помимо легких и простаты, и все больше очевидных фактов поддерживает ее более широкое применение, в том числе и для первичного рака почки. При этом экономическая эффективность играет немалую роль. В будущем требуются рандомизированные проспективные исследования с прямым сравнением результатов SBRT и РЧА/МВА, а также разработка протоколов стандартизации дозы ЛТ и фракционирования.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ПРОГНОСТИЧЕСКОЕ И ПРЕДИКТИВНОЕ ЗНАЧЕНИЕ ЛЮМИНАЛЬНЫХ ТИПОВ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ: АНАЛИЗ ИССЛЕДОВАНИЯ DATA
Исследование DATA III фазы (NCT00301457) оценивало эффективность длительной гормональной терапии у женщин в постменопаузе с люминальным раком молочной железы на ранних стадиях. Исследователи проанализировали его результаты, чтобы определить прогностическую значимость люминальных подтипов и сравнить эффективность длительной терапии анастрозолом у пациентов с люминальным А- и В-типами.
В исследование было включено 788 больных в постменопаузе с ранним люминальным раком молочной железы (491 пациенток с люминальным A подтипом, 297 – с люминальным B), получивших терапию тамоксифеном в течение 2-3 лет.
Пациентки были рандомизированы в 2 группы в соотношении 1:1:
- группа длительной 6-летней гормональной терапии;
- группа 3-летней гормональной терапии (контрольная группа).
Медиана времени наблюдения после рандомизации составила 13 лет. Пациентки с люминальным B подтипом в сравнении с люминальным A не имели cтатистически значимой разницы в отношении выживаемости без прогрессирования (HR 1,15; 95% ДИ 0,92-1,44; р=0,23) в течение всего периода наблюдения, однако они имели тенденцию к ухудшению общей выживаемости (HR 1,30; 95% ДИ 0,99-1,70; р=0,06) (рис.1).
Рисунок 1.
Результаты исследования DATA
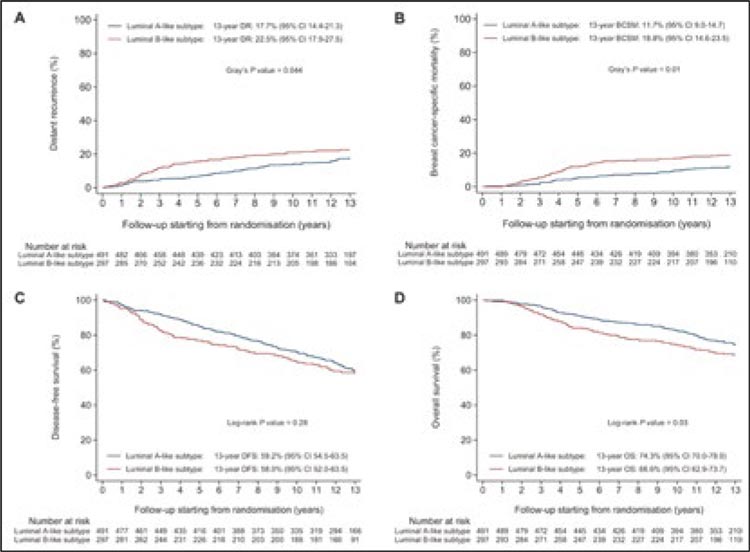
Эффективность длительной терапии анастрозолом различалась между пациентами с люминальным А и В подтипами опухоли. У пациенток с люминальным A более длительная терапия анастрозолом по сравнению с 3-летней значительно снизила 10-летний риск рецидива заболевания (sHR 0,51; 95% ДИ 0,30- 0,88; p=0,02). Однако у пациенток с люминальным B подтипом увеличение длительности терапии не дало значимых преимуществ, напротив, у этой группы больных наблюдался статистически значимо более высокий риск рецидивов (2,09; 95% ДИ 0,96-4,53; p=0,06).
У пациенток с люминальным А подтипом, получавших 6-летнюю гормональную терапию, 10-летний риск смертности также был статистически значимо ниже (sHR 0,39; 95% ДИ 0,19-0,82; p=0,01), тогда как у пациенток с люминальным В риск смертности был гораздо выше (HR 2,36; 95% ДИ 0,80-7,00; р=0,12) (рис.2).
Рисунок 2.
Результаты исследования DATA
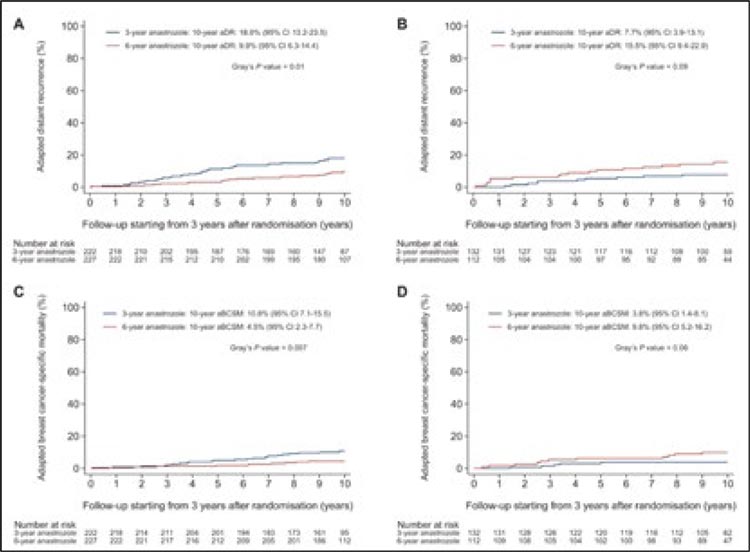
Целесообразность длительной терапии ингибиторами ароматазы остается предметом дискуссий, поскольку наряду с потенциальными преимуществами она ассоциирована с увеличением частоты нежелательных явлений, таких как остеопороз, артралгии и сердечнососудистые осложнения.
Результаты данного исследования позволяют сделать важные выводы о целесообразности длительной гормональной терапии в зависимости от биологических характеристик опухоли. У пациенток с люминальным A подтипом продление терапии анастрозолом значительно снижает риск рецидива и смертности, что подтверждает оправданность 6-летнего курса терапии. Однако у пациенток с люминальным B подтипом продление гормонального лечения не приводит к значимому снижению риска рецидива, что ставит под сомнение необходимость длительной терапии ингибиторами ароматазы в данной подгруппе.
Источник:
Lammers SWM, et al. The prognostic and predictive value of the luminal-like subtype in hormone receptor-positive breast cancer: an analysis of the DATA trial. ESMO Open. Vol.10, Issue 2, 104154
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ФАКТОРЫ ПРОГНОЗА, ВЛИЯЮЩИЕ НА ВЫЖИВАЕМОСТЬ, У ПАЦИЕНТОВ С ОСТЕОГЕННЫМИ САРКОМАМИ
Индийское исследование прогностических моделей у пациентов с остеогенными саркомами (остеосаркомами и саркомой Юинга), опубликованное в JCO, обозначает несколько факторов, связанных с низкой безрецидивной выживаемостью пациентов с подобной патологией. Для этого были проспективно проанализированы 748 клинических случаев, пациенты были пролечены в период с 2022 по 2021 гг.
Среди них:
- для неметастатических остеосарком: более высокие исходные уровни ЩФ и ЛДГ (HR, 1.63), некроз <90% опухоли (HR, 1.63), несоблюдение протокола лечения (HR 2.65). ЩФ и ЛДГ являются суррогатами активности остеобластов, и, таким образом, повышенные уровни могут указывать на повышенную агрессивность заболевания);
- для метастатических остеосарком: похожие факторы связаны с низкой БРВ, а также количество метастазов (>10);
- для пациентов с саркомой Юинга: некроз <100% (HR, 8.73), размер опухоли >8 см (HR, 2.64), несоблюдение протокола (HR, 2.84), а также невозможность проведения локального лечения (HR, 6.37).
Интересен тот факт, что несоблюдение протоколов, прерывание лечения или отказ от него оказался значимым фактором, влияющим на снижение БРВ в этой когорте пациентов. Это очень важный момент, особенно там, где проблемы лечения связаны с различными трудностями, включая финансовые, недостаток образования и отсутствие мотивации к лечению, а также логистические проблемы, связанные с необходимостью уезжать на большие расстояния и оставаться вдали от родного города на время лечения из-за недоступности онкологической помощи вблизи места жительства - что в целом характерно для стран с низким и средним уровнем дохода.
Трудности могут быть связаны и с низкой осведомленностью врачей первичного звена о том, как распознать костные саркомы и избежать непреднамеренного, неуместного хирургического вмешательства.
Источник:
Jyoti Bajpai, Laboni Sarkar, Sushmita Rath, Akash Pawar, et al. Prognostic Modeling for Bone Sarcomas Based on a Large Prospective Cohort From a Tertiary Care Cancer Center in India. JCO: Global Oncology. Feb 6, 2025
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / MORPHEUS-LIVER: ТИРАГОЛУМАБ В КОМБИНАЦИИ С АТЕЗОЛИЗУМАБОМ И БЕВАЦИЗУМАБОМ У ПАЦИЕНТОВ С МГЦР
Режим атезолизумаб/бевацизумаб стал стандартом 1-й линии при метастатическом ГЦР, продемонстрировав выигрыш в общей выживаемости в сравнении с сорафенибом. Тем не менее, медиана ОВ не превышает 2 лет. Сможет ли эскалация терапии с помощью дополнительного моноклонального АТ к TIGIT усилить эффективность иммунотаргетной комбинации (ИТК)?
В исследование MORPHEUS IB-II фазы были включены пациенты с мГЦР, классом А по Child-Pugh и рандомизированы в 2 группы: тираголумаб + ИТК (n=41) против ИТК (n=18). Первичная конечная точка – ЧОО (RECIST 1.1).
При медиане наблюдения в 20,6 мес. отмечено:
- ЧОО выше в группе экспериментального подхода (все ответы частичные): 43% против 11% (рис.1);
Рисунок 1.
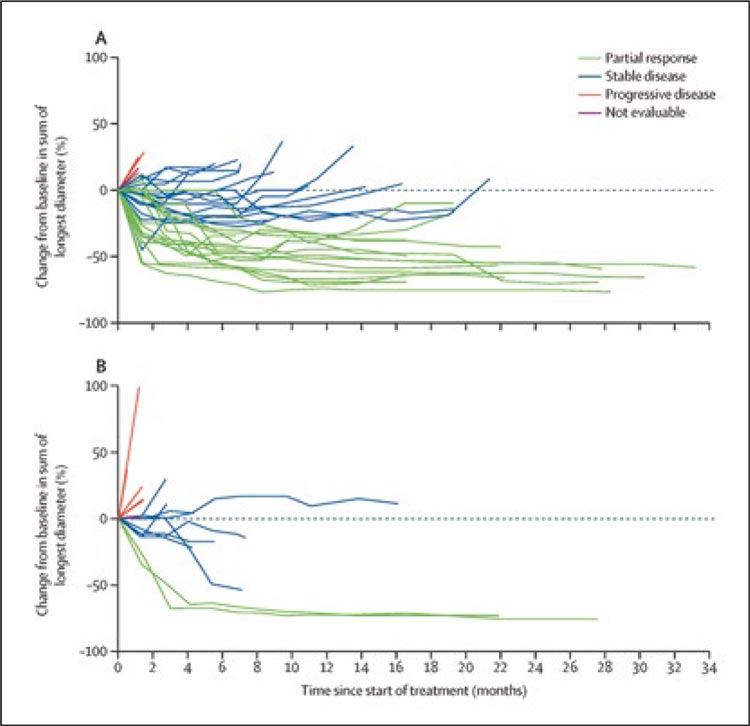
- медиана ВБП составила 12,3 против 4,2 мес. (HR 0,51; 95% CI 0,27- 0,95) в группах тираголумаба и стандарта соответственно;
- медиана ОВ – 28,9 против 15,1 мес. в пользу тираголумаба (HR 0,39; 95% CI 0,19-0,78);
- НЯ 3-4 степени отмечены у 40% пациентов в группе тираголумаба + ИТК и у 50% в группе ИТК, наиболее частые: гипертензия, повышение АСТ, протеинурия, сыпь.
В данном исследовании получены крайне перспективные результаты о преимуществе тираголумаба + ИТК в 1-й линии, однако дизайн исследования пока не позволяет высказаться однозначно в данном вопросе. С большим интересом будем ожидать итоги работы III фазы (IMbrave152/ SKYSCRAPER-14) по оценке роли тираголумаба в 1-й линии терапии мГЦР.
Источник:
Finn Richard S, et al. Tiragolumab in combination with atezolizumab and bevacizumab in patients with unresectable, locally advanced or metastatic hepatocellular carcinoma (MORPHEUS-Liver): a randomised, open-label, phase 1b2, study. The Lancet Oncology. 2025; Vol.26, Issue 2, P.214-226.
Материал подготовил Э.Р. Исраелян
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / TROPiCS-04: ФИНАЛЬНЫЕ РЕЗУЛЬТАТЫ
Не всегда ADC одинаково хорошо работают при разных нозологиях. И если сацитузумаб говитекан первым показал обнадеживающие результаты в РМЖ, то в случае уротелиальной карциноме все складывается иначе.
В журнале Annals of oncology опубликованы финальные результаты исследования III фазы TROPiCS-04; 711 пациентов с метастатическим раком мочевого пузыря, прогрессирующих после платиновой ХТ и чек-пойнт ингибиторов, рандомизировали в соотношении 1:1 на группы сацитузумаба говитекана против химиотерапии по выбору исследователя.
Первичной конечной точкой была общая выживаемость, вторичными – выживаемость без прогрессирования и частота объективных ответов. В результате:
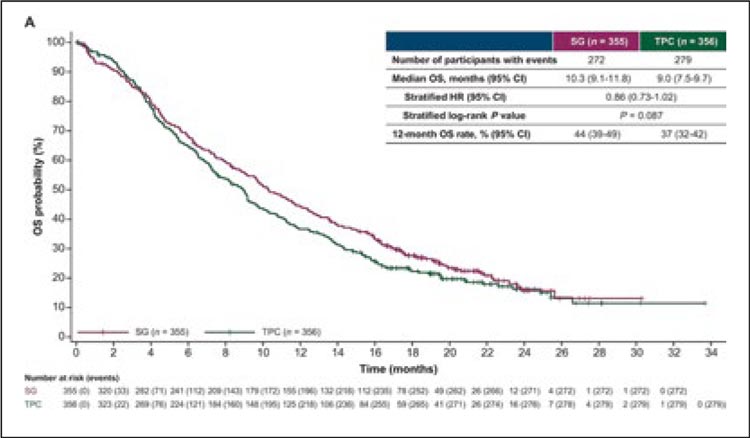
- не было достигнуто статистически значимых различий между группами в ОВ: 10,3 мес. против 9,0 мес.,
р=0,087 (рис.1);
Рисунок 1. Общая выживаемость в группах
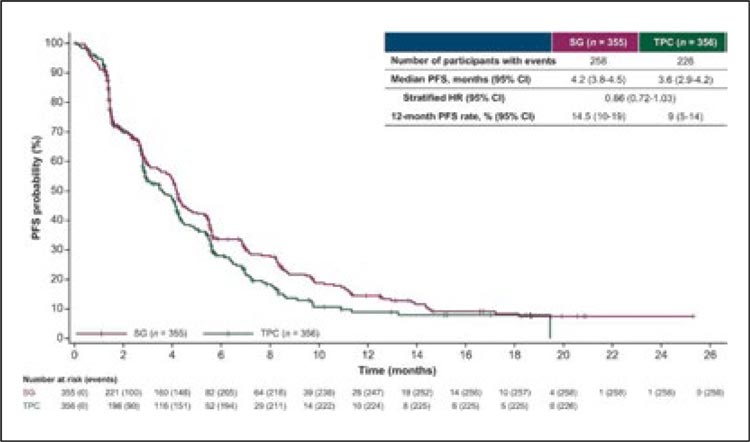
- аналогично в отношении ВБП: 4,2
мес. против 3,6 мес. (рис.2).
Правда, ЧОО в группе сацитузумаба оказалась в 2 раза выше: 23%
против 14%.
Рисунок 2. ВБП в группах
Исследованных образцов на TROP2 в популяции было всего 30%, в целом явных различий, зависящих от уровня экспрессии TROP-2, тоже получено не было, хотя кривые Каплана-Майера разошлись между группами при H-score <243.
В конечном итоге сацитузумаб говитекан не продемонстрировал значимого улучшения выживаемости по сравнению с химиотерапией в этой когорте пациентов. Так, что пока - увы.
Источник:
T. Powles et al. Sacituzumab govitecan in advanced urothelial carcinoma: TROPiCS-04, a phase III randomized trial. Annals of Oncology, February 10, 2025
Материал подготовил Э.Р. Исраелян.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / KEYLINK-006: ЭФФЕКТИВНА ЛИ ПОДДЕРЖИВАЮЩАЯ ТЕРАПИЯ ОЛАПАРИБОМ И ПЕМБРОЛИЗУМАБОМ ПРИ ДИССЕМИНИРОВАННОМ НЕПЛОСКОКЛЕТОЧНОМ НМРЛ?
Более чем у половины пациентов с немелкоклеточным раком легкого заболевание клинически манифестирует и впервые выявляется уже на стадии опухолевой диссеминации, когда потенциальные лечебные опции преимущественно ограничены самостоятельной противоопухолевой терапией [1]. Длительное время стандартом оставалось проведение платиносодержащей химиотерапии с таксанами или пеметрекседом, позволяющей добиться 8-10% 5-летней общей выживаемости (ОВ) и медианы ОВ в 12-13 месяцев. Появление в широком доступе ингибиторов контрольных точек (ИКТ) канцерогенеза и их добавление к ХТ привело к улучшению прогноза пациентов, обеспечив 5-летний контроль заболевания при PDL1 TPS >1% у 16-22% [2]. Однако выраженность терапевтического эффекта напрямую коррелировала с высоким уровнем экспрессии PD-L1 (>50%), определяющимся лишь у 14,7-24% в общей популяции пациентов и у 22,3-23% больных с плоскоклеточным раком [3-4], что мотивировало поиск новых противоопухолевых агентов, способных дополнительно улучшить результаты лечения даже при низкой или отрицательной экспрессии PD-L1. Одним их возможных направлений стало изучение возможностей добавления к иммунотерапии ингибиторов репарации ДНК (PARP-ингибиторов). Подобное сочетание аргументировалось их способностью к индукции иммунного ответа за счет активации сигнальных путей интерферона, стимуляции инфильтрации опухолевого микроокружения иммунокомпетентными клетками и даже вероятным повышением экспрессии PD-L1 [5-7].
Изучение комбинации олапариба, пембролизумаба и ХТ на основе пеметрекседа у пациентов с неплоскоклеточным диссеминированным немелкоклеточным раком легкого (НМРЛ) легло в основу исследования 3 фазы KEYLINK-006 [8]. Работа включила 672 пациента без активирующих мутаций, не получавших ранее противоопухолевую терапию или завершивших ее по поводу локализованного или местнораспространенного заболевания не менее 12 месяцев назад. Всем больным проводилась терапия в объеме 4 курсов ХТ с пембролизумабом (с трехнедельным интервалом), после чего при отсутствии признаков прогрессирования выполнялась рандомизация на 2 группы – экспериментальную (поддерживающая терапия – пембролизумаб 200 мг 1 р/3 недели + олапариб 300 мг 2 р/д, n=337) и контрольную (поддерживающая терапия – пембролизумаб 200 мг 1 р/3 недели + пеметрексед 500 мг/ м2 1 р/3 недели, n=335). Лечение продолжалось до прогрессирования заболевания, непереносимой токсичности или выполнения 31 введения пембролизумаба. В качестве первичных конечных точек были выбраны показатели общей и безрецидивной выживаемости, а факторами стратификации служили статус ECOG (0 или 1), экспрессия PD-L1 (TPS <50% или ≥50%) и степень клинического ответа перед началом рандомизации (частичный/полный ответ или стабилизация).
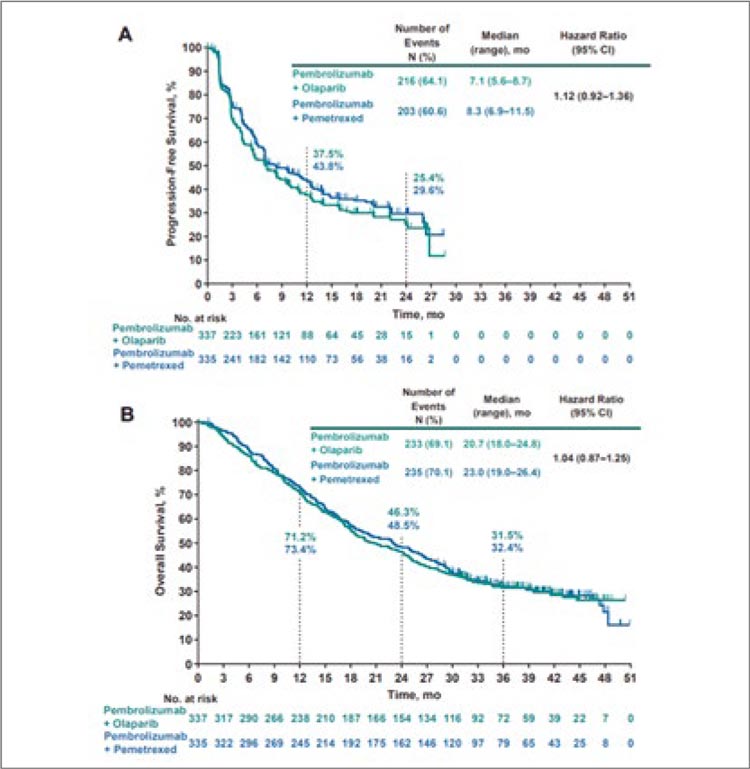
К моменту проведения финального анализа 88,1% и 90,4% пациентов в экспериментальной и контрольной группах прекратили лечение по запланированной схеме, из которых 48,1% и 43,5% соответственно получали последующие схемы терапии. При медиане наблюдения в 19,2 мес. медиана выживаемости без прогрессирования в двух группах составила 7,1 и 8,3 мес. (ОР 1,12; p=0,87) (рис.1A). Медиана общей выживаемости при медианной длительности наблюдения в 39,9 мес. составила 20,7 мес. в группе поддерживающей терапии олапарибом + пембролизумабом и 23 мес. в группе пеметрекседа + пембролизумаба (ОР 1,04; p=0,66) (рис.1B). Общая частота объективных ответов составила 16,6% и 20%, а медиана длительности ответа – 20,4 и 18,8 мес. соответственно.
Таблица 1.
Характеристика анализируемых групп
по факторам стратификации
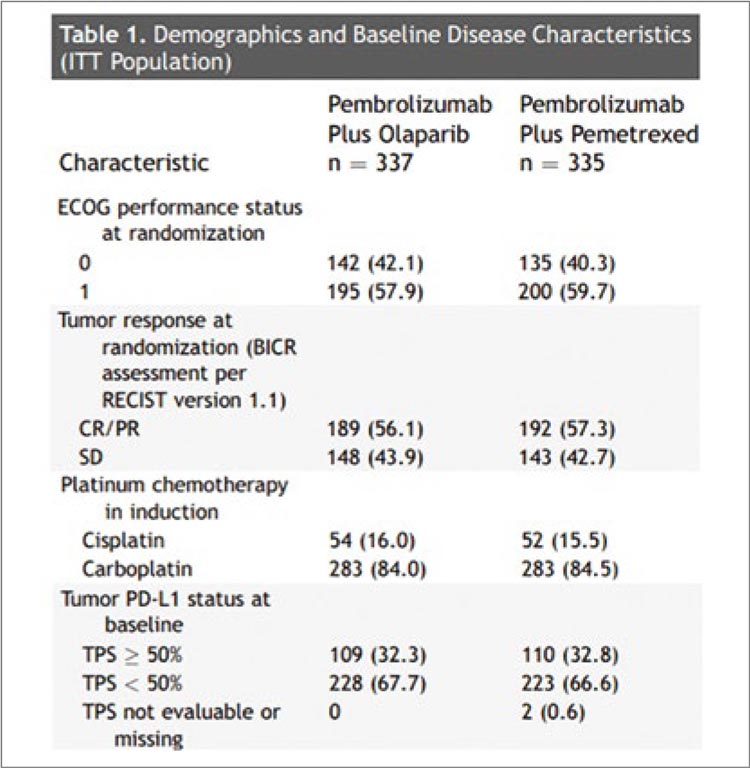
Рисунок 1.
Безрецидивная (А) и общая (B) выживаемость в
KEYLINK-006
При этом подгруппой анализ не выявил корреляции между стратификационными факторами (статус ECOG, глубина клинического ответа, экспрессия PD-L1) и эффективностью терапии (рис.2). Также не было выявлено клинически значимых различий по переносимости лечения с частотой развития нежелательных явлений 3-5 ст. у 26,1% пациентов в экспериментальной и 30,1% пациентов в контрольной группах.
Рисунок 2.
Подгрупповой анализ KEYLINK-006
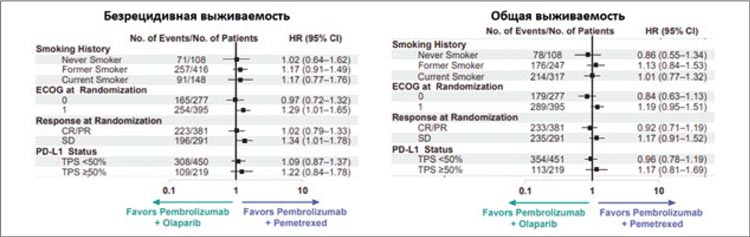
Авторы приходят к выводу, что, несмотря на гипотетическую оправданность сочетания PARPингибиторов и иммунотерапевтических агентов, на практике подобная комбинация не ассоциируется с каким-либо изменением прогноза больных. Полученные данные соотносятся с результатами предыдущих работ по включению PARP-ингибиторов в процесс лечения НМРЛ, также не показавших статистически значимых различий при добавлении олапариба или нирапариба к ИКТ [9-10]. Таким образом, данная опция пока не может быть рекомендована к применению, а стандартом попрежнему остается сочетание платиносодержащей химиотерапии с добавлением ингибиторов контрольных точек.
Источники:
- National Cancer Institute Surveillance, Epidemiology, and End Results Program. Cancer Stat Facts: lung and bronchus cancer. https://seer. cancer.gov/statfacts/html/lungb.html. Accessed: June 6, 2024.
- Shields MD, Marin-Acevedo JA, Pellini B. Immunotherapy for advanced non-small cell lung cancer: a decade of progress. Am Soc Clin Oncol Educ Book. 2021; 41: 1-23.
- Dietel M, Savelov N, Salanova R, Micke P, Bigras G, Hida T, Antunez J, Guldhammer Skov B, Hutarew G, Sua LF, Akita H, Chan OSH, Piperdi B, Burke T, Khambata-Ford S, Deitz AC. Real-world prevalence of programmed death ligand 1 expression in locally advanced or metastatic non-small-cell lung cancer: The global, multicenter EXPRESS study. Lung Cancer. 2019 Aug; 134: 174-179. doi: 10.1016/j. lungcan.2019.06.012. Epub 2019 Jun 12. PMID: 31319978.
- Liu LU, Xie B, Zhu W, He Q, Zhou J, Liu S, Tao Y, Xiao D. High expression of PD-L1 mainly occurs in non-small cell lung cancer patients with squamous cell carcinoma or poor differentiation. Oncol Res. 2023 May 24; 31(3): 275-286. doi: 10.32604/ or.2023.028227. PMID: 37305382; PMCID: PMC10229306.
- Shen J, Zhao W, Ju Z, et al. PARPi triggers the STINGdependent immune response and enhances the therapeutic efficacy of immune checkpoint blockade independent of BRCAness. Cancer Res. 2019; 79: 311-319.
- Wang Z, Sun K, Xiao Y, et al. Niraparib activates interferon signaling and potentiates anti-PD-1 antibody efficacy in tumor models. Sci Rep. 2019; 9: 1853.
- Jiao S, Xia W, Yamaguchi H, et al. PARP inhibitor upregulates PD-L1 expression and enhances cancerassociated immunosuppression. Clin Cancer Res. 2017; 23: 3711-3720.
- Gray JE, Schenker M, Şendur MAN, Leonova V, Kowalski D, Kato T, Orlova R, Yang JC, Langleben A, Pilz A, Ungureanu A, Mak MP, De Angelis F, Aggarwal H, Zimmer Z, Zhao B, Shamoun M, Kim TM. The Phase 3 KEYLYNK-006 Study of Pembrolizumab Plus Olaparib Versus Pembrolizumab Plus Pemetrexed as Maintenance Therapy for Metastatic Nonsquamous NSCLC. J Thorac Oncol. 2025 Feb; 20(2): 219-232. doi: 10.1016/j.jtho.2024.10.026. Epub 2024 Nov 7. PMID: 39521434.
- Ramalingam SS, Thara E, Awad MM, et al. Jasper: phase 2 trial of firstline niraparib plus pembrolizumab in patients with advanced non-small cell lung cancer. Cancer. 2022; 128: 65-74.
- Ahn MJ, Bondarenko I, Kalinka E, et al. Durvalumab in combination with olaparib versus durvalumab alone as maintenance therapy in metastatic NSCLC: the phase 2 ORION study. J Thorac Oncol. 2023; 18: 1594-1606.
Материал подготовил И.М. Боровков
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НОВАЯ РОЛЬ СА-125
Медуллярная карцинома почки (RMC) — это высокоагрессивная злокачественная опухоль, одна из типичных характеристик которой - потеря супрессора опухоли SMARCB1. Она в основном поражает молодых людей, преимущественно африканского происхождения с серповидноклеточной анемией, устойчива к традиционным методам лечения других почечно-клеточных карцином. Целью данного исследования было выявление потенциальных биомаркеров для раннего выявления и мониторинга течения RMC.
Интегрированное профилирование первичных нелеченых опухолевых тканей с RMC и сопоставленных парных соседних контрольных тканей почек было выполнено с использованием секвенирования РНК и иммунопреципитации гистонового хроматина. Экспрессия сывороточного ракового антигена 125 (CA-125) была проспективно оценена у 47 пациентов с RMC. Функциональные исследования были проведены в линиях клеток RMC для оценки эффектов повторной экспрессии SMARCB1.
В результате, MUC16, кодирующий CA-125, был идентифицирован как один из самых высокорегулируемых генов в тканях RMC. Повышенные уровни сывороточного CA-125 были обнаружены у 31 из 47 (66%) пациентов с RMC и значительно коррелировали с метастатической опухолевой нагрузкой (P = 0,03). Функциональные исследования в клеточных линиях RMC показали, что ре-экспрессия SMARCB1 значительно снижала экспрессию MUC16.
Помимо диагностических целей, MUC16 проявил свойства терапевтической мишени. Ре-экспрессия SMARCB1 в клеточных линиях медуллярной карциномы почки подавила MUC16/СА-125. Авторы инициировали клиническое исследование биспецифической терапии MUC16 х CD3 при злокачественных опухолях с дефицитом SMARCB1.
Исследование определяет СА-125 как клинически значимый биомаркер для медуллярной карциномы почки, что может позволить проводить неинвазивный мониторинг лечебного процесса и ответа опухоли. Будущие исследования, возможно, будут включать изучение MUC16 таргетной терапии в объединении с СА-125 с ctDNA для более прецизионного наблюдения. Работа с большим энтузиазмом была воспринята научным сообществом, авторы получили немало комплиментов и поздравлений в соцсетях: онкологи, вероятно, получили еще один эффективный биомаркер для медуллярного рака почки.
Источник:
Sandra L. Grimm et al. CA125 as a Biomarker in Renal Medullary Carcinoma: Integrated Molecular Profiling, Functional Characterization, and Prospective Clinical Validation. Clin Cancer Res OF1–OF12.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / РАК МОЧЕВОГО ПУЗЫРЯ: ДВОЙНАЯ ИММУНОТЕРАПИЯ В КОМБИНАЦИИ С ЛТ В КАЧЕСТВЕ СЕЛЕКТИВНОГО ОРГАНОСОХРАНЯЮЩЕГО ПОДХОДА
Отдельной категории пациентов с локализованным раком мочевого пузыря (РМП) ввиду различных причин невозможно провести неоадъювантную терапию, альтернативным подходом в такой ситуации является химиолучевая или лучевая терапия в самостоятельном варианте.
В исследование IMMUNOPRESERVE включены больные с сТ2-Т4N0 РМП (n=32), которым проведена ТУР, затем 3 курса двойной иммунотерапии (ИТ) – дурвалумаб + тремелимумаб – с параллельным проведением лучевой терапии (46 Гр на малый таз и 64 Гр на мочевой пузырь), затем рестадирующий ТУР. Пациенты, достигшие полного ответа (ПО), оставались под динамическим наблюдением, в случае наличия жизнеспособной опухолевой ткани проводилась радикальная цистэктомия. Первичная конечная точка - частота полного ответа.
При медиане наблюдения в 27 мес.: • Полный ответ достигнут у 81% пациентов, резидуальный мышечно-инвазивный РМП отмечен у 2 больных; • 2-летняя орган-интактная выживаемость, безметастатическая выживаемость и ОВ составили 65%, 83% и 84% соответственно;• 2-летняя частота немышечно- и мышечно-инвазивного рецидивов составила 3% и 19% соответственно.
Органосохраняющий подход, безусловно, занимает все бОльшие позиции в лечении МИРМП, особенно в комбинации с ИТ. Несмотря на продемонстрированные приемлемые результаты, у работы есть некоторые ограничения: малое количество пациентов, отсутствие радиомодификации и группы контроля.
С течением времени наши возможности в лечении МИРМП расширяются, и уже ИТ можно совмещать не только с НАХТ, но и с ЛТ. Надо лишь понять наиболее оптимальный алгоритм в периоперационном подходе.
Источник:
Xavier Garcia-del-Muro et al. Bladder Preservation with Durvalumab plus Tremelimumab and Concurrent Radiotherapy in Patients with Localized Muscle-Invasive Bladder Cancer (IMMUNOPRESERVE): A Phase II Spanish Oncology GenitoUrinary Group Trial. Clin Cancer Res 2025;31:659–66
Материал подготовил Э.Р.Исраелян.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НОВЫЙ ЦВЕТ ТЕРАПИИ РАКА ПРОСТАТЫ: ФИОЛЕТОВЫЙ. VIOLET STUDY ДЛЯ ТЕРБИЯ-161-PSMA
Австралийские авторы недавно анонсировали важное событие: первое клиническое исследование "VIOLET" с тербием-161 PSMA для лечения рака простаты. «Мы не только не наблюдали дозолимитирующей токсичности в течение 6 циклов до 7,4 ГБк у 30 пациентов, прошедших лечение на сегодняшний день, но и завершили набор пациентов!»
Итак, вспомним таблицу Менделеева: элемент Тèрбий (химический символ — Tb, от лат. Terbium) шестого периода периодической системы химических элементов Д.И. Менделеева с атомным номером 65. Название восходит к поселению Иттербю в Швеции. Относится к семейству лантаноидов (иттриевая подгруппа). Как и любой лантаноид, тербий принадлежит к редкоземельным элементам и переходным металлам. Простое вещество тербий — мягкий металл серебристо-белого цвета. Единственным стабильным изотопом тербия является 159Tb. Самым долгоживущим радиоактивным изотопом является 158Tb с периодом полураспада 180 лет.
В настоящее время в ядерной медицине интенсивно развиваются подходы, связанные с сочетанием диагностики и терапии. При этом роль терапевтического фактора играет корпускулярное излучение, поражающее опухолевые клетки, а роль диагностического - фотонное излучение, позволяющее выполнить молекулярную визуализацию методом однофотонной эмиссионной компьютерной томографии (ОФЭКТ). В связи с этим большой интерес представляют радионуклиды, сочетающие низкоэнергетическое бета-излучение с мягким гамма-излучением. Эти требованиям идеально соответствует радионуклид 161Tb (Т½ - 6,89 сут; Eβav=154 кэВ; Еγ=74,6 кэВ (10%)). По своим ядерно-физическим характеристикам он близок к 177Lu, однако, как показано в экспериментах на животных, несколько превосходит его по терапевтическим свойствам [1]. Преимуществом 161Tb в сравнении с 177Lu является его особенность излучать при радиоактивном распаде Оже-электроны, действующие как дополнительный поражающий фактор в клеточных масштабах. Их малый радиус излучения позволяет им высвобождать всю свою энергию непосредственно в раковых клетках, практически не повреждая соседние здоровые клетки (см. рис.).
Рисунок 1.
[161Tb]Tb-PSMA-I&T Оже электроны и конверсионные электроны от [161Tb]
Tb-PSMA-I&T обладают высокой линейной передачей энергии, доставляя большую
дозу излучения к микрометастазам (как показано на увеличенной клетке рака простаты
справа). Напротив, b-частицы передают свою энергию на большем пробеге (слева)
и имеют меньшую вероятность причинения летального ущерба микрометастазам
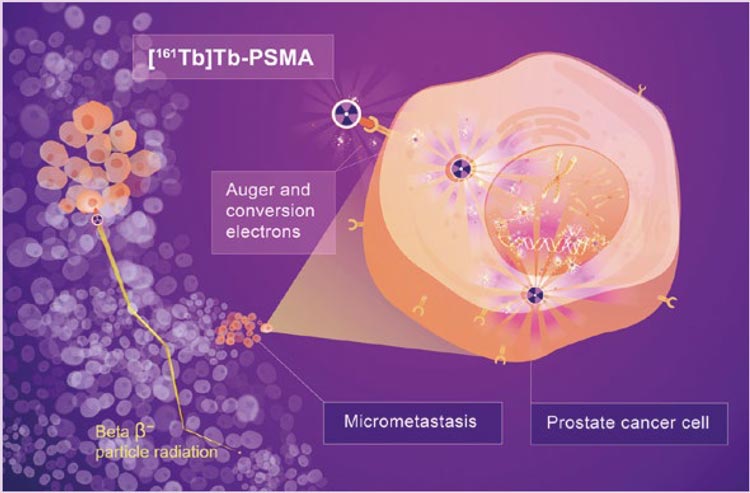
До настоящего времени работы по тербию-161 в мире находились на этапе доклинических исследований, предполагается использование его в виде таргетных препаратов на основе пептидов и антител, тогда как аналогичные препараты на основе лютеция-177 уже получили одобрение FDA для лечения метастатического рака простаты. В настоящее время 161Tb получают облучением нейтронами 160Gd через промежуточное образование 161Gd по реакции 160Gd(n,γ)161Gd→161Tb.
VIOLET — это австралийское открытое одногрупповое одноцентровое исследование фазы I/II с эскалацией дозы, разработанное для оценки безопасности и эффективности [161Tb] Tb-PSMA-I&T у пациентов с мКРРПЖ [2]. Фаза I с эскалацией дозы — это традиционный 3+3 дизайн с 3 заранее заданными уровнями активности. Период оценки дозо-лимитирующей токсичности составляет 6 недель с 1-го дня цикла. Пациенты с мКРРПЖ, у которых наблюдалось прогрессирование по крайней мере на одной линии химиотерапии таксанами (если нет медицинских противопоказаний) и ингибиторами андрогеновых рецепторов, будут включаться в это исследование. Анализ данных продолжается, первые результаты уже в копилке авторов и будут представлены в 2025 году.
Источники:
- Eur. J. Nucl. Med. Mol. Imaging (2014) 41:1907-1915)
- James P. Buteau et al. Clinical Trial Protocol for VIOLET: A Single-Center, Phase I/II Trial Evaluation of Radioligand Treatment in Patients with Metastatic Castration-Resistant Prostate Cancer with [161Tb]Tb-PSMA-I&T. J Nucl Med 2024; 00:1–8 DOI: 10.2967/ jnumed.124.267650
НОВОСТИ ASCO GI 2025 / РАК ЖЕЛУДКА
EORTC-1203 GITC «INNOVATION»: сравнение эффективности комбинации химиотерапии и трастузумаба с или без пертузумаба в периоперационной химиотерапии рака желудка
В исследование было включено 172 пациента с HER-2 положительным резектабельным РЖ (Ib-III стадии). Пациенты были рандомизированы в соотношении 1:2:2:
- группа пациентов, получивших только химиотерапию, (n=35);
- группа пациентов, получивших химиотерапию + трастузумаб (8 мг/к, затем 6 мг каждые 3 недели) (n=67);
- группа пациентов, получивших химиотерапию + трастузумаб + пертузумаб 840 мг, каждые 3 недели (n=70).
В качестве периоперационного режима химиотерапии изначально применялся режим цисплатин + капецитабин (3 курса до и после операции).
После публикации FLOT-4 (AlBatran, Lancet 2019) протокол был изменен. Затем применялся режим FLOT или FOLFOX/CAPOX в течение 4 циклов. После оперативного лечения проведение ХТ в группах с таргетной терапией было продолжено до 17 курсов.
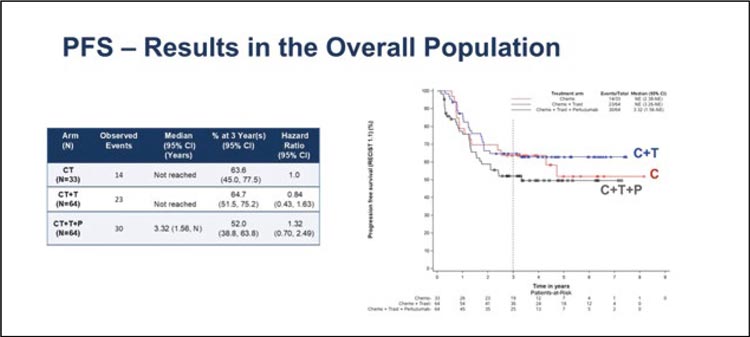
Частота выраженных лечебных патоморфозов (mpRR) в группах составила 33,3%, 53,3% и 37,9%. А ВБП (ОР 0,88; 90% ДИ 0,51-1,53) и ОВ (0,89; 95% ДИ 0,42-1,88) статистически значимо не различались между группами с химиотерапией и химиотерапии с трастузумабом (рис.1,2).
Рисунок 1.
График общей выживаемости
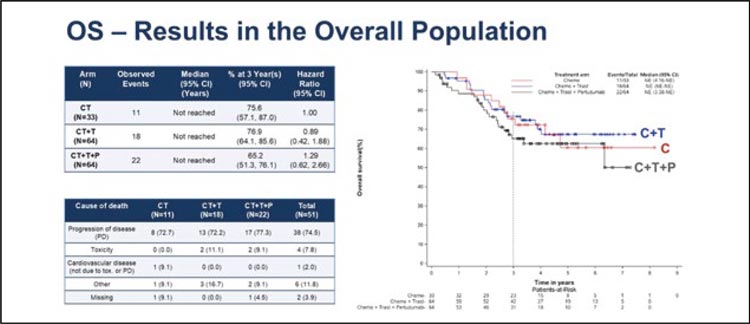
Рисунок 2.
График выживаемости без прогрессирования
Рандомизированное исследование II фазы Trigger: комбинация химиотерапии с трастузумабом у пациентов с HER2-положительной аденокарциномой желудка/пищеводно-желудочного перехода с обширными метастазами в лимфатические узлы
В исследование было включено 46 пациентов с HER2-положительным раком желудка с N+, которые были рандомизированы в две группы:
- проведение предоперационной химиотерапии с S-1/цисплатином (n=22);
- ХТ плюс трастузумаб (8 мг/кг, затем 6 мг/кг) (n=24).
- После гастрэктомии адъювантная химиотерапия с S-1 проводилась в течение года в обеих группах. Первичной конечной точкой была общая выживаемость.
При медианном периоде наблюдения в 4,1 года трехлетняя общая выживаемость составила 68,2% в группе ХТ и 78,9% в группе ХТ + трастузумаб (ОР 0,698; 95% ДИ 0,221-2,209), а трехлетняя ВБП составила 39,3% в группе ХТ и 62,3% в группе ХТ + трастузумаб (ОР 0,562; 95% ДИ 0,229-1,377) (рис.3).
Рисунок 3.
Результаты исследования Trigger
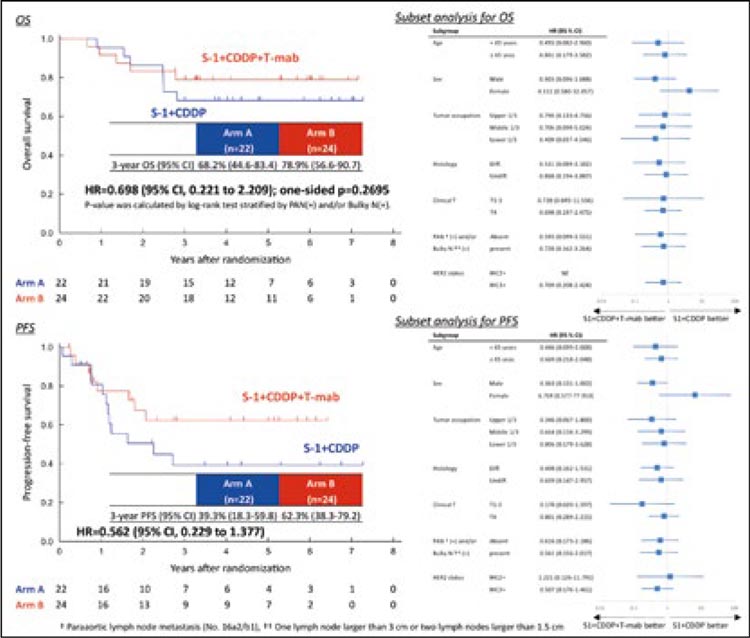
Результаты лечения пациентов с метастатическим раком желудка, с изолированными метастазами по брюшине после химиотерапии и циторедуктивной операцией с внутрибрюшинной химиотерапией (HIPEC)
В исследование было включено 34 пациента с метастатическим раком желудка, у которых в течение 24 недель не было зафиксировано прогрессирование опухолевого процесса после проведенной химиотерапии.
В качестве химиотерапии применялся паклитаксел 50 мг/м2, S-1 80 мг/м2 и IP PTX (интраперитонеальное внутрибрюшное введение) 20 мг/м2, либо XELOX и IP PTX 40 мг/м2. В качестве внутрибрюшной химиотерапии применялся цисплатин 50 мг/м2 при 40° в течение 60 минут (рис.4).
Рисунок 4.
Дизайн исследования
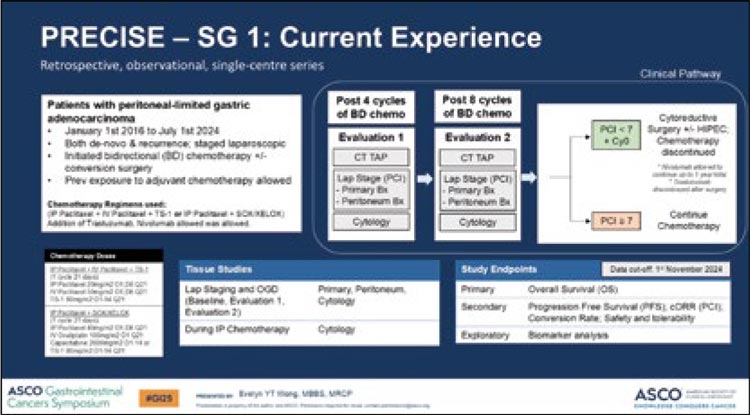
Проведение циторедуктивного оперативного лечения было показано только пациентам с индексом перитонеального канцероматоза (PCI) 7 при достижении контроля заболевания в течение 24 недель после проведенной химиотерапии.
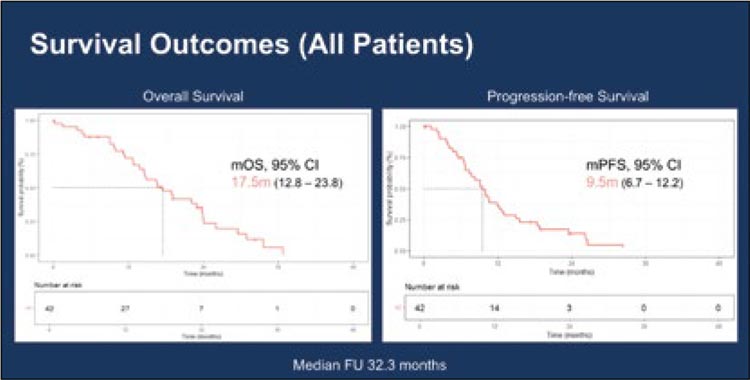
Медиана ВБП и ОВ составили 9,1 и 16,5 мес. (рис.5).
Рисунок 5.
График общей выживаемости и выживаемости
без прогрессирования
7 пациентов (20,6%) перенесли циторедуктивное оперативное лечение со средним диапазоном PCI 1 (0-15,0). Медиана ОВ у пациентов, подвергшихся циторедуктивному оперативному лечению, составила 23,8 мес. в сравнении с пациентами без него – 14,6 мес. (p=0,4) (рис.6). У пациентов с PCI<7 в сравнении с пациентами с PCI≥7 составила 23,8 и 14,6 мес. (p=0,63) (рис.7).
Рисунок 6.
График общей выживаемости и выживаемости без
прогрессирования пациентов в зависимости от проведенного
оперативного лечения
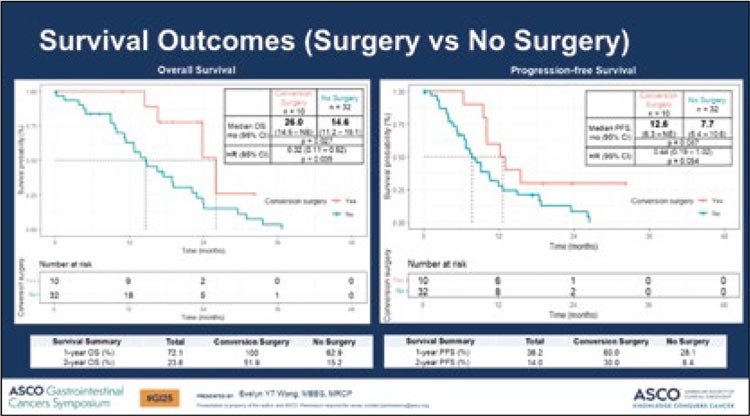
Рисунок 7.
График общей выживаемости и выживаемости
без прогрессирования пациентов в зависимости от индекса
перитонеального канцероматоза
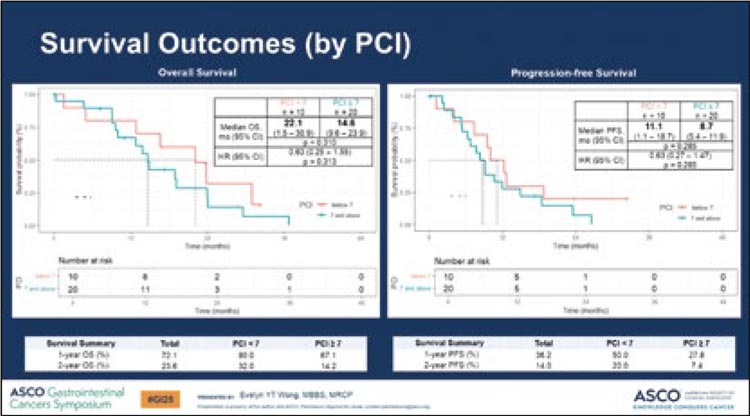
Материал подготовила Абдулаева Рукият Шамильевна
Врач-онколог отделения
противоопухолевой лекарственной терапии №2
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
Москва
а
НОВОСТИ ASCO GI 2025 / КОЛОРЕКТАЛЬНЫЙ РАК
Комбинированная иммунотерапия в лечении КРР с MSI/dMMR в исследовании CheckMate 8HW
Ранее уже были продемонстрированы преимущества комбинированной иммунотерапии перед химиотаргетной терапией 1 линии у пациентов с КРР и MSI/dMMR. На ASCO GI 2025 представлены данные по другой первичной точке исследования – времени без прогрессирования (ВБП) при сравнении комбинации ниволумаб + ипилимумаб против ниволумаба в исследовании CheckMate 8HW [1]. Пациенты с неоперабельным или мКРР и статусом MSI/dMMR, не получавшие иммунотерапию, были рандомизированы в 3 группы в соотношении 2:2:1 (Ниво + Ипи, Ниво, химиотерапия ± таргетная терапия). Пациенты, которые получили ≥2 линий терапии, были рандомизированы в соотношении 1:1 в группы Ниво + Ипи или Ниво. Иммунотерапию в качестве 1 линии лечения получали 57% пациентов. Иммунотерапия проводилась до прогрессирования заболевания, непереносимой токсичности или максимум в течение 2 лет
При медианном наблюдении в 47,0 мес. (16,7-60,5) комбинированная иммунотерапия продемонстрировала значимое и достоверное улучшение ВБП (HR 0,62; 95% ДИ 0,48-0,81; P=0,0003) по сравнению с ниволумабом в монорежиме (рис.1). Частота объективного ответа также выше (71% по сравнению с 58%; P=0,0011); наилучший общий ответ на прогрессирующее заболевание был зарегистрирован у 10% и 19% пациентов соответственно. В подгрупповом анализе различий между режимами в отношении ВБП не было только при синдроме Линча. В первом рандомизированном исследовании по сравнению иммунотерапии с двумя и одним агентом при MSI/dMMR мКРР продемонстрирована лучшая ВБП при комбинированной иммунотерапии во всех линиях лечения с приемлемым профилем безопасности. Учитывая выход кривых на плато у ответивших пациентов, очевидно, что ипилимумаб необходим не всем пациентам. Необходимо дождаться данных по общей выживаемости. Как и ожидалось, на комбинированной иммунотерапии реже наблюдалось прогрессирование заболевания как лучший ответ на терапию (10% против 19%) (рис.2); 10% больных – это заставляет задуматься о поиске дополнительных характеристик и предикторов ответа на терапию при MSI. Время до достижения ответа среди ответивших пациентов оказалось одинаковое (2,8 мес.), повидимому, добавление ипилимумаба не является спасением в случаях, когда заболевание опережает врача.
Рисунок 1.
ВБП в исследовании
CheckMate 8HW
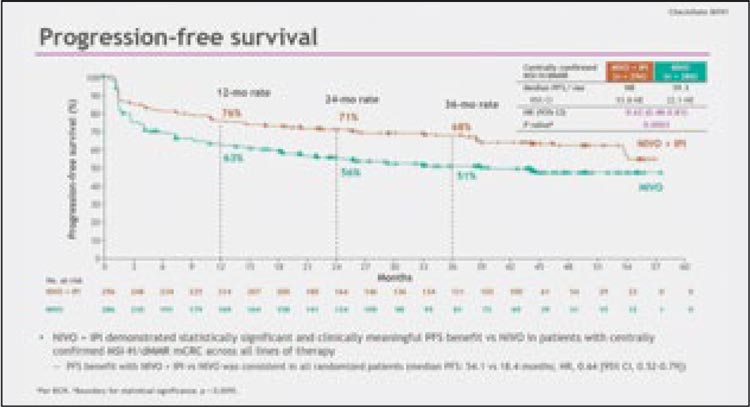
Рисунок 2.
Ответ на иммунотерапию
в исследовании CheckMate 8HW
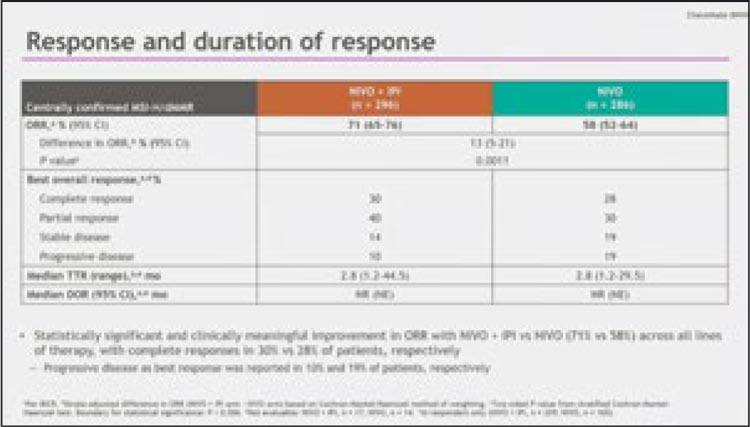
Неоадъювантная терапия КРР в виде однократного введения пембролизумаба в исследовании RESET-C
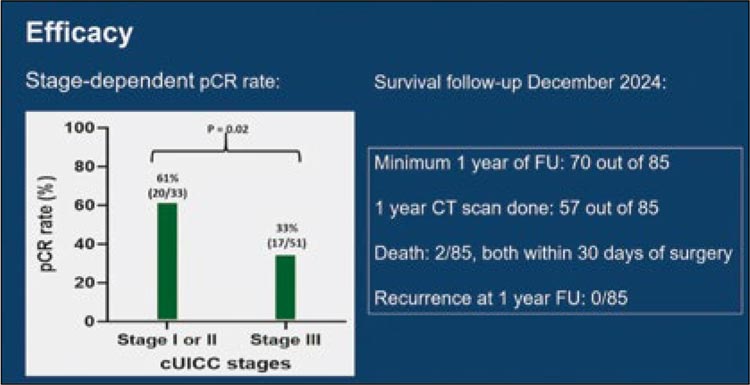
Неоадъювантное лечение ингибиторами иммунных контрольных точек уже показало высокую эффективность в неоадъювантном режиме у пациентов с локализованным колоректальным раком с MSI/dMMR. Существует ряд данных, указывающих на то, что снижение дозы этих препаратов или длительности терапии не ухудшает результаты лечения. В исследовании RESET-C (NCT05662527) II фазы показана эффективность и безопасность однократного неоадъювантного введения пембролизумаба 4 мг/кг (максимум 400 мг) у 85 пациентов с резектабельным раком толстой кишки I-III стадии и dMMR [2]. Первичной конечной точкой был показатель полного патологического ответа (pCR) в соответствии с градацией регрессии опухоли по Mandard (метод Clopper-Pearson).
Зарегистрированы частота pCR у 44% больных (37/84; 95% ДИ 33-55) и частота выраженного патоморфоза у 57% (48/84; 95% ДИ 46-68) (рис.3). Это является сопоставимым с более привычными вариантами проведения неоадъювантной иммунотерапии. Значительно более высокая частота pCR наблюдалась у пациентов с заболеванием I-II стадии (20/33) по сравнению с III стадией (17/51) (61% против 33%; p=0,02). То есть один цикл неоадъювантного пембролизумаба оказался эффективным и безопасным у пациентов с локализованным раком толстой кишки с dMMR. Для большинства пациентов с клинической стадией заболевания I-II одного цикла было достаточно для достижения pCR. Требуются данные по отдаленным результатам для определения дальнейшей тактики у таких пациентов после операции.
Рисунок 3.
Полные ответы в исследовании RESET-C
Адъювантное применение аспирина снизило частоту рецидивов при КРР с мутациями в пути PIK3 в исследовании ALASCCA
Как известно, среди больных КРР II-III стадии у 20-40% развивается метастатическое заболевание. Аспирин снижает частоту аденом и КРР у пациентов с высоким риском. Кроме того, наблюдательные исследования показывают, что лечение аспирином после постановки диагноза улучшает безрецидивную выживаемость в неотобранных группах населения. Также ретроспективные результаты показывают, что соматические мутации PIK3CA предсказывают ответ на лечение, но требуют проверки в рандомизированных исследованиях.
В рандомизированное исследование ALASCCA [3] были включены больные раком прямой кишки I-III стадии или раком толстой кишки II-III стадии, у которых наблюдались соматические изменения в сигнальном пути PI3K. Пациенты были рандомизированы для приема 160 мг аспирина в день или плацебо, прием начинался в течение трех месяцев после операции и продолжался в течение трех лет. Чтобы определить отношение рисков (HR) 0,36 для первичного результата времени до рецидива, оцениваемого через 3 года, с 80% мощностью и альфа 0,05, на каждую группу требовалось 150 пациентов с мутациями PIK3CA в экзоне 9 и/или 20 (группа A). Для вторичных анализов потребовалось дополнительно 300 пациентов с другими соматическими мутациями пути PI3K (PIK3CA вне экзона 9/20, PIK3R1 или PTEN – группа B).
Всего было обследовано 3508 пациентов на предмет соматических изменений в пути PI3K. Из 2980 больных с окончательным геномным анализом у 1103 пациентов (37%) было обнаружено изменение в пути PI3K: 515 пациентов (17,3%) в группе A и 588 пациентов (19,7%) в группе B. Всего было рандомизировано 626 пациентов. После трех лет наблюдения HR для времени до рецидива при сравнении аспирина с плацебо составили 0,49 (95% ДИ 0,24-0,98; p=0,044) в группе A и 0,42 (95% ДИ 0,21-0,83; p=0,013) в группе B. Для ВБПБ HR составили 0,61 (95% ДИ 0,34-1,08; p=0,091) в группе A и 0,51 (95% ДИ 0,29-0,88; p=0,017) в группе B (рис. 4).
Рисунок 4.
Частота рецидивов КРР в исследовании ALASCCA
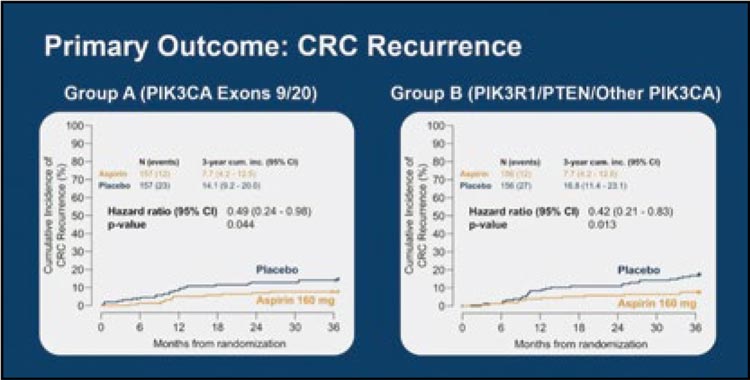
Первичная конечная точка была достигнута. Адъювантное лечение 160 мг аспирина ежедневно в течение трех лет снизило частоту рецидивов у пациентов с КРР с соматическими изменениями в сигнальном пути PI3K. Применение аспирина значимо уменьшило частоту прогрессирований в течение 3 лет на 7% в 1 группе и 9,1% во второй группе. Также наблюдалось увеличение 3-летней ВБПБ. Эти результаты могут привести к изменениям в клинической практике примерно у трети пациентов с КРР.
Принцип тотального неоадъюванта при ранних стадиях рака прямой кишки в исследовании NEO (CCTG СO.28) [4]
Учитывая возможность достижения полного клинического ответа (cCR), кажется целесообразным изучить неоадъювантную химиотерапию и при ранних стадиях (T1-3N0) для возможного избежания или отсрочки серьезного хирургического вмешательства при раке прямой кишки, особенно низкой локализации. Так, в исследование II фазы NEO включались больные средне- и нижнеампулярным раком прямой кишки со стадией T1-3N0M0. Им проводили 3 месяца терапии по схеме FOLFOX или XELOX и в дальнейшем выполняли эндоскопическую эксцизию. В случае недостижения pCR или pT1а рекомендовалось выполнять полноценную хирургию (TME). В 57% случаях удалось реализовать органосохраняющий подход, а при добавлении пациентов, которые отказались от TME, это уже 74%. Трехлетняя выживаемость без признаков болезни составила 94,7%.
Существует ряд вопросов к такому подходу, и в настоящее время эти данные никак не повлияют на существующие стандарты. Однако в данной работе были представлены интересные данные по применению циркулирующей опухолевой ДНК (цоДНК) в качестве критерия отбора пациентов на TME (рис.5). Всего лишь у 8,7% пациентов после завершения ХТ выявлялась цоДНК. Всем им по патоморфологическим критериям рекомендовалась ТМЕ. Данный маркер может быть перспективным для отбора пациентов на TME в случае проведения неоадъювантной химиотерапии при раке прямой кишки.
Рисунок 5.
Связь цоДНК и выживаемостью в исследовании NEO
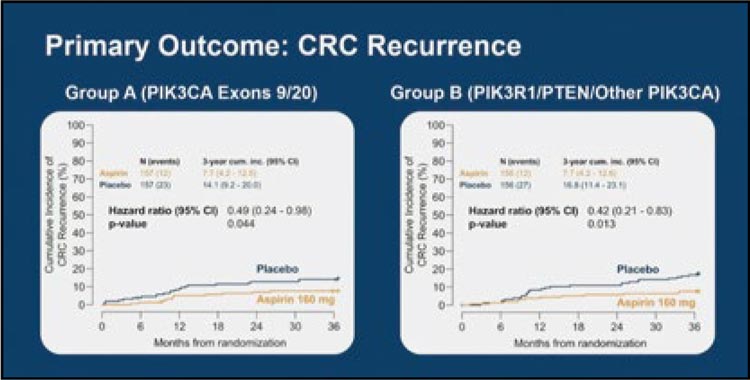
Источники:
- Thierry Andre, et al. First results of nivolumab (NIVO) plus ipilimumab (IPI) vs NIVO monotherapy for microsatellite instability-high/mismatch repair-deficient (MSI-H/dMMR) metastatic colorectal cancer (mCRC) from CheckMate 8HW. Journal of Clinical Oncology. 2025; Vol.43, Issue 4_suppl. https://doi.org/10.1200/ JCO.2025.43.4_suppl.LBA143.
- Camilla Qvortrup, et al. Single-cycle neoadjuvant pembrolizumab in patients with stage I-III MMR-deficient colon cancer: Final analysis of the RESET-C study. Journal of Clinical Oncology. 2025; Vol.43, Issue 4_suppl. https://doi. org/10.1200/JCO.2025.43.4_suppl.19.
- Anna Martling, et al. Low-dose aspirin to reduce recurrence rate in colorectal cancer patients with PI3K pathway alterations: 3-year results from a randomized placebo-controlled trial. Journal of Clinical Oncology. 2025; Vol.43, Issue 4_suppl. https:// doi.org/10.1200/JCO.2025.43.4_suppl. LBA125.
- Jonathan M. Loree, et al. Tumourfree ctDNA detection as a decision tool to support organ preservation in node-negative rectal cancer undergoing neoadjuvant chemotherapy, excision, and observation in the phase II NEO trial (CCTG CO.28). Journal of Clinical Oncology. 2025; Vol.43, Issue 4_suppl. https://doi.org/10.1200/JCO.2025.43.4_ suppl.20.
Материал подготовил Макиев Георгий Георгиевич,
врач-онколог отделения противоопухолевой терапии №2
ФГБУ «НМИЦ онкологии им. Н.Н.
Блохина» Минздрава России
НОВОСТИ ASCO GU 2025 / РАК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
С 13 по 15 февраля в Сан-Франциско прошел очередной конгресс ASCО Genitourinary 2025. Давайте рассмотрим последние новости с конгресса и решим, позволят ли новые данные изменить нашу реальную практику уже сейчас.
Радикальная простатэктомия vs лучевая терапия при раке предстательной железы (РПЖ) высокого риска: индивидуальные данные пациентов из двух исследований III фаз
Согласно рекомендациям NCCN, больным РПЖ высокого риска (ПСА >20 нг/мл, сумма баллов по Глисону 8-10, с ≥Т3) возможно как проведение ДЛТ с АДТ, так и радикальной простатэктомии (РПЭ). Roy S. с соавторами решили оценить, какому способу лечения стоит отдать предпочтение в рамках систематического анализа, включившего 2 крупных исследования в популяции пациентов высокого риска – CALGB 90203 (РПЭ vs неоадъювантная терапия доцетакселом + АДТ + РПЭ) [1] и RTOG0521 (АДТ + ДЛТ vs АДТ + ДЛТ + доцетаксел) [2] (рис.1). Первичной конечной точкой выбрана оценка кумулятивной частоты появления дистантных метастазов, оцененная методом IPTW (inverse probability of treatment weighting).
Рисунок 1.
Изучаемые когорты пациентов в данном анализе
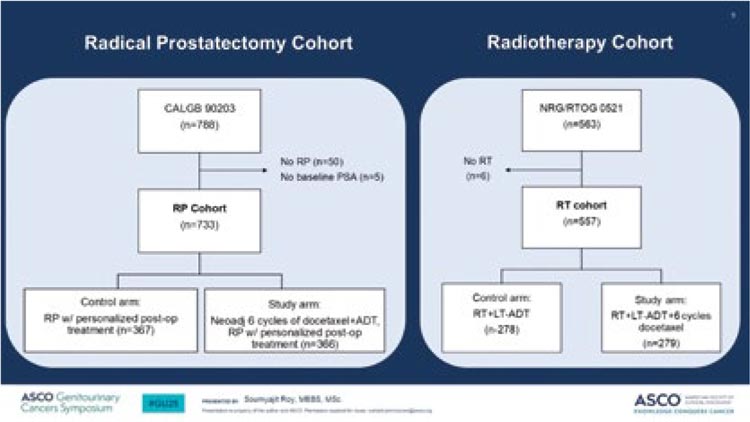
Во всей когорте 8-летний риск развития метастатического поражения оказался выше в группе хирургического лечения – 23% vs 16% (ОР 0,56; 95%ДИ 0,38-0,81; р=0,002) (рис.2А). В группах контрольных (рис. 2В) и экспериментальных подходов (рис. 2С) также продемонстрировано преимущество ЛТ над РПЭ (по р=0,03). И лишь триплетный/квадриплетный режим (доцетаксел + АДТ + РПЭ +/- ЛТ) не уступил ЛТ (рис. 2D). Поставлена ли точка в спорах между онкоурологами и радиотерапевтами, в какой все-таки стационар попадет больной с РПЖ высокого риска? Кажется, что доказательная база ЛТ стала чуть больше. К тому же триплет – абиратерона ацетат (АА) + АДТ + ЛТ – стал текущим стандартом в данной популяции пациентов [3]. Тем не менее продолжается проспективное исследование SPCG-15, сравнивающее РПЭ и ЛТ среди пациентов с РПЖ с ≥Т3 – может, у хирургии появится шанс [4]?
Рисунок 2.
Кумулятивный риск развития дистантных
метастазов: А – во всей группе, В – в группах ЛТ+АДТ vs
РПЭ+/-ЛТ, С – РПЭ + неоадъювантный доцетаксел + АДТ +/-
ЛТ vs ЛТ + АДТ и адъювантный доцетаксел, D – ЛТ + АДТ vs
Доцетаксел + АДТ + РПЭ +/- ЛТ
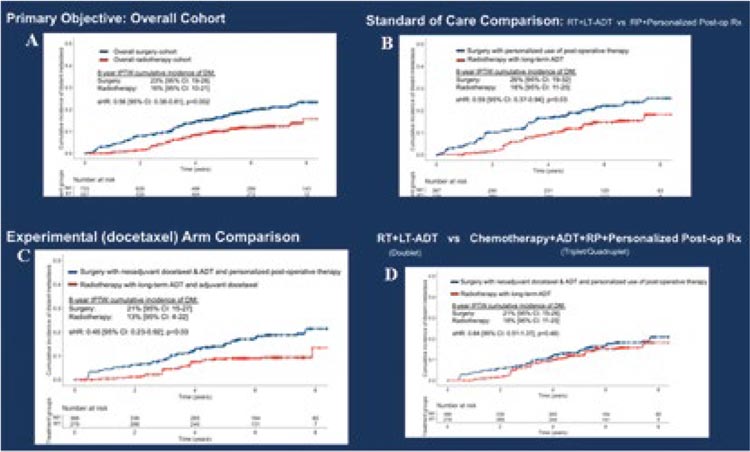
Финальные данные TALAPRO-2: талазопариб + энзалутамид vs энз
Ранее уже были представлены промежуточные результаты, подтверждающие эффективность комбинации талазопариба/энзалутамида в HRRдефицитной когорте. На конгрессе были показаны финальные результаты исследования. Напомним, в данную работу III фазы включены пациенты, которым планировалось проведение 1 линии мКРРПЖ, и были рандомизированы вне зависимости от HRR-статуса (он явился фактором стратификации) в 2 группы – талазопариб + энзалутамид и плацебо + эназалутамид. Первичная конечная точка – радиологическая ВБП (рВБП), главная вторичная точка – ОВ.
Во всей популяции пациентов комбинация ИАС и PARPi продемонстрировала улучшение ОВ (ОР=0,796; 95% ДИ 0,66-0,958; р=0,015) (рис.3).
Рисунок 3.
Общая выживаемость во всей популяции в
исследовании TALAPRO-2
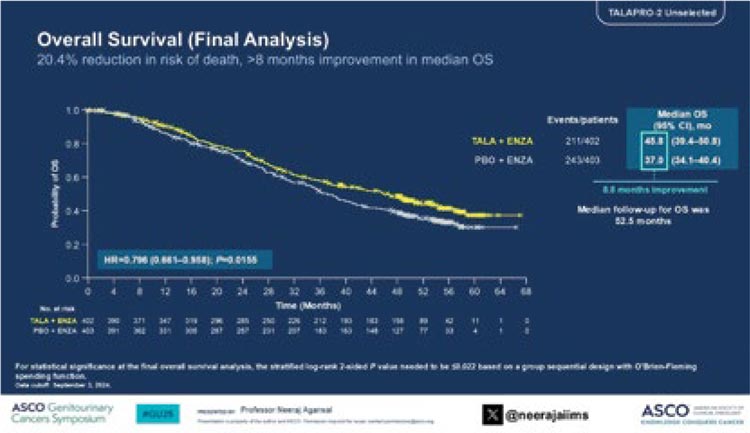
В подгрупповом анализе показано, что наибольший выигрыш от комбинации получили пациенты с костным поражением, HRR-дефицитным статусом и после терапии доцетакселом либо АА (рис.4).
Рисунок 4.
Подгрупповой анализ исследования TALAPRO-2
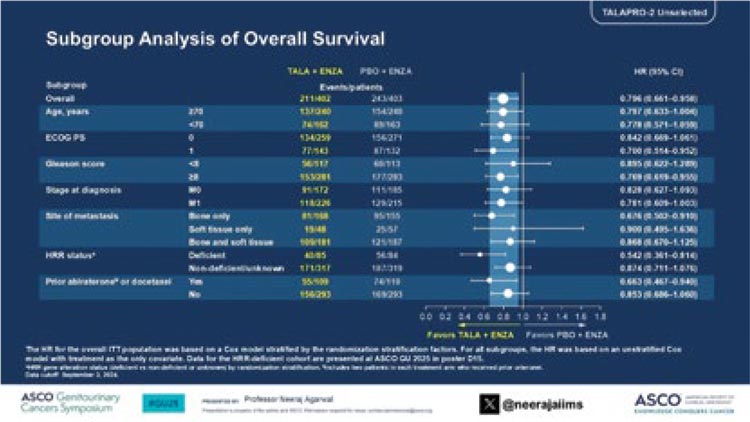
Хоть авторы и заявляют о выраженном клиническом превосходстве комбинации в когорте пациентов без мутаций BRCA и HRR, но давайте разберемся несколько подробнее (рис.5). В подгруппе больных без мутаций BRCA1/2 явно были больные с иными HRR-нарушениями, что позволило продемонстрировать пограничную значимость различий (ОР 0,749; 95% ДИ 0,582 – 0,963; р=0,02) в пользу комбинации. В группе без альтераций в системе HRR достоверных результатов не получено вовсе (р=0,108) несмотря на дельту рВБП в 9,2 мес. в пользу талазопариба/энзалутамида.
Какое-либо противоопухолевое лечение по поводу прогрессирования заболевания получили 37,4% и 52,6% пациентов в группах ИАС + PARPi и ИАС соответственно. Наиболее часто назначались таксаны (до трети случаев), АА (~15%), ПСМАтаргетная терапия (в 4%). В контрольной группе лишь 4% пациентов получили в дальнейшем PARPi (а альтерации HRR обнаружены у 20% больных в каждой группе), что безусловно также могло оказать влияние на итоговые результаты.
Рисунок 5.
ОВ в подгруппах пациентов без мутаций BRCA1/2 и
альтераций HRR
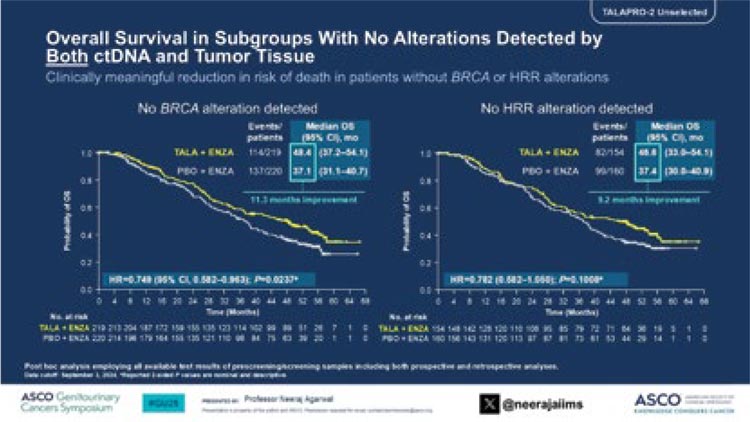
Еще ни в одном исследовании по изучению эффективности ИАС + PARPi не продемонстрировано статистически значимого и достоверного выигрыша в популяции больных без альтераций HRR (PROpel, TALAPRO-2, MAGNITUDE). Таким образом, на самых ранних этапах лечения пациента с диссеминированным РПЖ целесообразно проводить МГИ для планирования дальнейших линий терапии.
Мета-анализ STOPCAP, или какой пациент с гчРПЖ выиграет от терапии ИАС?
Эффективность антиандрогенов в лечении пациентов с гчРПЖ не вызывает ни у кого сомнений. Тем не менее до сих пор остаются вопросы: а все ли ИАС одинаково эффективны? Различается ли эффект между ИАС в зависимости от исходных характеристик пациентов? На эти непростые вопросы попыталась ответить работа STOPCAP, в которой проведен парный мета-анализ данных пациентов из завершенных исследований. Первичные конечные точки – ОВ (главная цель работы) и ВБП (для подгруппового анализа).
Характеристика пациентов и включенные в мета-анализ работы указаны на рис.6. Обращает на себя внимание превалирование пациентов с большим объемом поражения в исследовании LАTITUDE (AA). В некоторых протоколах планируемое использование доцетаксела явилось фактором стратификации пациентов (PEACE-1, ENZAMET).
Рисунок 6.
Характеристики пациентов в исследованиях,
включенных в анализ, а также достигнутые показатели
общей выживаемости
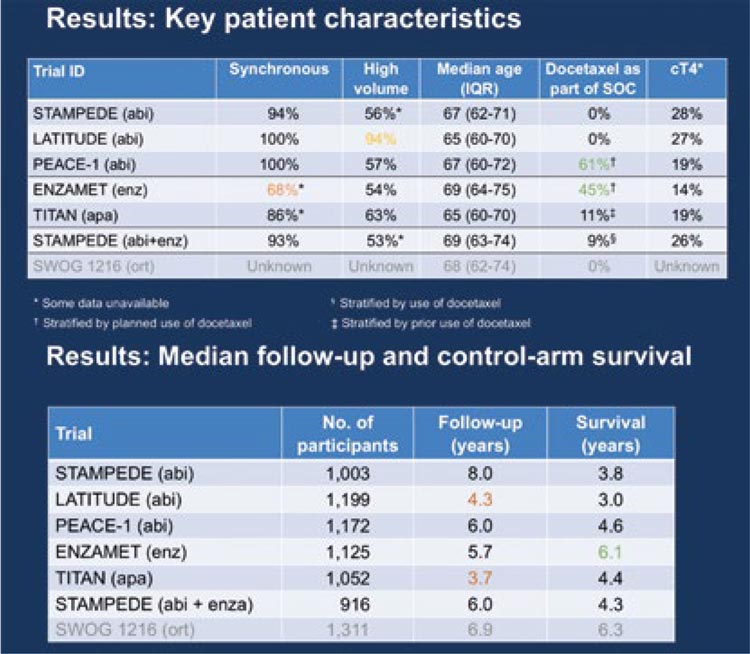
Все ИАС продемонстрировали свою эффективность как в ОВ (ОР 0,66; 95% ДИ 0,62 – 0,71), так и ВБП (ОР 0,51; 95% ДИ 0,48 – 0,55), при этом не отмечено преимуществ одного ИАС над другим в зависимости от объема метастатического поражения, суммы баллов по Глисону, поражения л/у и локализации метастазов. Авторы разделили пациентов на возрастные группы и показали, что эффективность АА в возрастной популяции >75 лет практически нивелируется (для ВБП: ОР 0,80; для ОВ: ОР 1,01) (рис.7).
Рисунок 7.
Эффективность абиратерона ацетата в
зависимости от возраста пациентов

А вот для «амидов» выигрыш продемонстрирован вне зависимости от возраста как в ВБП, так и ОВ (рис.8). Крайне интересная работа, позволяющая расставить некоторые акценты в лечении ИАС: препараты равноэффективны, нет преимуществ одного агента над другим в зависимости от исходных характеристик больных, АА лучше назначать молодым пациентам (интересно, а если больному в процессе терапии АА исполнилось 76 лет это влияет на его прогноз?), а энзалутамид стоит приберечь для более возрастных пациентов.
Рисунок 8.
Эффективность «амидов» в зависимости от
возраста пациентов
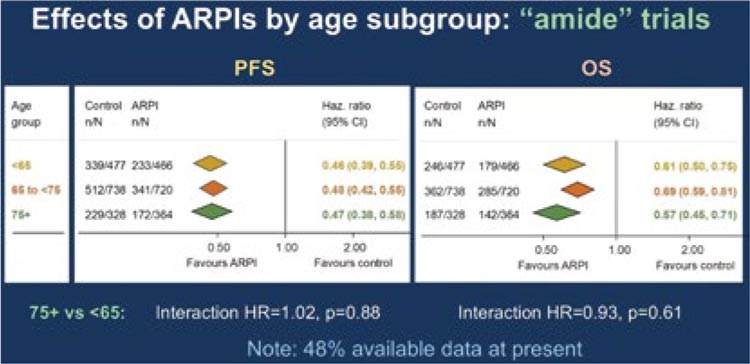
ENZA-p: 177-Lu-PSMA-617 + энзалутамид vs энзалутамид – данные по ОВ и качеству жизни
На ESMO 2023 были представлены первые результаты данной работы – комбинация ИАС + ПСМАтаргетная терапия продемонстрировала свое преимущество в ПСА-ВБП (первичная конечная точка) по сравнению с монотерапией ИАС (медиана 13 мес. vs 7.8 мес.; ОР 0.43; p <0.001) [5]. На ASCO GU 2025 представлены результаты по ОВ и качеству жизни. Авторами обновлена рВБП и составила 17 мес. vs 14 мес. (ОР 0,61; 95% ДИ 0,42 – 0,87) в группах лютеций/ энзалутамид и энзалутамид соответственно. ОВ оказалась выше в группе комбинации (мОВ 34 мес. vs 26 мес., ОР 0,549; р=0,0053) (рис.9). Отрадно, что 38% пациентов в группе монотерапии энзалутамидом получили в дальнейшем терапию Lu-PSMA.
Рисунок 9.
Общая выживаемость в исследовании ENZA-p
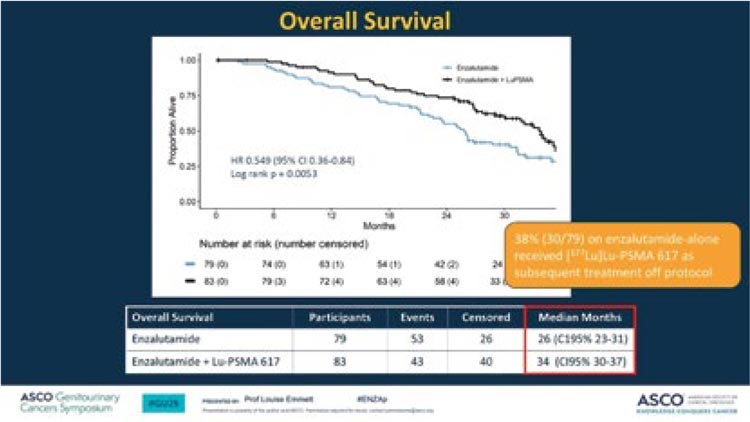
Время до ухудшения физической активности (медиана 10,6 мес. vs 3.4 мес.), общего соматического статуса (8,7 мес. vs 3,3 мес.) было лучше в группе комбинации (р=0,0001). Среднее количество баллов по усталости (разница 5,9; р=0,02) и боли (разница 7,3; р=0,01) до прогрессирования были в пользу лютеция/энзалутамида (рис.10).
Рисунок 10.
Оценка качества жизни пациентов в
исследовании ENZA-p
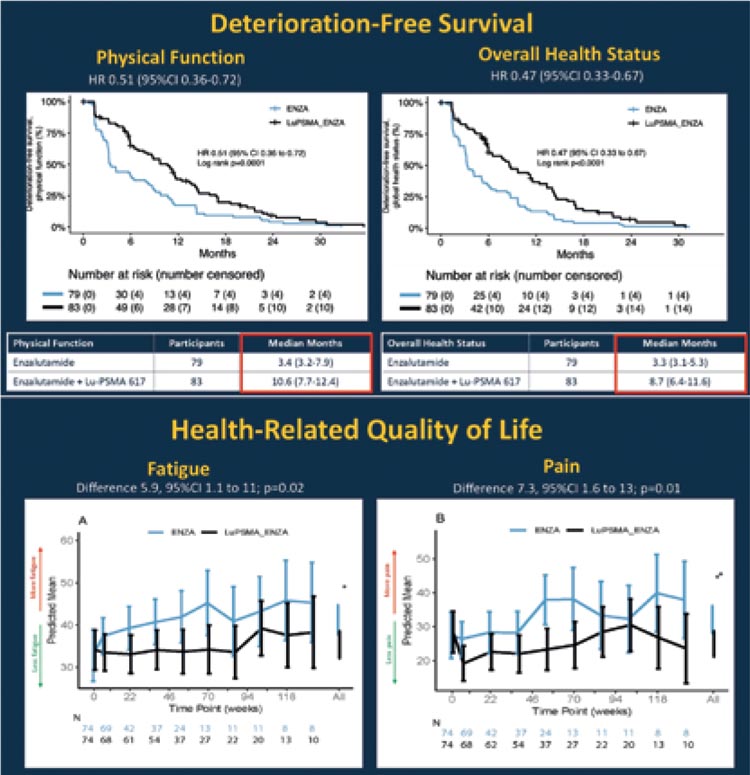
НЯ 3-5 степеней отмечены у 44% больных в группе энзалутамида и у 46% в группе комбинации. Гематологическая токсичность 3 степени зафиксирована только в группе лютеций/энзалутамид (до 4%).
Финальные данные ENZA-p оставляют странное послевкусие: с одной стороны скромные результаты в рВБП (незапланированная оценка), с другой – выраженное преимущество в ОВ и качестве жизни пациентов. Безусловно, комбинация ПСМАтаргетной терапии и антиандрогенов выглядит крайне привлекательно, но для четкого понимания эффективности подхода и его места в лечении мКРРПЖ необходимо проведение исследование III фазы с первичными конечными точками рВБП и ОВ, и возможностью кроссовера на терапию Lu-PSMA в случае прогрессирования пациентов из группы монотерапии ИАС.
PRECISION real-world data: раннее или отсроченное назначение LuPSMA в зависимости от предшествующей терапии антиандрогенами и доцетакселом (постер)
На постерной сессии американскими коллегами представлено ретроспективное исследование, оценивавшее оптимальную последовательность Lu-PSMA в мКРРПЖ. Из базы PRECISION взяты пациенты, получившие Lu-PSMA, и разделены на 2 группы в зависимости от времени ПСМА-таргетной терапии – «ранняя» (после 1 линии ИАС и таксанов (n=177)) vs «поздняя» (после 1 линии ИАС и таксанов + ≥1 линия ИАС и/ или таксанов) (n=256)).
Стоит отметить, что пациенты в «ранней» группе оказались моложе и с менее высоким стартовым уровнем ПСА (106,2 нг/мл vs 135,5 нг/мл), а также чаще получали лечение в академических центрах.
Большая эффективность Lu-PSMA отмечена в «ранней» группе как в частоте ПСА50 ответов (54,5% vs 41,8%), так и мОВ (не достигнуто vs 15,1 мес.).
К полученным результатам стоит относиться с осторожностью по нескольким причинам: гетерогенная популяция пациентов, возможность больных в группе «ранней» терапии после прогрессирования на Lu-PSMA получить последующее адекватное противоопухолевое лечение (в отличие от больных «поздней» группы ввиду своей предлеченности), ретроспективный характер работы. Тем не менее, растет число публикаций, указывающих на то, что оптимальное место ПСМА-таргетной терапии – третья линия лечения – после таксанов и ИАС.
НОВОСТИ ASCO GU 2025 / РАК МОЧЕВОГО ПУЗЫРЯ
NIAGARA trial: влияние pCR на отдаленные результаты лечения
На ESMO 2024 представлены первые данные исследования NIAGARA – периоперационный дурвалумаб + GC vs GC при МИРМП. Первичными конечными точками явилась бессобытийная выживаемость (БСВ) и pCR, оказавшиеся значимо выше в группе химиоиммунотерапии (ХИТ).
Давно известный факт, что достижение pCR напрямую коррелирует с улучшением отдаленных результатов лечения у пациентов с МИРМП [6,7]. Авторы работы NIAGARA также решили продемонстрировать свои результаты. Полный патоморфологический отмечен у 37,3% vs 27,5% в группах ХИТ и ХТ соответственно (р=0,0005). В подгруппе pCR мБСВ не достигнута ни в одной из групп, среди пациентов с nonpCR мБСВ составила 34,7 мес. vs 22,8 мес. для ХИТ и ХТ (ОР 0,77; 95% ДИ 0,631-0,948) соответственно (рис.12).
Рисунок 12.
Бессобытийная выживаемость в зависимости от
достигнутого патоморфоза в исследовании NIAGARA
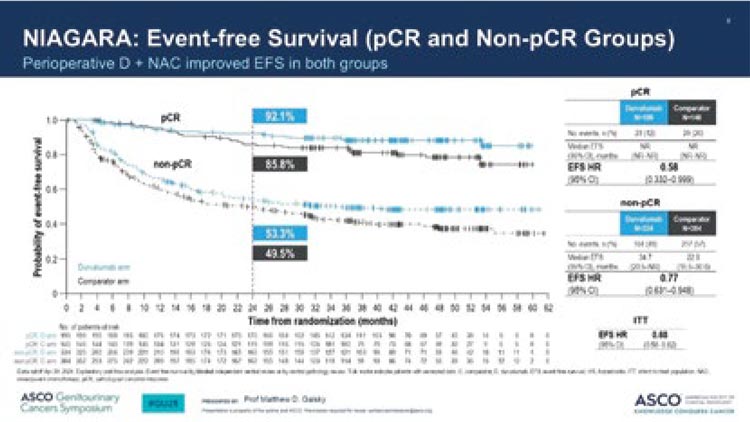
Медиана ОВ не достигнута ни в одной из подгрупп (рис.13). В связи с малой медианой наблюдения влияние периоперационного дурвалумаба на ОВ нам только предстоит узнать. Интересное наблюдение. В рандомизированном исследовании VESPER частота pCR в группах GC и ddMVAC составила 36% и 42% соответственно [8], а в NIAGARA в рукаве ХИТ – 37%. Так ли важна ИТ на предоперационном этапе? Может, эту опцию стоит резервировать только пациентам с non-pCR? Вопрос все еще открыт.
Рисунок 13.
Общая выживаемость в зависимости от
достигнутого патоморфоза в исследовании NIAGARA
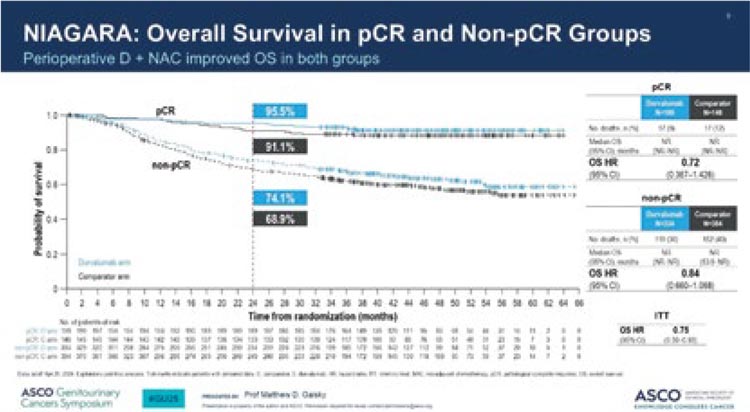
MEDI 4736: дурвалумаб в неоадъювантной терапии рака верхних мочевых путей высокого риска Пациенты с уротелиальным раком верхних мочевых путей (РВМП) часто исключаются из неоадъювантных исследований. Логично представить, что эти больные тоже могут выиграть от предоперационной лекарственной терапии как при раке мочевого пузыря, но проспективной базы недостаточно.
В исследовании POUT [9] адъювантная ХТ (как цис-, так и карбоплатин-содержащая) продемонстрировала свою эффективность в сравнении с наблюдением. Но перенос ХТ на предоперационный этап кажется актуальнее ввиду лучшей почечной функции, возможности эрадикации микрометастазов и оценки эффекта лечения.
В исследование MEDI 4736 включены пациенты с РВМП (highgrade опухоли, верифицированные с помощью биопсии или цитологии мочи, или поражение стенки лоханки/мочеточника с негативным цистоскопическим исследованием) ≤cT3N1M0 и рандомизированы в 2 группы (в зависимости от СКФ) – дурвалумаб + GC vs дурвалумаб + GemCarb, далее хирургическое лечение (рис.14). Первичная конечная точка – частота ypT0.
В исследование включено 49 пациентов, 30 в группу дурмалумаб + GC и 19 – дурвалумаб + GemCarb. Характеристики пациентов (за исключением почечной функции) были сбалансированы между группами.
Рисунок 14.
Дизайн исследования MEDI 4736
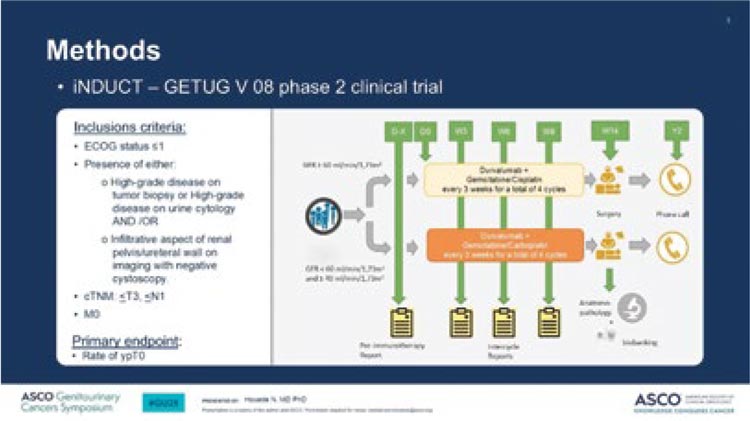
Диагноз был поставлен после биопсии 15% больных, цитологически – 44%, обоими методами в 41% случаев. Дискордантность между биопсией и цитологией составила 64% (рис. 15). Не отмечено значимого ухудшения почечной функции в процессе ХИТ ни в одном из режим.
Рисунок 15.
Методы верификации опухолей верхних мочевых
путей
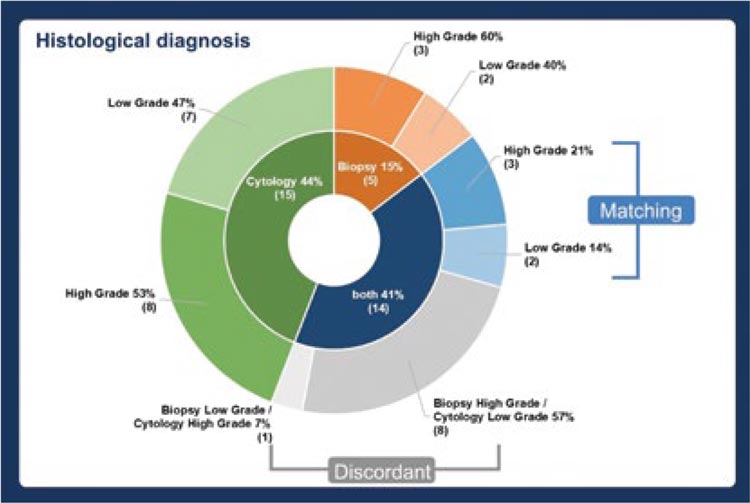
Полный ответ отмечен у 4 (13%) и 1 (5%) пациентов в группах циси карбоплатин-содержащих режимов. Снижение стадии <урT2 (урТ0, урТis/Ta, ypT1) отмечено у 60% и 46% в вышеуказанных группах (рис. 16).
Рисунок 16.
Патоморфологический ответ на проведенное
лечение
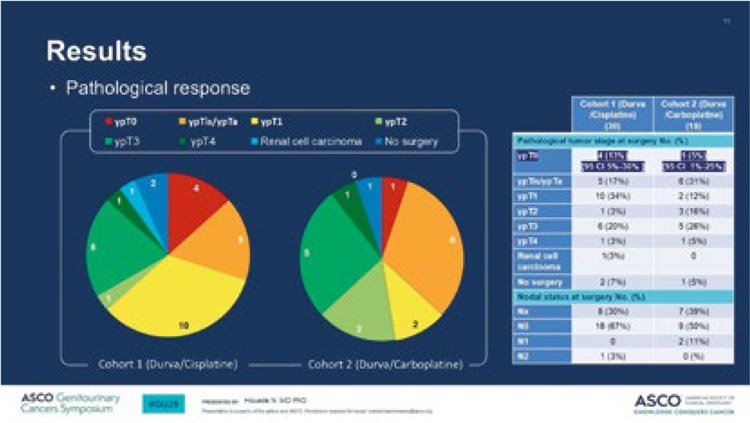
Представленные непосредственные результаты имеют ряд ограничений: лишь у 50% пациентов имелась морфологическая верификация диагноза, нет контрольной группы с только платиносодержащим режимом. Данные по отдаленным результатам пока что ожидаются. Очень интересное исследование, ждем зрелых данных.
RC48-C017 trial: диситамаб ведотин + торипалимаб в неоадъюванте МИРМП с экспрессией HER2
Гиперэкспрессия HER2/neu является фактором агрессивного течения РМП. В рандомизированном исследовании II фазы добавление трастузумаба к GC в неоадъюванте среди больных с HER2 IHC 2+/3+ не продемонстрировало своей эффективности [10]. Диситамаб ведотин успешно зарекомендовал себя при диссеминированном опухолевом процессе и HER2-позитивном статусе в комбинации с торипалимабом [11]. На ASCO GU 2025 представлены данные по изучению данной комбинации в неоадъюванте (рис. 17). Первичной конечной точкой выбран полный ответ (урТ0N0).
Рисунок 17.
Дизайн исследования RС48-С017
Рисунок 18.
Подгрупповой анализ pCR в зависимости от
исходной стадии и гистотипа
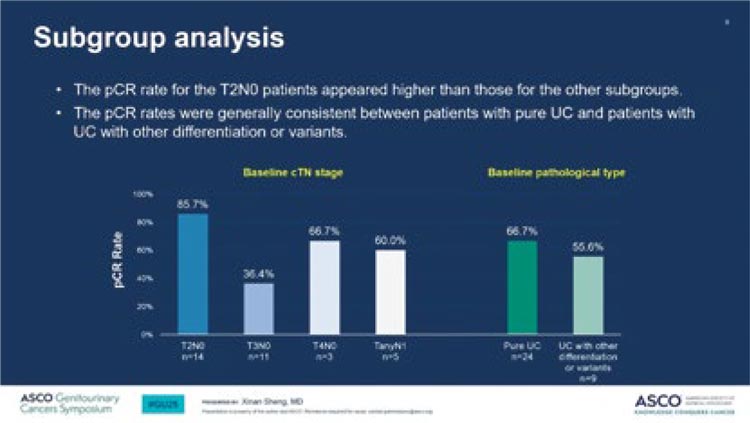
В анализ включено 47 больных. Большинство пациентов представлены II стадией заболевания (40%), треть – III стадией, гиперэкспрессия HER2 IHC 3+ отмечена у 32% пациентов, СКФ <60 мл/мин/1.73м2 у 25%.
Радикальная цистэктомия (РЦЭ) проведена 33 пациентам. Полный ответ отмечен у 63,6% больных, патоморфологический ответ (урТ ≤1N0) у 75,8%. Очевидно, что наибольшая частота pCR достигнута среди больных с сТ2N0 (85,7%), в трети случаев с сТ3N0. У пациентов как с типичным уротелиальным раком, так и дивергентным гистотипом pCR отмечен более чем в 50% случаев.
Однолетняя БСВ среди больных, кому проведена РЦЭ, составила 92,5%, медиана не достигнута, во всей когорте 1-летняя БСВ 90,5%, медиана также не достигнута (рис.19). Однолетняя ОВ равнялась 95,5%, медиана не достигнута.
Рисунок 19.
Бессобытийная выживаемость во всей популяции
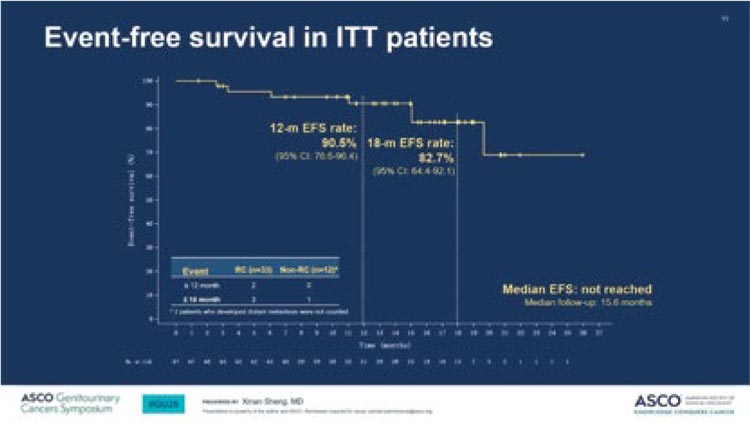
Рисунок 20.
Результат лечения в группе локального контроля
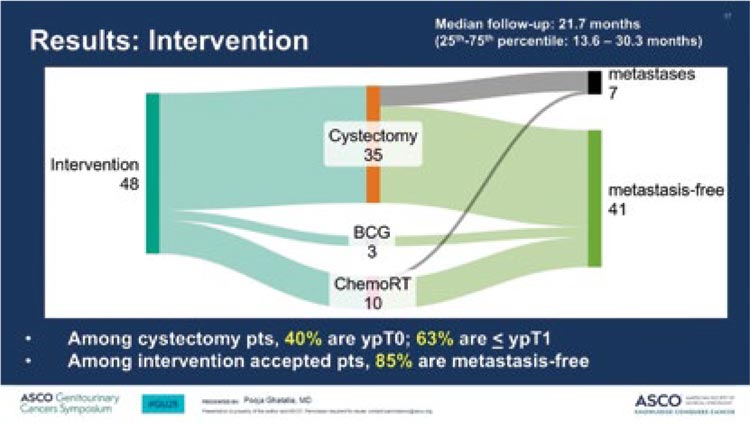
Идея таргетного воздействия на HER2/neu с помощью конъюгата моноклонального АТ и цитостатика в комбинации с ИТ при РМП демонстрирует свою противоопухолевую активность. У данной работы есть некоторые ограничения: короткий период наблюдения, малое количество пациентов, включение цисплатин-пригодных больных и нерандомизированный характер. Тем не менее, сам подход комбинации анти-HER2 конъюгата и ИТ должен изучаться в неоадъюванте, но в сравнении с стандартной платиносодержащей ХТ.
RETAIN-2: риск адаптированный подход после ХИТ у пациентов с МИРМП (промежуточный анализ)
Не так давно мы уже разбирали исследование RETAIN-1 – риск адаптированный подход после НАХТ в режиме ddMVAC в зависимости от мутационного статуса DDR. Исследование признано негативным в связи с недостижением первичной конечной точки. Но команду исследователей это не остановило, и они добавили к ddMVAC ниволумаб и повторили все то же самое. Пациентам после 3 курсов ХИТ выполнялась ТУР. В случае сТ0 и позитивным мутационным статусом DDR больные оставались под активным (!) наблюдением. При отсутствии DDRmut или наличии резидуальной опухоли пациентам предлагалось на выбор несколько опций – ВПХТ или ХЛТ, или РЦЭ. Первичная конечная точка – 2-летняя безметастатическая выживаемость (БМВ).
В работу включен 71 пациент. Большая часть (58%) представлена II стадией заболевания и негативным мутационным статусом (56,3%), вариантный гистотип определен у 32%.
Полный патоморфоз отмечен у 23 пациентов с DDRmut, и опцию активного наблюдения продолжили 19 пациентов, четверо предъявили желание получить локальное лечение несмотря на сТ0. Из 47 пациентов, которые попали в группу локального контроля, 3 от него отказались и перешли под активное наблюдение.
В группе локального контроля (n=48) 35 (73%) пациентам выполнена РЦЭ, полный патоморфоз отмечен у 40%, а у 63% ≤ урТ1. Отсутствие метастатического поражения при медиане наблюдения 21,7 мес. зафиксировано у 41 пациента.
Среди пациентов (n=19), распределенных в группу активного наблюдения, у 16 не отмечено метастатического поражения. При этом двоим пациентам выполнена отсроченная РЦЭ и у одного из них позже обнаружен диссеминированный процесс. Двум больным, которым был показан локальный контроль, но они выбрали наблюдение (n=3) выполнена отсроченная РЦЭ (рис. 21). Промежуточная БМВ в ITT равняется 77,4%, ОВ – 93%.
При сравнении с результатами RETAIN-1 в текущей работе выше частота ypT0 после РЦЭ (15% vs 40%), а также полный ответ (клинический + патоморфологический) в ITT популяции (27% vs 54%).
Рисунок 21.
Результат лечения в группе активного
наблюдения
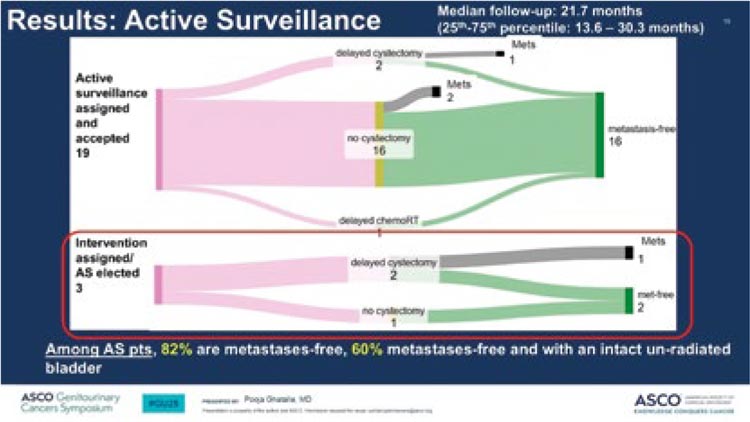
Лично для автора заметки вывод таков: пора изучить ddMVAC с ниволумабом в неоадъюванте (и желательно проводить стандартные 6 курсов)! А после его завершения все же пациентов прооперировать.
CheckMate 274: адъювантная терапия ниволумабом при МИРМП
СМ274 довольно обсуждаемое исследование в мире онкоурологии. Не утихают споры относительно того в какой популяции пациентов адъювантный ниволумаб после РЦЭ действительно дает выигрыш, а в какой мы просто перелечим пациентов.
Согласно подгрупповому анализу от 2023 года [12], наибольшую эффективность аИТ продемонстрировала среди пациентов с PD-L1-позитивными опухолями, ранее получивших неоадъювантную цисплатин-содержащую ХТ (НАХТ) и с пораженными л/у по данным гистологического исследования после РЦЭ. Эти же критерии выбора отражены в рекомендациях RUSSCO по лечению РМП [13].
В обновленном анализе все также демонстрируется преимущество аИТ в выживаемости без признаков болезни во всей популяции пациентов (ОР 0,63; 95% ДИ 0,51 – 0,78) и в подгруппе НАХТ (ОР 0,58; 95% ДИ 0,43 – 0,79), в группе без НАХТ эффективность данного подхода имеет пограничное значение (ОР 0,69; 95% ДИ 0,50 – 0,94) (рис.22).
Рисунок 22.
Выживаемость без признаков болезни
в зависимости от факта проведения НАХТ
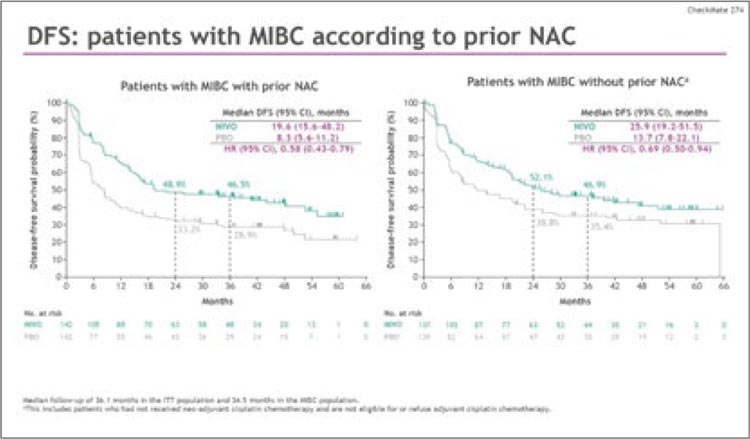
ОВ во всей популяции (ОР 0,70; 95% ДИ 0,55-0,90) и PD-L1- позитивной когорте (ОР 0,48; 95% ДИ 0,29-0,77) выше в рукаве аИТ. Удивительные результаты ОВ получены в зависимости от проведения НАХТ (рис.23): в подгруппе предшествующей лекарственной терапии преимущество ниволумаба недостоверно (верхняя граница 95% ДИ – 1,03) хотя и без нее значимость различий погранична (верхняя граница 95% ДИ – 0,95).
Рисунок 23.
Общая выживаемость в зависимости от
проведения НАХТ в исследовании CheckMate-274
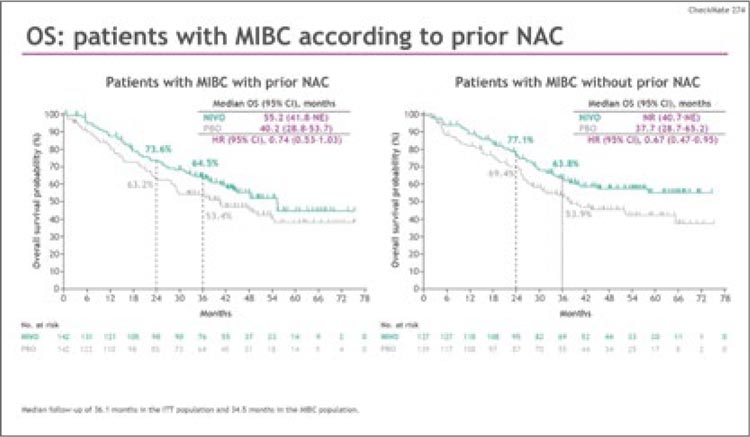
Что у нас остается в сухом остатке:
- назначим ли аИТ преимущественно пациентам с PD-L1- позитивным статусом – да,
- будем ли мы проводить всем цисплатин-пригодным пациентам НАХТ – преимущественно да,
- будем ли учитывать факт проведения НАХТ для определения показаний к аИТ в случае факторов риска после РЦЭ – продолжим этот спор на онкоурологических консилиумах.
Авторы умело подогревают наш интерес к данной работе. Продолжим следить за обновлениями.
НОВОСТИ ASCO GU 2025 / РАК ПОЧКИ
Финальные данные CheckMate 9ER: ниволумаб + кабозантиниб vs сунитиниб в 1й линии терапии диссеминированного почечно-клеточного рака (ПКР)
Эффективность иммунотаргентных комбинаций (ИТК) в 1й линии ПКР не вызывает ни у кого сомнений, в частности ниволумаба и кабозантиниба. Авторы в этом году представили данные после более 5,5 лет наблюдения (67,6 мес.).
ВБП в ITT популяции составила 16,4 мес. vs 8,3 мес. (ОР 0,58; 95% ДИ 0,49-0,70) в группах ИТК и монотерапии сунитинибом (рис. 24А), ОВ – 46,5 мес. vs 35,5 мес. (ОР 0,79; 95% ДИ 0,65-0,96) соответственно (рис. 24В). В подгруппе благоприятного прогноза по IMDC различия в ВБП имеют пограничную значимость (верхняя граница 95% ДИ – 0,97), а в ОВ их попросту нет (ОР 1,08) (рис. 24С). В группе промежуточного/плохого прогнозов явное преимущество ИТК демонстрирует в ВБП, а в ОВ после 5 лет наблюдения кривые начинают сходиться (рис. 24D).
С течением времени становится понятно, что пациенты благоприятного прогноза не нуждаются в эскалации 1й линии терапии, ведь они не получают преимуществ в ОВ (как и в других исследованиях с ИТК при ПКР). В представленных слайдах на конгрессе авторы несколько схитрили, объединив больных промежуточного и неблагоприятного прогнозов в одну группу. В ESMO Open в 2024 году [14] были представлены обновленные результаты при длительном наблюдении, оказалось, что только пациенты плохого прогноза имеют явный выигрыш от ИТК (ОР 0,46; 95% ДИ 0,30-0,72), при промежуточном анализе эффективность комбинации менее очевидна (ОР 0,75; 95% ДИ 0,56- 1,0) (рис. 25).
Стоит сделать вывод, что на текущий момент ИТК мы резервируем для пациентов плохого и промежуточного прогнозов. При благоприятном прогнозе рациональнее проведение монотерапии тирозинкиназными ингибиторами или ИТ с последующим кроссовером в случае прогрессирования. Некоторые эксперты отдельно выделяют категорию больных «с функционально значимыми метастазами» в рамках благоприятного прогноза, которой необходима ИТК для достижения большей ЧОО. Решение о назначении комбинации в таких случаях всегда должно приниматься коллегиально.
COSMIC-313: финальные результаты комбинации ниволумаба/ипилимумаба/кабозантиниба в 1й линии терапии диссеминированного ПКР
В исследовании COSMIC-313 – ниволумаб/ипилимумаб/кабозантиниб vs ниволумаб/ипилимумаб в 1й линии терапии ПКР групп промежуточного и плохого рисков – ранее продемонстрировано улучшение ВБП (первичная конечная точка) в группе триплета при медиане наблюдения 20 мес. (ОР 0,73; 95% ДИ 0,57-0,94; р=0,01) [15]. Однако большая токсичность рукава с кабозантинибом, пограничные значения в ВБП не сделали подобный подход стандартным.
В обновленном анализе кривые ВБП пересеклись воедино после 3 лет наблюдения (ОР 0,82; 95% ДИ 0,69-0,98) (рис.26), в ОВ также не получено различий (ОР 1,02; р=0,8366).
Ни в одной из прогностических групп не продемонстрировано эффективности от триплета (что удивительно в плохом прогнозе кабозантиниб даже вредил) (рис. 27).
В подгрупповом анализе ни одна из категорий пациентов не получила значимого выигрыша от триплета (рис.28).
Неожиданного поворота в данной работе не произошло, триплет не оказался лучше двойной иммунотерапевтической блокады. Мы никогда так не делали, а теперь точно не будем.
COTRIMS: первичная лимфаденэктомия у пациентов с диссеминированной семиномной герминогенной опухолью (СГО) (финальные результаты)
ГО – высокочувствительные к цисплатин-содержащей ХТ опухоли. Согласно обновленным данным консорциума IGCCCG 5-летняя ВБП и ОВ в группе СГО благоприятного прогноза при использовании современных режимов ХТ составили 89% и 95% соответственно [16]. Текущим стандартом лечения диссеминированных СГО (≥ II стадии) является проведение ХТ 1й линии (3 или 4 курса ВЕР в зависимости от группы прогноза IGCCCG) с последующим проведением ПЭТ/КТ и оценкой SUVmax в резидуальных очагах [17].
Принимая во внимание высокую курабельность ГО, молодой возраст пациентов, отдаленную токсичность платиносодержащей ХТ, немецкие авторы инициировали исследование COTRIMS – проспективное изучение нервосберегающей забрюшинной лимфаденэктомии (нсЗЛАЭ) у пациентов СГО IIA/IIB стадий и негативными опухолевыми маркерами (АФП, бета-ХГЧ, ЛДГ). Проведение аХТ не предусмотрено. Первичная конечная точка – 2-летняя безрецидивная выживаемость (БРВ).
Медиана возраста пациентов составила 34,2 года, большинство пациентов (65%) были с IIA стадией (к моменту нсЗЛАЭ). Антеградная эякуляция сохранена у 88,2% пациентов (очень важный демографический и не только показатель). Осложнения по ClavienDindo III-IV степени отмечены у 11,7% пациентов. Патоморфологически у 85% верифицирована семинома, у 9% – нет данных за опухолевое поражение, у 6% – эмбриональный рак. Авторы также продемонстрировали высокую как позитивную (95,8%), так и негативную (100%) предиктивную значимость miRNA-371 в оценке гистологического подтипа опухоли.
При медиане наблюдения 43,2 мес. 2-летняя БРВ составила 88,3% (стат. гипотезой закладывалось ≤20%), ОВ – 100%. Все пациенты в случае прогрессирования были излечены стандартной ХТ.
Лечение пациентов с ГО, в частности, хирургическое – удел высококвалифицированных центров, имеющих большой опыт в ведении данной редкой нозологии. В широкой клинической практике именно ХТ излечивает >90% пациентов с СГО и большинству уже не потребуется хирургическое лечение. Необходимо очень тщательно отбирать кандидатов для первичной нсЗЛАЭ и делать это только в профильных учреждениях.
Источники:
- J. A. Eastham et al., “Cancer and Leukemia Group B 90203 (Alliance): Radical Prostatectomy With or Without Neoadjuvant Chemohormonal Therapy in Localized, High-Risk Prostate Cancer,” Journal of Clinical Oncology, vol. 38, no. 26, pp. 3042–3050, Sep. 2020, doi: 10.1200/JCO.20.00315.
- S. A. Rosenthal et al., “Effect of Chemotherapy With Docetaxel With Androgen Suppression and Radiotherapy for Localized High-Risk Prostate Cancer: The Randomized Phase III NRG Oncology RTOG 0521 Trial,” Journal of Clinical Oncology, vol. 37, no. 14, pp. 1159–1168, 2019, doi: 10.1200/JCO.18.02158.
- G. Attard et al., “Abiraterone acetate and prednisolone with or without enzalutamide for high-risk nonmetastatic prostate cancer: a metaanalysis of primary results from two randomised controlled phase 3 trials of the STAMPEDE platform protocol,” The Lancet, vol. 399, no. 10323, pp. 447– 460, Jan. 2022, doi: 10.1016/S0140- 6736(21)02437-5.
- M. Gongora et al., “Characteristics of Patients in SPCG-15—A Randomized Trial Comparing Radical Prostatectomy with Primary Radiotherapy plus Androgen Deprivation Therapy in Men with Locally Advanced Prostate Cancer,” Eur Urol Open Sci, vol. 41, pp. 63–73, Jul. 2022, doi: 10.1016/J. EUROS.2022.04.013.
- L. Emmett et al., “LBA84 Enzalutamide and 177Lu-PSMA-617 in poor-risk, metastatic, castrationresistant prostate cancer (mCRPC): A randomised, phase II trial: ENZA-p (ANZUP 1901),” Annals of Oncology, vol. 34, p. S1325, Oct. 2023, doi: 10.1016/j.annonc.2023.10.086.
- A. Sherif et al., “Neoadjuvant C i s p l a t i n - M e t h o t r e x a t e Chemotherapy for Invasive Bladder Cancer - Nordic Cystectomy Trial 2,” Scand J Urol Nephrol, vol. 36, no. 6, pp. 419–425, 2002, doi: 10.1080/003655902762467567.
- H. B. Grossman et al., “Neoadjuvant Chemotherapy plus Cystectomy Compared with Cystectomy Alone for Locally Advanced Bladder Cancer,” New England Journal of Medicine, vol. 349, no. 9, pp. 859–866, Aug. 2003, doi: 10.1056/NEJMOA022148/ ASSET/F328C430-940F-408D-8FA7- 306BB89CF876/ASSETS/IMAGES/ LARGE/NEJMOA022148_F3.JPG.
- C. Pfister et al., “Randomized Phase III Trial of Dose-dense Methotrexate, Vinblastine, Doxorubicin, and Cisplatin, or Gemcitabine and Cisplatin as Perioperative Chemotherapy for Patients with Muscle-invasive Bladder Cancer. Analysis of the GETUG/AFU V05 VESPER Trial Secondary Endpoints: Chemotherapy Toxicity and Pathological Responses,” Eur Urol, vol. 79, no. 2, pp. 214–221, Feb. 2021, doi: 10.1016/J.EURURO.2020.08.024.
- A. J. Birtle et al., “Improved Disease-Free Survival With Adjuvant Chemotherapy After Nephroureterectomy for Upper Tract Urothelial Cancer: Final Results of the POUT Trial,” Journal of Clinical Oncology, vol. 42, no. 13, pp. 1466–1471, May 2024, doi: 10.1200/ JCO.23.01659.
- S. Oudard et al., “Multicentre randomised phase II trial of gemcitabine + platinum, with or without trastuzumab, in advanced or metastatic urothelial carcinoma overexpressing Her2,” Eur J Cancer, vol. 51, no. 1, pp. 45–54, Jan. 2015, doi: 10.1016/j.ejca.2014.10.009.
- L. Zhou et al., “Study RC48-C014: Preliminary results of RC48-ADC combined with toripalimab in patients with locally advanced or metastatic urothelial carcinoma.,” Journal of Clinical Oncology, vol. 40, no. 6_ suppl, pp. 515–515, Feb. 2022, doi: 10.1200/JCO.2022.40.6_SUPPL.515.
- M. D. Galsky et al., “Extended follow-up results from the CheckMate 274 trial.,” Journal of Clinical Oncology, vol. 41, no. 6_suppl, pp. LBA443–LBA443, Feb. 2023, doi: 10.1200/JCO.2023.41.6_SUPPL. LBA443.
- “Рак мочевого пузыря”, doi: 10.18027/2224-5057-2024-14-3s2-1.2- 09.
- T. Powles et al., “Nivolumab plus cabozantinib versus sunitinib for firstline treatment of advanced renal cell carcinoma: extended follow-up from the phase III randomised CheckMate 9ER trial,” ESMO Open, vol. 9, no. 5, p. 102994, May 2024, doi: 10.1016/j. esmoop.2024.102994.
- T. K. Choueiri et al., “Cabozantinib plus Nivolumab and Ipilimumab in Renal-Cell Carcinoma,” New England Journal of Medicine, vol. 388, no. 19, pp. 1767–1778, May 2023, doi: 10.1056/ NEJMOA2212851/SUPPL_FILE/ NEJMOA2212851_DATA-SHARING. PDF.
- J. Beyer et al., “Survival and New Prognosticators in Metastatic Seminoma: Results From the IGCCCG-Update Consortium,” Journal of Clinical Oncology, vol. 39, no. 14, pp. 1553–1562, May 2021, doi: 10.1200/JCO.20.03292.
- “Герминогенные опухоли у мужчин”, doi: 10.18027/2224-5057-2024- 14-3s2-1.2-11.
Материал подготовил Э.Р. Исраелян.
ЭТО ИНТЕРЕСНО / КОФЕ УТРОМ – НИЖЕ РИСКИ

Кофе является одним из наиболее любимых и часто употребляемых напитков в мире. Большинство проспективных исследований показали, что умеренное потребление кофе связано с более низким риском развития диабета 2 типа, сердечнососудистых заболеваний (ССЗ) и смерти. Однако наличие связи между чрезмерным потреблением кофе (более 3–5 чашек в день) и риском смертности по-прежнему остается спорным фактом. Учитывая важность кофе для нашей повседневной жизни, ряд исследований изучали, существует ли связь между потреблением кофе, особенно чрезмерным, и показателями здоровья, и могут ли клинические или поведенческие факторы, включая курение, потребление кофе без кофеина и подсластителей, добавляемых в кофе, генетически обусловленную скорость метаболизма кофеина, а также способ заваривания кофе повлиять на эту возможную связь. Однако нет последовательных доказательств, подтверждающих, что эти факторы изменяют связь между потреблением кофе и показателями здоровья.
В частности, все больше данных указывают на важность циркадного ритма в регулировании поведения человека, связанного с приемом пищи, и метаболизма, и некоторые предыдущие исследования показали, что время приема пищи может иметь значение для показателей здоровья. Интересно, что кофе уже давно используется для улучшения бодрствования и снятия сонливости из-за стимулирующего воздействия кофеина на центральную нервную систему. Однако употребление кофе позже в течение дня может нарушить суточные циркадные ритмы. Неясно, существуют ли определенные закономерности в отношении времени употребления кофе среди населения, и, если да - связаны ли эти закономерности с риском смертности. Этим вопросом задались американские исследователи и опубликовали свои данные в январском номере журнала Европейского общества кардиологии «European Heart Journal».
В это исследование были включены 40 725 взрослых из Национального опросника по исследованию здоровья и питания за период 1999–2018 гг. и 1463 взрослых из исследования по валидации образа жизни женщин и мужчин; в отношении всех включенных пациентов имелась полная информация о питании. Кластерный анализ использовался для выявления закономерностей по времени употребления кофе.
В этом наблюдательном исследовании были выявлены две различные модели времени употребления кофе: утренний тип (36% участников, n =14 643) и коуглосуточный тип (14% участников, потреблявших кофе в течение всего дня, n = 6489); еще 48% (n = 19 593) вообще не употребляли кофе.
В течение медианного (межквартильного) периода наблюдения в 9,8 (9,1) лет было зарегистрировано в общей сложности 4295 случаев смерти от всех причин, 1268 случаев смерти от сердечно-сосудистых заболеваний и 934 случая смерти от рака. После корректировки с учетом количества потребляемого кофе с кофеином и без кофеина, часов сна и других факторов, именно утренний тип потребления, а не круглосуточный, был значимо ассоциирован с более низкими рисками смертности от всех причин (коэффициент риска: 0.84; 95% ДИ 0.74–0.95) и сердечно-сосудистых заболеваний (коэффициент риска: 0.69; 95% ДИ 0.55–0.87) по сравнению с неупотреблением кофе (рис.1). Время употребления кофе значительно повлияло на связь между количеством потребляемого кофе и смертностью от всех причин (P = 0.031).
Рисунок 1.
Время потребления кофе
(утренний и круглосуточный паттерны)
и смертность от всех причин и ССЗ
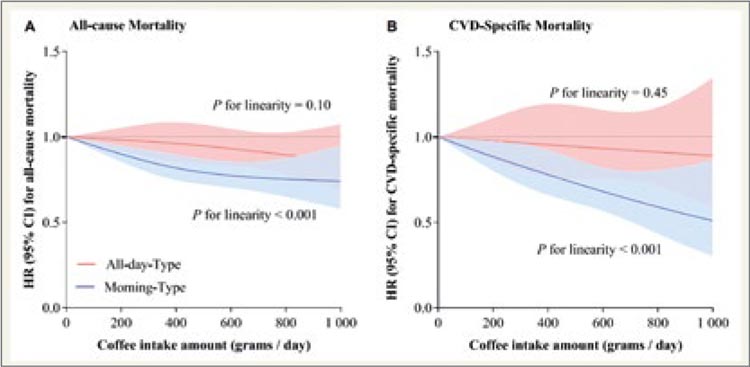
Более частое потребление кофе было достоверно связано с более низким риском смертности от всех причин у участников с утренним типом приема кофе, но не у тех, кто придерживался круглосуточного режима (рис.2).
Рисунок 2.
Ассоциация между паттерном потребления кофе
и количеством чашек кофе и смертностью от всех причин
в сравнении людьми, не употребляющими кофе.
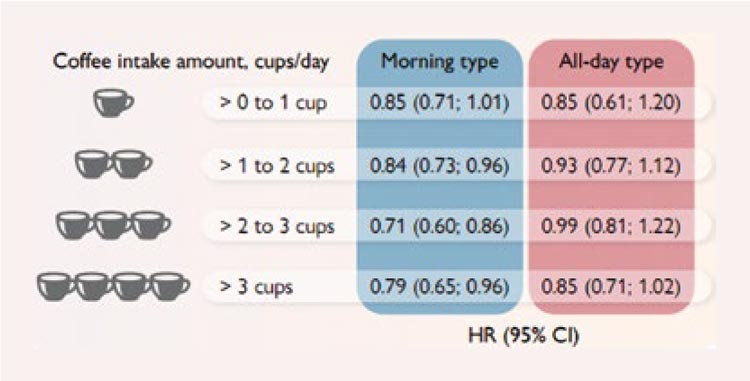
Несмотря на немалое число ограничений этой работы, над ее результатами стоит задуматься и принять к сведению: авторы все же обнаружили, что время употребления кофе связано с риском смертности от всех причин и риском смертности от сердечно-сосудистых заболеваний независимо от количества потребляемого кофе. Употребление кофе по утрам может быть в большей степени связано с более низкой смертностью, чем употребление кофе позднее в течение дня.
Источник:
Xuan Wang et al. Coffee drinking timing and mortality in US adults. European Heart Journal (2025) 00, 1–11 https:// doi.org/10.1093/eurheartj/ehae871