Дорогие коллеги, дорогие друзья!
Этот номер газеты увидел свет на стыке зимы и весны, объединив в себе и зимние события (юбилей RUSSCO с множеством поздравлений наших коллег из разных регионов, Всемирный день борьбы против рака, очередной симпозиум ASCO GU 2026 в...

Эдвард Мунк. Spring in Åsgårdstrand. 1905. 80 x 60 см, холст, масло. Местонахождение картины неизвестно.
Spring in Åsgårdstrand. 1905. 80 x 60 см, холст, масло. Местонахождение картины неизвестно.

15 ЛЕТ RUSSCO / 15 лет назад, 31 января 2011 года, в России было зарегистрировано Межрегиональное общество онкологов-химиотерапевтов
Тогда, в отсутствие профессиональных сообществ, это была действительно передовая идея, энтузиасты в различных регионах имели большое желание объединиться и работать совместно....

15 ЛЕТ RUSSCO / Юбилей RUSSCO. Это было недавно…
…Это было давно. Не было интернета, мобильных телефонов, сегодня молодым коллегам кажется, что тогда мамонты еще бродили по улицам. А вот онкология была, в онкологических диспансерах лечили пациентов, на кафедрах онкологии проводили...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения Красноярского края
Замечательная дата – 15 лет RUSSCO, хотя, если честно, в это даже не верится: кажется, что наше профессиональное сообщество было всегда и имеет долгую и богатую историю. Это, видимо, связано с тем, что за эти годы общество реализовало немало...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения Владимирской области
15 лет назад, когда мы были совсем юными онкологами (засыпали в операционных, стоя на крючках, считали, что названия химиопрепаратов имеют явно инопланетное происхождение, а чтобы стать радиотерапевтом необходимо пройти...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от Тюменского регионального отделения Российского общества клинической онкологии
От имени онкологов Тюменской области и от себя лично сердечно поздравляю Российское общество клинической онкологии (RUSSCO) с юбилеем – 15-летием со дня основания! ...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения в Республике Саха (Якутия)
В этом году мы отмечаем знаменательное событие – 15-летие Российского общества клинической онкологии (RUSSCO), которое стало ведущей профессиональной ассоциацией, объединившей специалистов нашей страны для достижения общей цели...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от Приморского регионального отделения Российского общества клинической онкологии
С самого создания RUSSCO в 2011 г. Приморские онкологи неразрывно связывают с Обществом свою профессиональную деятельность. Особенно обращает внимание личное, теплое участие руководителей RUSSCO к его членам из отдаленных..

15 ЛЕТ RUSSCO / Путь борьбы за жизнь длиною в 15 лет: RUSSCO глазами региона
Размах истории в 15 лет – это миг, но не для медицинской науки. Для онкологии – это целая эпоха грандиозных открытий и свершений. Оглядываясь назад, я вспоминаю, как всё начиналось. Тогда, на заре создания Российского общества клинической...

15 ЛЕТ RUSSCO / К юбилею RUSSCO от Свердловского регионального отделения Российского общества клинической онкологии
От имени Свердловского регионального отделения сердечно поздравляю всех нас с 15-летием Российского общества клинической онкологии! ..

15 ЛЕТ RUSSCO / К юбилею RUSSCO от онкологов регионального отделения Хабаровского края
В этом году Российское общество клинической онкологии отмечает свой 15-летний юбилей. За этот срок организация прошла путь от смелой идеи до главного профессионального сообщества страны. ...

15 ЛЕТ RUSSCO / Так получилось...
Так получилось, что большую часть моей практической деятельности я проживаю с RUSSCO, иду рука об руку с любимым сообществом, радуюсь его успехам, постоянному увеличению числа членов, количества мероприятий, переживаю – как и все мы...
НОВОСТИ ОНКОЛОГИИ / 4 ФЕВРАЛЯ ЕЖЕГОДНО ОТМЕЧАЕТСЯ ВСЕМИРНЫЙ ДЕНЬ БОРЬБЫ ПРОТИВ РАКА
Цель этого Дня – повышение осведомленности населения планеты об онкологических заболеваниях, их профилактике, раннем выявлении и лечении, акцентирование внимания на том, что рак – не приговор, и современная медицина способна...

НОВОСТИ ОНКОЛОГИИ / КАК ЭФФЕКТИВНОСТЬ ИММУНОТЕРАПИИ ЗАВИСИТ ОТ ЦИРКАДНЫХ РИТМОВ
Циркадные ритмы представляют собой эндогенные биологические колебания с периодом около 24 часов, которые влияют на большинство физиологических процессов, происходящих в организме человека, обеспечивая его благополучие и...
НОВОСТИ ОНКОЛОГИИ / ДВУХСТОРОНЯЯ САЛЬПИНГЭКТОМИЯ КАК ЭФФЕКТИВНЫЙ МЕТОД ПРОФИЛАКТИКИ РАКА ЯИЧНИКОВ
Рак яичников остается одним из самых смертельных гинекологических злокачественных новообразований, при этом, несмотря на достижения в лечении, за последние десятилетия наблюдается незначительное улучшение пятилетней...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ЛОКАЛЬНАЯ ТЕРАПИЯ ОЛИГОМЕТАСТАЗОВ: ЕЩЕ ОДИН ПЛЮС К ДОКАЗАТЕЛЬНОЙ БАЗЕ
Олигометастатическое заболевание представляет собой проксимальный отрезок спектра метастазирования, и для лечения пациентов с олигометастазами различных опухолей все чаще используются локальные методы, вкупе получившие название...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / SABR И ИММУНОТЕРАПИЯ ДЛЯ УВЕЛИЧЕНИЯ ЧАСТОТЫ PCR: ИССЛЕДОВАНИЕ 2 ФАЗЫ
Несмотря на уже имеющиеся отличные отдаленные результаты проспективных исследований по применению стереотаксической лучевой терапии при раннем раке легкого (в частности, обновленное исследование STARS [1]), скепсис в отношении...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / О СТАРОМ ДОБРОМ ТАМОКСИФЕНЕ – В ДОЛГОСРОЧНОМ АНАЛИЗЕ STO
У пациенток с рецептор-положительным раком молочной железы (РМЖ) стандартом адъювантного лечения является гормональная терапия тамоксифеном; при этом сохраняется весьма значительный поздний риск отдаленного рецидива, однако...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / РМЖ И РЧА: АДЕКВАТНАЯ АЛЬТЕРНАТИВА?
Пока сложно представить себе, что лечение раннего рака молочной железы (РМЖ) может обойтись без хирургического вмешательства, когда для этого есть все условия. Тем не менее, варианты малоинвазивных или неинвазивных процедур...

ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ПОТЕРЯ ВКУСА ПРИ ОБЛУЧЕНИИ ОПУХОЛЕЙ ГОЛОВЫ И ШЕИ: ЧТО ПРОИСХОДИТ И ПОЧЕМУ
Нарушение вкуса – один из самых частых и недооцененных побочных эффектов лучевой терапии при опухолях головы и шеи. Большое проспективное исследование китайских авторов, инициированное в августе 2023 года и опубликованное в...
НОВОСТИ ОНКОЛОГИИ / ФИНАЛЬНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ SONIA У БОЛЬНЫХ МЕТАСТАТИЧЕСКИМ ЛЮМИНАЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Исследование SONIA не раз было предметом оживленных дискуссий и споров вследствие актуальности изучаемой проблемы: использовать ли назначение CDK4/6 ингибиторов в первой или во второй линии гормонотерапии у больных...

НОВОСТИ ASCO GU 2026 / РАК ПОЧКИ
Итак, что же нового нам было представлено по раку почки на симпозиуме в этом году? ....
ТЕЗИСЫ КОНФЕРЕНЦИИ RUSSCO
ОСОБЕННОСТИ ГИСТОЛОГИЧЕСКОЙ КАРТИНЫ ..., Индукционная стратегия при раке шейки ..., Комбинированная мелкоклеточная нейроэндокринная ..., и т.д

ДОВЕРИТЕЛЬНЫЙ ИНТЕРВАЛ / НА ЧТО МЫ ДЕЙСТВИТЕЛЬНО ДОЛЖНЫ СМОТРЕТЬ В АНАЛИЗЕ ВЫЖИВАЕМОСТИ?
Кривые Каплана-Майера и связанные с ними показатели – медиана, отношения рисков, p-value – во многом определяют наш выбор тактики лечения в онкологии. Однако эти показатели нередко интерпретируются изолированно: из контекста...
Анонс
-

17 АПРЕЛЯ ПЯТИГОРСК
ЭКЗАМЕН ПО КЛИНИЧЕСКОЙ ОНКОЛОГИИ
Российского общества клинической онкологии (RUSSCO)
-

26 - 27 МАРТА МОСКВА
РАК МОЛОЧНОЙ ЖЕЛЕЖЫ
XIII КОНФЕРЕНЦИЯ RUSSCO
Дорогие коллеги, дорогие друзья!
Этот номер газеты увидел свет на стыке зимы и весны, объединив в себе и зимние события (юбилей RUSSCO с множеством поздравлений наших коллег из разных регионов, Всемирный день борьбы против рака, очередной симпозиум ASCO GU 2026 в последние дни февраля), и тезисы с первой весенней конференции по онкогинекологии, и – безусловно – поздравления наших милых коллег женского пола-племени с мартовским праздником.
Этот день – 8 Марта — символ Весны, красоты и силы, которые вы приносите в нашу жизнь. Вы — вдохновение и опора для своих близких, вы обладаете невероятной стойкостью и мудростью. Ваша забота и любовь делают мир лучше, а ваша решимость и смелость служат примером для всех нас. В этот особенный день мы желаем вам здоровья, мира, счастья и благополучия. Пусть каждый день будет наполнен радостью, а все мечты сбываются. Мы ценим ваш вклад в борьбу с онкологическими заболеваниями и уверены, что вместе, в едином сообществе, мы сможем преодолеть любые трудности. Весной нас, дорогие коллеги, ждет немало мероприятий, в том числе Экзамен RUSSCO и несколько больших конференций; вся информация о них содержится на сайте RosOncoWeb. А программный комитет грядущего юбилейного XXX Российского онкологического конгресса уже начинает свою работу по его подготовке. Ждем от вас предложений по тематике сессий, докладов, готовьте тезисы – одним словом, станьте активным участником юбилейного Конгресса!
Мы понемногу начинаем облачаться в более легкие пальто, прячем подальше зимнюю обувь, любуемся мартовскими тюльпанами… а в голове крутится детский, коротенький и совершенно мартовский стишок:
О чём поют воробушки
В последний день зимы?
-Мы выжили!
-Мы дожили!
-Мы живы, живы мы! (В.Берестов)
Будем жить! Доброй Весны вам, дорогие друзья!
Ваша команда RUSSCO
Эдвард Мунк. Spring in Åsgårdstrand. 1905. 80 x 60 см, холст, масло. Местонахождение картины неизвестно.
Spring in Åsgårdstrand. 1905. 80 x 60 см, холст, масло. Местонахождение картины неизвестно.

15 ЛЕТ RUSSCO / 15 лет назад, 31 января 2011 года, в России было зарегистрировано Межрегиональное общество онкологов-химиотерапевтов
Автор: Тимофеев Илья Валерьевич,
один из основателей и первый исполнительный директор RUSSCO
Тогда, в отсутствие профессиональных сообществ, это была действительно передовая идея, энтузиасты в различных регионах имели большое желание объединиться и работать совместно.
Со временем инициатива выросла во всем известное Российское общество клинической онкологии – RUSSCO. В этом же году появились и первые региональные отделения общества. Начиная с нескольких десятков участников, RUSSCO сейчас насчитывает более 8,5 тыс. членов. Количество инициатив RUSSCO составляет уже солидный список, а Российский онкологический конгресс стал самым главным и крупнейшим научным событием года.
— 15 лет – это возраст подростка: уже есть характер, принципы, опыт и собственный голос, но впереди ещё много роста, открытий и больших свершений. Горжусь пройденным путём, людьми, которые были и остаются рядом, и тем, во что эта идея превратилась. История продолжается!
15 ЛЕТ RUSSCO / Юбилей RUSSCO. Это было недавно…
Автор: Королева Ирина Альбертовна
д.м.н., профессор, Медицинский университет «Реавиз»,
врач онколог-химиотерапевт «Многопрофильной клиники Реавиз»,
Самара
…Это было давно. Не было интернета, мобильных телефонов, сегодня молодым коллегам кажется, что тогда мамонты еще бродили по улицам. А вот онкология была, в онкологических диспансерах лечили пациентов, на кафедрах онкологии проводили исследования, научные институты разрабатывали новые методы лечения. В эти удивительные времена я стала химиотерапевтом. Оказалось, что самая главная проблема химиотерапевта - не отсутствие лекарств, а отсутствие информации. Моя общая тетрадь с конспектами лекций Ирины Владимировны Поддубной по химиотерапии лежала в ординаторской, эта тетрадь и руководство Натальи Иннокентьевны Переводчиковой вели нас крутыми тропами химиотерапии. Первые конференции ESMO в России, организованные Сергеем Алексеевичем Тюляндиным изменили наш мир, ради этих конференций, которые переросли в Российский онкологический конгресс, мы тянули жребий, оставляли в отделении одного врача и всем коллективом ехали слушать, учиться, впитывать драгоценные знания. Мы все понимали, что онкология, в частности лекарственная терапия, развивается с невероятной скоростью, новые противоопухолевые препараты появлялись один за другим. Прекрасно помню, как наш неизменный лидер Сергей Алексеевич Тюляндин сказал в 2010 году, что нам нужен не только Российский онкологический конгресс, но профессиональное сообщество, распространяющее профессиональные знания каждый день, круглый год, во всех регионах, а в 2011 году уже было создано RUSSCO. Практические рекомендации RUSSCO сразу стали настольной книгой химиотерапевтов. RUSCCO для меня - это круг единомышленников, людей, про которых я знаю что-то очень важное, как и они про меня. Мы RUSSCO – а значит мы готовы получать знания, делиться знаниями, внедрять новое, лечить эффективнее!
15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения Красноярского края
Автор: Зуков Руслан Александрович
д.м.н., профессор, ФГБОУ ВО «КГМУ им. проф. В.Ф. Войно-Ясенецкого»
Минздрава России, главный врач КГБУЗ «Красноярский краевой клинический
онкологический диспансер им. А.А. Крыжановского, председатель регионального
отделения RUSSCO Красноярского края, Красноярск
Замечательная дата – 15 лет RUSSCO, хотя, если честно, в это даже не верится: кажется, что наше профессиональное сообщество было всегда и имеет долгую и богатую историю. Это, видимо, связано с тем, что за эти годы общество реализовало немало успешных научных, практических и образовательных проектов, востребованных не только онкологами-химиотерапевтами, но и всей мультидисциплинарной командой специалистов, участвующих в лечении онкологических пациентов.
Хочу поздравить всю команду RUSSCO и нас всех, пожелать здоровья, энергии, сил, успехов и так же высоко держать эту планку, как это было на протяжении многих лет. Дальнейшего развития и процветания!
15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения Владимирской области
Автор: Шейко Андрей Владимирович
Онколог, радиотерапевт, заведующий радиотерапевтическим отделением
№2 ГБУЗ ВО «Областной клинический онкологический диспансер»,
председатель регионального отделения RUSSCO Владимирской области,
Владимир
15 лет назад, когда мы были совсем юными онкологами (засыпали в операционных, стоя на крючках, считали, что названия химиопрепаратов имеют явно инопланетное происхождение, а чтобы стать радиотерапевтом необходимо пройти профпереподготовку на радио-ди-джея), в стране появилось маленькое, но очень гордое и многообещающее сообщество RUSSCO. Онкологи стали объединяться, общаться, шутить и, похлопывая друг друга по плечу, затевать жаркие споры на ежегодных онкоконгрессах. Оказавшись на одном из таких конгрессов году так в 2015-м, мы тоже поняли, что нам пора в команду, пора в науку, пора в споры, пора в междисциплинарные баталии, пора в жестокую критику и приятное одобрение, пора в неостанавливаемый мыслительный процесс в режиме 24/7! Прошло еще несколько лет, и мы жадно нырнули в круговерть мастер-классов, конференций и встреч под эгидой RUSSCO, зачастую пожимая руки знаменитым зарубежным коллегам – настоящим стейкхолдерам мировой онкологии, чьи имена мы видели только на обложках книг и гайдлайнов. А потом... А потом привозили все эти эмоции, эти знания, эти вопросы и эти стимулы домой. И страстно, почти фанатически, старались делать региональную онкологическую службу чуточку лучше. Из года в год.
Мы до сих пор в RUSSCO, теперь мы и есть часть RUSSCO, часть той мощно летящей вперед онкологической машины, которая когда-то привила нам любовь к науке, любовь к своему делу, любовь к Пациенту. Пациенту, который всегда останется центростремительной силой нашей профессии.
С Днем Рождения, RUSSCO! Владимирское региональное отделение шлет тебе воздушный поцелуй и миллиард благодарностей!
15 ЛЕТ RUSSCO / К юбилею RUSSCO от Тюменского регионального отделения Российского общества клинической онкологии
Автор: Гайсин Тимур Ахатович
Начальник организационнометодической службы ГАУЗ ТО
«Медицинский город», председатель регионального
отделения RUSSCO Тюменской области, Тюмень
Уважаемые коллеги, дорогие друзья!
От имени онкологов Тюменской области и от себя лично сердечно поздравляю Российское общество клинической онкологии (RUSSCO) с юбилеем – 15-летием со дня основания!
Пятнадцать лет – это возраст зрелости, мудрости и огромного профессионального авторитета. За эти годы RUSSCO прошло путь от инициативной группы энтузиастов до крупнейшего профессионального объединения, задающего стандарты онкологической помощи в стране. Главная сила вашей организации – в умении объединять. Вы доказали, что победа над раком не может быть делом одной специальности. Благодаря вашей работе онколог садится за один стол с патоморфологом, радиотерапевт обсуждает тактику с хирургом, а фармацевт и исследователь становятся полноправными участниками лечебного процесса. Этот мультидисциплинарный подход, который вы возвели в абсолют, сегодня спасает жизни в каждом регионе России.
В свой юбилей примите самые искренние пожелания дальнейшего процветания. Пусть каждое ваше начинание находит поддержку, каждый новый проект приносит плоды, а число спасенных жизней растет с каждым годом. Мы гордимся возможностью быть частью большого сообщества RUSSCO и верить, что следующие 15 лет принесут еще больше открытий и побед!
С уважением и глубокой признательностью,
Гайсин Тимур Ахатович
15 ЛЕТ RUSSCO / К юбилею RUSSCO от регионального отделения в Республике Саха (Якутия)
Автор: Иванова Феодосия Гаврильевна
к.м.н., Главный онколог Министерства здравоохранения Республики Саха (Якутия),
заслуженный врач РС (Я) и РФ, руководитель отдела лекарственного лечения ГБУ РС (Якутия)
«Якутский республиканский онкологический диспансер», председатель регионального отделения RUSSCO в
Республике Саха (Якутия)
Глубокоуважаемые коллеги!
В этом году мы отмечаем знаменательное событие – 15-летие Российского общества клинической онкологии (RUSSCO), которое стало ведущей профессиональной ассоциацией, объединившей специалистов нашей страны для достижения общей цели – повышения качества онкологической помощи пациентам.
За эти годы Общество стало надёжной опорой для практикующих врачей, став площадкой для разработки клинических рекомендаций, организации образовательных программ и конференций, а также поддержки научных исследований. Особенно важна профессиональная поддержка, которую Общество оказывает врачам в регионах: доступ к актуальным клиническим данным, экспертным мнениям и образовательным ресурсам в области диагностики и лечения. Это значительно облегчает нашу ежедневную работу и способствует повышению качества лечения больных со злокачественным новообразованием, что, безусловно, улучшает результат лечения пациентов.
Мы искренне благодарим всех членов RUSSCO за вашу готовность поддерживать коллег из регионов. Эта взаимопомощь вдохновляет нас на новые свершения и позволяет решать любые поставленные задачи.
Уважаемые коллеги, сердечно поздравляем Российское общество клинической онкологии с юбилеем! Желаем вам крепкого здоровья и созидательной энергии, стойкости и надежности – как якутский алмаз, мудрости и дальновидности – как течение великой реки Лена. Пусть ваши научные открытия продолжают удивлять, а единство профессионального сообщества станет залогом нашего успеха.
Пусть ваше дело и дальше служит людям, а совместная работа помогает нам уверенно идти к главной цели – победе над онкологическими заболеваниями.
С уважением, Иванова Феодосия Гаврильевна
15 ЛЕТ RUSSCO / К юбилею RUSSCO от Приморского регионального отделения Российского общества клинической онкологии
Автор: Гурина Людмила Ивановна
д.м.н., профессор, главный внештатный онколог Министерства здравоохранения
Приморского края, председатель регионального отделения RUSSCO Приморского края,
г. Владивосток
С самого создания RUSSCO в 2011 г. Приморские онкологи неразрывно связывают с Обществом свою профессиональную деятельность. Особенно обращает внимание личное, теплое участие руководителей RUSSCO к его членам из отдаленных территорий нашей страны: это проведение научных образовательных мероприятий, регистрация и участие в национальном онкологическом конгрессе, бесплатное обеспечение Клиническими рекомендациями Российского общества клинической онкологии (настольная книга каждого онколога), рассылка замечательной газеты RUSSCO и доступность информации сайта RosOncoWeb.ru, которые знакомят нас не только с новостями в онкологии, но и с прекрасной живописью. Главный редактор газеты и сайта Илья Валерьевич Тимофеев оказал неоценимую поддержку при организации Приморского отделения межрегиональной общественной организации «Общество онкологов химиотерапевтов». Вера Витальевна Карасева, проф., исполнительный директор RUSSCO, оказала неоценимое содействие в совершенствовании деятельности и научного прогресса Приморского отделения Общероссийской общественной организации «Российское общество клинической онкологии», одним из учредителей которого, а в последствии председателем явилась д.м.н. Гурина Людмила Ивановна (протокол №1 от 12.10.2012 г. учредительного собрания Приморского отделения межрегиональной общественной организации «Общество онкологов химиотерапевтов»).
Мы, Приморские онкологи, дорожим знакомством и гордимся дружбой с доктором медицинских наук, профессором Сергеем Алексеевичем Тюляндиным, долгие годы возглавлявшим RUSSCO. Сергей Алексеевич неоднократно выезжал к нам в Приморский край с научно-образовательной миссией. Его визиты собирали полные аудитории, вызывали дискуссии и подвигали нас к совершенствованию знаний, опыта работы и научной деятельности в области онкологии. Это Сергей Алексеевич одним из первых знакомил нас с инновационными технологиями в лечении рака: молекулярно-генетические исследования, нефармакологические интервенции, иммунотерапия и таргетная, борьба с олигометастазами, лечение тройного негативного рака молочной железы и другое. Между RUSSCO и ГБУЗ «Приморский краевой онкологический диспансер» заключен 13.10.2020 г. договор №30-9-131020 о проведении молекулярно-генетических и иммуногистохимических исследований, безвозмездного обеспечения маршрутизации и логистики биообразцов пациентов из ГБУЗ «Приморский краевой онкологический диспансер» в референсную лабораторию в рамках Национальной Программы RUSSCO «Совершенствование молекулярно-генетической диагностики в Российской Федерации с целью повышения эффективности противоопухолевого лечения». Сергей Алексеевич научил нас применять на практике результаты отечественных и мировых клинических исследований по онкологии. При участии Сергея Алексеевича и поддержке RUSSCO в столице Приморского края городе Владивосток в 2014 г. стартовали ежегодные конференции «Лучшее по материалам международных конференций и симпозиумов – Восток». Лучшие российские эксперты и лекторы были включены в наши ежегодные комплексные планы научно-практических мероприятий края, семинары из циклов «Возможности современной иммунотерапии злокачественных опухолей». Организованы мероприятия с участием зарубежных экспертов, например, 12-14 сентября 2019 г. – Международный курс по паллиативной онкологии – International Palliative Care Workshop (IPCW). При поддержке RUSSCO организовано проведение конференций «PD-L1 – предиктор эффективного ответа на checkpoint ингибиторы при НМКРЛ», «Циторедукция при метастазах колоректального рака. Когда это удлиняет ОВ и потенциально излечивает?», мастеркласс «Опухоли головы и шеи», семинар «Опухоли желудочно-кишечного тракта», вебинары «1-я линия терапии почечноклеточного рака», «Хирургический опыт лечения BRCA-ассоциированного РМЖ» и многое другое. По приглашению RUSSCO врач-онколог ГБУЗ «Приморский краевой онкологический диспансер» Анастасия Валерьевна Фатеева презентовала свой доклад «Опыт лечения онкологических пациентов в условиях пандемии COVID-19» на VII Российской конференции «Поддерживающая терапия в онкологии». В связи с 5-летним юбилеем за результативную и плодотворную совместную работу Приморское отделение Российского общества клинической онкологии награждено Дипломом RUSSCO.
Сегодня Приморское отделение Общероссийской общественной организации «Российское общество клинической онкологии» насчитывает 46 членов. А Сергей Алексеевич Тюляндин является для нас примером беззаветного служения людям на медицинском поприще.
С глубоким уважением, Л.И. Гурина
15 ЛЕТ RUSSCO / Путь борьбы за жизнь длиною в 15 лет: RUSSCO глазами региона
Автор: Огнерубов Николай Алексеевич
д.м.н., д.ю.н., профессор, Председатель Тамбовского регионального отделения RUSSCO,
заслуженный работник высшей школы РФ, заслуженный врач РФ, Тамбов
Размах истории в 15 лет – это миг, но не для медицинской науки. Для онкологии – это целая эпоха грандиозных открытий и свершений. Оглядываясь назад, я вспоминаю, как всё начиналось. Тогда, на заре создания Российского общества клинической онкологии (RUSSCO), мы все остро чувствовали необходимость создания сообщества. Причем нам нужна была не просто организация, а профессиональная семья, объединяющая врачей, ученых и исследователей с одной целью – сделать лечение рака эффективным и доступным.
Для меня большая честь стоять у истоков этого движения в нашем регионе. Организовав и возглавив Тамбовское региональное отделение RUSSCO, я видел, как стал меняться подход к лечению, как точная и скрупулёзная наука начала трансформироваться в спасенные жизни наших пациентов.
Все эти годы мы, безусловно, росли вместе. Я помню наши первые конференции, жаркие дискуссии в кулуарах, обмен бесценным клиническим опытом. Сегодня RUSSCO – это флагман и знак качества отечественной онкологии. Это уникальная площадка, где стираются границы между федеральными центрами и регионами, где мнение профессора и практика слышат и уважают.
Ваши образовательные программы, конференции и, конечно же, клинические рекомендации стали для нас, практикующих врачей, фундаментом, надежным компасом в океане новых препаратов и методов лечения. Как доктор юридических наук, я особенно ценю тот вклад, который Общество вносит в правовую защиту врача и пациентов, а также стандартизацию по оказанию специализированной помощи. Как врач и ученый – я благодарен за возможность непрерывного профессионального развития.
Хочу поздравить всех нас с этим замечательным юбилеем – 15-летием Российского общества клинической онкологии! Это были годы неустанного труда, поиска истины и профессионального единства.
Желаю Обществу процветания, новых научных прорывов и расширения горизонтов. Пусть наша совместная работа и дальше дарит надежду на выздоровление нашим пациентам. Мы вместе, и это наша главная сила!
С уважением, Николай Алексеевич Огнерубов
15 ЛЕТ RUSSCO / К юбилею RUSSCO от Свердловского регионального отделения Российского общества клинической онкологии
Автор: Петкау Владислав Владимирович
к.м.н.,Заместитель главного врача по лекарственному лечению ГАУЗ СО «СООД»,
доцент кафедры онкологии ФГБОУ ВО «Уральский государственный медицинский университет»,
Екатеринбург
Уважаемые коллеги!
От имени Свердловского регионального отделения сердечно поздравляю всех нас с 15-летием Российского общества клинической онкологии!
Не каждому профессиональному сообществу удаётся стать своим, родным, близким. RUSSCO это удалось.
RUSSCO – это не отдельно «где-то в Москве существующая организация». RUSSCO – это мы, врачи-онкологи. За эти годы врачи, в том числе и из регионов, стали реальными участниками профессионального диалога на всех уровнях. Мы выступаем на мероприятиях Общества, работаем в экспертных советах, участвуем в создании клинических рекомендаций, делимся опытом на страницах газеты и сайта, обсуждаем сложные случаи и радуемся общим достижениям. Мы не наблюдатели, мы – соавторы.
Мы растем вместе с RUSSCO. Школы RUSSCO, экзамен, конкурсы для молодых специалистов – это не просто образовательные проекты, это пространство возможностей. Восхищает энергия и энтузиазм молодых онкологов, их смелость задавать вопросы и предлагать новые решения. В их глазах – будущее нашей специальности.
И, конечно, RUSSCO – это общение. Это встречи с экспертами мирового уровня, коллегами и друзьями со всех уголков страны. Мы ждём конференций и ежегодного Конгресса не только ради научных прорывов, но и ради живого разговора, профессионального спора, человеческой поддержки. Всегда есть с кем обсудить сложный клинический случай, научную гипотезу или просто обменяться дружеским приветствием.
И вот эта теплота – то, за что мы любим RUSSCO! Пусть впереди будет ещё больше совместных проектов, открытий и побед, в нашей непростой, но удивительно важной и интересной профессии.
С юбилеем, дорогие коллеги!
15 ЛЕТ RUSSCO / К юбилею RUSSCO от онкологов регионального отделения Хабаровского края
Автор: Новикова Ольга Юрьевна
к.м.н., главный внештатный специалист онколог МЗ ХК, председатель регионального
отделения Российского общества клинической онкологии RUSSCO,
Хабаровск
Глубокоуважаемые коллеги!
В этом году Российское общество клинической онкологии отмечает свой 15-летний юбилей. За этот срок организация прошла путь от смелой идеи до главного профессионального сообщества страны.
RUSSCO для нас – это про дружбу, которая не знает часовых поясов. Это про ту искру в глазах, когда мы встречаемся на конференциях, и про общую тихую радость, когда пациент идет на поправку. Мы здесь, на берегах Амура, первыми встречаем солнце, и сегодня это солнце – в честь нашего юбилея!
Мы ценим Общество за то, что оно научило нас мыслить глубже, искать истину в доказательствах и никогда не останавливаться в развитии. Благодаря вам сложнейшие научные достижения мирового уровня стали инструментом в руках практического врача.
Говоря об успехах RUSSCO, невозможно не отметить неоценимый вклад Сергея Алексеевича Тюляндина. Его профессиональный авторитет, научная честность и стратегическое видение стали тем фундаментом, на котором выросло Общество. Именно благодаря его инициативе были заложены основы современных клинических рекомендаций и создана уникальная образовательная среда, объединившая тысячи врачей.
Спасибо всем, кто стоял у истоков, и тем, кто каждый день вкладывает душу в развитие Общества. Пусть следующие 15 лет будут наполнены новыми надеждами и, конечно, Жизнью, которую мы вместе защищаем.
С юбилеем, коллеги!
15 ЛЕТ RUSSCO / Так получилось...
Автор: Деньгина Наталья Владимировна
к.м.н., Заведующая радиологическим отделением ГУЗ «Областной клинический онкологический диспансер»,
главный врач Центра лучевой терапии «R-Spei», председатель Ульяновского регионального отделения RUSSCO,
Ульяновск
Так получилось, что большую часть моей практической деятельности я проживаю с RUSSCO, иду рука об руку с любимым сообществом, радуюсь его успехам, постоянному увеличению числа членов, количества мероприятий, переживаю – как и все мы - из-за невзгод, что выпали на долю RUSSCO, и надеюсь, что «…все еще будет, и южный ветер еще подует!»
Мое RUSSCO – это, в первую очередь, его лидеры, основатели – Сергей Алексеевич Тюляндин, Илья Валерьевич Тимофеев, Дмитрий Александрович Носов и многие другие, в том числе и те, кто навеки остался в истории сообщества.
Моё RUSSCO – это та команда, возглавляемая проф. Верой Витальевной Карасевой, которая с видимой легкостью движет этот локомотив вперед, реализуя огромное количество задумок, поддерживая любое начинание и стимулируя каждого из нас двигаться дальше, к безграничному совершенству.
Мое RUSSCO – это региональные отделения, многим из которых тоже 15 лет, ибо инициатива лидеров была подхвачена сразу; и каждому из них хочется передать горячий привет и самые лучшие пожелания на много лет вперед! Мое RUSSCO – это сайт и газета, информационные каналы, текущие «вести с полей» онкологии и обзоры экспертов в отношении свежайших данных с конгрессов мирового уровня.
Мое RUSSCO – это общество, которое никого и никогда не оставляло равнодушным, наша онкологическая семья, наша гордость, наша любовь.
Процветания и долголетия тебе, наше RUSSCO!
НОВОСТИ ОНКОЛОГИИ / 4 ФЕВРАЛЯ ЕЖЕГОДНО ОТМЕЧАЕТСЯ ВСЕМИРНЫЙ ДЕНЬ БОРЬБЫ ПРОТИВ РАКА
Цель этого Дня – повышение осведомленности населения планеты об онкологических заболеваниях, их профилактике, раннем выявлении и лечении, акцентирование внимания на том, что рак – не приговор, и современная медицина способна эффективно бороться с ним, особенно при ранней диагностике. По данным UICC (Международный союз по борьбе с онкологическими заболеваниями), инициатора проведения Дня, около 43% злокачественных заболеваний можно предотвратить, ведя здоровый образ жизни и проходя регулярные медицинские осмотры.
Незадолго до этого события, в середине января, мир увидел новые данные по статистике рака – публикация в журнале A Cancer Journal For Clinicians «Cancer Statistics 2026» [1]. Ежегодно Американское онкологическое общество оценивает количество новых случаев рака и смертей в Соединенных Штатах и концентрирует самые последние данные о распространенности рака и исходах заболевания среди населения, используя данные, собранные центральными онкологическими регистрами и Национальным центром статистики здравоохранения. Эти регулярно обновляемые данные впоследствии используют авторы многих статей, таблицы и рисунки мы видим в различных презентациях, и, экстраполируя эти данные на мировой уровень, мы видим, что происходит с заболеваемостью и смертностью в мире за определенные отрезки времени, какие злокачественные новообразования лидируют, в лечении которых из них удалось достичь наибольшего прогресса, а где еще предстоит немало работать.
Основные выводы последнего анализа:
- Уровень смертности от рака продолжает снижаться, предотвратив 4,8 миллиона смертей с 1991 года, в основном благодаря сокращению курения, более ранней диагностике и улучшению качества лечения.
- Отмечено увеличение относительной пятилетней выживаемости, которая достигла важной отметки в 70% для всех диагнозов ЗНО, поставленных в период 2015-2021 годов в целом, 69% для заболеваний на ранней стадии и 35% для метастатических заболеваний, по сравнению с 63%, 54% и 17% соответственно в середине 1990-х годов.
Рисунок 1.
Тенденции заболеваемости ЗНО (1975-2022 гг.) и смертности (1975-2023 гг.) по полу, США. Показатели скорректированы по возрасту в соответствии со стандартной популяцией США 2000 года, а показатели заболеваемости скорректированы с учетом задержек в отчетности о случаях заболевания.
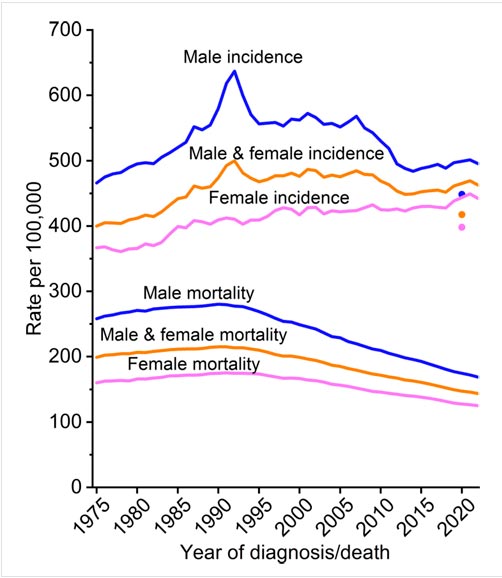
- Наибольший прогресс наблюдался в отношении опухолей, характеризующихся высокой смертностью и высокой запущенностью: отмечено увеличение показателей ОВ с 32% до 62% для миеломы, с 7% до 22% для рака печени, с 16% до 35% для метастатической меланомы, с 8% до 18% для метастатического рака прямой кишки, с 20% до 37% для местнораспространенного рака легкого и с 2% до 10% для метастатического рака легкого. Тем не менее, рак легкого остается главным «киллером» и станет причиной основного числа смертей в 2026 году, второй по распространенности – колоректальный рак и третий – рак поджелудочной железы.
Рисунок 2.
Основные виды ЗНО, по которым прогнозируется наибольше число новых случаев заболевания и смертей от рака по полу, США, 2026 год. Оценки округлены до ближайших 10, и случаи не включают базальноклеточный и плоскоклеточный рак кожи, а также карциному in situ, за исключением рака мочевого пузыря.

Интересные данные предоставила практически та же команда авторов недавнего статистического анализа в журнале JAMA [2]. Данные о ежегодном количестве смертей от рака и стандартизированных по возрасту показателях на 100 000 мужчин и женщин моложе 50 лет за период с 1990 по 2023 год были получены из базы данных SEER*Stat (версия 9.0.41.4; Национальный институт рака) на основе информации, предоставленной Национальным центром статистики здравоохранения (NCHS). Тенденции в показателях смертности от всех видов рака в совокупности и от 5 основных причин смерти от рака за период с 1990 по 2023 год были количественно оценены, и в итоге авторы пришли к выводу, что и для более молодого контингента онкологических больных показатели смертности снизились заметно за более чем 30-летний период времени – в среднем на 44%, особенно это касается рака молочной железы, рака легкого, лейкозов и рака поджелудочной железы. Однако у пациентов до 50 лет главным «киллером» признан колоректальный рак – показатели смертности от этой опухоли продолжают увеличиваться.
Рисунок 3.
Тенденции заболеваемости ЗНО (1975-2022 гг.) и смертности (1975-2023 гг.) по полу, США. Показатели скорректированы по возрасту в соответствии со стандартной популяцией США 2000 года, а показатели заболеваемости скорректированы с учетом задержек в отчетности о случаях заболевания.

В целом, десятилетия научных инвестиций привели к увеличению жизни людей даже с самыми смертельными формами рака. Однако дальнейший прогресс находится под угрозой из-за предполагаемых во многих странах федеральных сокращений финансирования исследований рака и медицинского страхования, которое обеспечивает доступ к жизненно важному лечению рака.
Источники:
- Siegel RL, Kratzer TB, Wagle NS, Sung H, Jemal A. Cancer statistics, 2026. CA Cancer J Clin. 2026; e70043. doi:10.3322/caac.7004.
- Siegel RL, Wagle NS, Jemal A. Leading Cancer Deaths in People Younger Than 50 Years. JAMA. 2026 Jan 22; e2525467. doi: 10.1001/jama.2025.25467. Epub ahead of print. PMID: 41569583; PMCID: PMC12828652.
НОВОСТИ ОНКОЛОГИИ / КАК ЭФФЕКТИВНОСТЬ ИММУНОТЕРАПИИ ЗАВИСИТ ОТ ЦИРКАДНЫХ РИТМОВ
Автор: Тюляндин Сергей Алексеевич
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
профессор, доктор медицинских наук, Москва
Циркадные ритмы представляют собой эндогенные биологические колебания с периодом около 24 часов, которые влияют на большинство физиологических процессов, происходящих в организме человека, обеспечивая его благополучие и здоровье. У млекопитающих циркадные ритмы регулируют сон-бодрствование, отдых-активность, аппетит, мышечную и когнитивную работоспособность, температуру тела, гормональную секрецию, клеточный метаболизм, пролиферацию и гибель клеток, а также продукцию, функционирование и транспорт иммунных клеток. Циркадные ритмы демонстрируют точные 24-часовые периоды, синхронизируясь с 24-часовыми циклами окружающей среды и особенно – с регулярным чередованием света и темноты. Другие факторы окружающей среды, влияющие на циркадные ритмы, включают в себя физическую активность и отдых в определенное время, социально-профессиональные и семейные взаимодействия, а также режим питания. Циркадная координация и адаптация к сигналам окружающей среды в основном осуществляются через супрахиазматические ядра, расположенные в зрительном перекресте головного мозга. Зависимые от этих ядер ритмические сигналы координируют генетические молекулярные часы, находящиеся внутри каждой клетки млекопитающих, в результате чего образуется иерархическая сеть часов, составляющая циркадную систему синхронизации. Каждая клетка млекопитающих наделена молекулярными часами, включающими 15 генов (NPAS2, PER2, DBP, ARNTL, PER3, NR1D1, CRY1, NR1D2, CLOCK, CRY2, BHLHE40, PER1, BHLHE41, RORA и TIMELESS), которые, взаимодействуя друг с другом посредством транскрипции в определенное время, регулируют важнейшие внутриклеточные физиологические процессы, такие как пролиферация, репарация ДНК, апоптоз и аутофагия.
Эффект любого лекарственного средства определяется циркадной регуляцией механизмов абсорбции, распределения, метаболизма, элиминации и токсичности на молекулярном, тканевом и органном уровнях. Циркадные ритмы влияют на процессы биоактивации, детоксикации и элиминации на транскрипционном, белковом и ферментативном уровнях в печени, главном органе, метаболизирующем лекарственные средства, а также в кишечнике, почках, легких и т.д. Ранее были проведены многочисленные исследования, включая рандомизированные, с целью определения влияния циркадных ритмов на эффективность химиотерапии и определения времени максимальной активности и минимальной токсичности противоопухолевых препаратов. Большинство исследований предоставили доказательства снижения токсичности, вызванной хрономодулированной химиотерапией без потери противоопухолевой эффективности. В ходе проведенных в последнее время клинических исследований и наблюдений была отмечена достоверная тенденция увеличения времени до прогрессирования (PFS) и общей выживаемости (OS) у больных, получавших иммунотерапию и иммунохимиотерапию в утренние и дневные часы в сравнении с пациентами, которые получали лечение вечером. В настоящее время семнадцать из восемнадцати ретроспективных исследований сообщают об увеличении PFS и OS при проведении иммунотерапии в утренние-дневные часы у больных с различными локализациями опухоли (рис.1).
Рисунок 1.
Сравнение медиан PFS и OS при проведении иммунотерапии различных опухолей в ранние (синий цвет) и поздние часовые интервалы (фиолетовый цвет) [1].
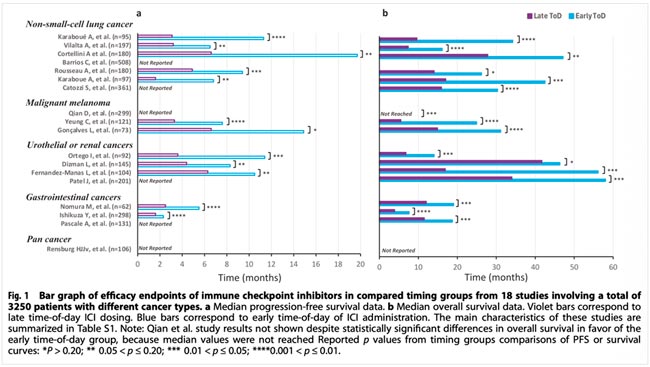
И вот только что были опубликованы результаты китайского рандомизированного исследования III фазы LungTIME-C01, включившего 210 пациентов, не получавших ранее лечения по поводу немелкоклеточного рака легкого IIIC-IV стадий без драйверных мутаций [2]. Пациенты были случайным образом распределены в соотношении 1:1 либо в группу раннего, либо в группу позднего начала лечения, определяемого введением первых четырех циклов анти-PD-1 препарата до или после 15:00. Пациенты исключались из исследования, если у них имелись симптоматически активные метастазы в центральной нервной системе, пневмонит, требующий глюкокортикоидной терапии, или активное аутоиммунное заболевание. Пембролизумаб или синтилимаб (200 мг) вводили каждые три недели до прогрессирования заболевания, смерти или возникновения непереносимых побочных эффектов. Синтилимаб (Тайвит®) – это гуманизированное моноклональное антитело IgG4, которое блокирует рецептор PD-1. Разработанный совместно компаниями Innovent Biologics и Eli Lilly, он одобрен в Китае для лечения рецидивирующей/рефрактерной лимфомы Ходжкина и различных солидных опухолей, включая немелкоклеточный рак легкого и рак желудка. Иммунотерапию комбинировали с химиотерапией каждые три недели в зависимости от гистологического типа. Пациенты с плоскоклеточным раком получали карбоплатин (AUC×5) и наб-паклитаксел (200 мг/м2). Пациенты с гистологически подтвержденной аденокарциномой получали карбоплатин (AUC×5) и пеметрексед (500 мг/м2) с последующей поддерживающей терапией пеметрекседом после 4-го цикла. Первичной конечной точкой была медиана PFS (ВБП), а вторичными конечными точками – медиана OS и частота объективного ответа (ЧОО).
Среди 210 рандомизированных пациентов с медианой возраста 60 лет в общем хорошем состоянии (PS 0/1) преобладали мужчины (90%), стадия IV (80%), плоскоклеточный рак (55%). Большинство пациентов (n=162, 77,1%) получали синтилимаб, в то время как 48 пациентов (22,9%) получали пембролизумаб. Все пациенты получили первые четыре цикла иммунохимиотерапии в пределах установленного протоколом временного окна (до или после 15:00). Медианное время начала инфузии ингибиторов контрольных точек иммунитета в группах с ранним и поздним временным окном составило 10:55 (7:34-14:00) и 15:57 (15:00-20:39) соответственно. Поддерживающая терапия ингибиторами контрольных точек иммунитета (ICI) была назначена 98,1% пациентов в группе раннего начала терапии и 96,2% пациентов в группе позднего начала терапии. Большинство пациентов, отнесенных к группе раннего начала терапии, продолжали получать инфузии преимущественно до 15:00, в то время как пациенты в группе позднего начала терапии преимущественно получали их после 15:00, несмотря на отсутствие в протоколе каких-либо положений о начале терапии после четвертого цикла.
При медиане наблюдения 28,7 мес. медиана PFS составила 11,3 мес. в группе раннего ведения и 5,7 мес. в группе позднего, что соответствует достоверному снижению относительного риска прогрессирования на 40% (HR=0,60; р<0,001). Медиана OS составила 28,0 и 16,8 мес. соответственно с достоверным снижением относительного риска смерти на 42% (HR=0,58; р<0,001). При многофакторном анализе OS во всех изученных подгруппах отмечался выигрыш при раннем назначении иммунотерапии. Объективный противоопухолевый эффект был зарегистрирован у 69% больных при раннем и у 56% при позднем введении иммунотерапии (р=0,046). Связанные с лечением нежелательные явления соответствовали установленному профилю безопасности, не отмечено существенной разницы в частоте серьезных осложнений между двумя группами. Иммунофенотипирование периферической крови показало, что ранние инфузии иммунотерапии были связаны с повышением уровня циркулирующих CD8+ Т-клеток и более высоким соотношением активированных (CD38+ HLA-DR+) к истощенным (TIM-3+PD-1+) CD8+ Т-клеткам. Эти изменения в субпопуляциях Т-клеток, вероятно, отражают повышенную цитотоксическую активность и могут частично объяснить улучшенную клиническую эффективность, наблюдаемую в группе раннего введения иммунотерапии. Ранее проведенные исследования также связывали более высокие показатели периферических CD8+ Т-клеток с улучшенным ответом опухоли на ингибиторы контрольных точек иммунитета.
Рисунок 2.
Кривые PFS в зависимости от времени введения иммунотерапии.
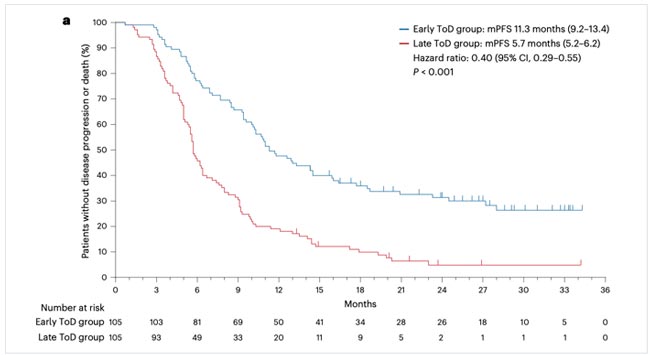
Рисунок 3.
Кривые OS в зависимости от времени введения иммунотерапии.
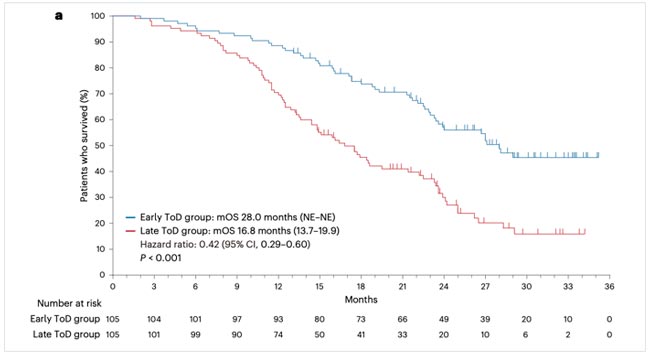
Таким образом, получено еще одно свидетельство о влиянии циркадных ритмов на результаты противоопухолевого лекарственного лечения. В частности, введение ингибиторов контрольных точек в утренние и ранние дневные часы достоверно и значительно повышает эффективность иммунохимиотерапии немелкоклеточного рака легкого в сравнении с введением после 15:00. В китайском исследовании медиана времени введения в ранней группе составила 10:55, т.е. половина больных получила лечение до этого времени. Вряд ли можно рассчитывать на разницу в результатах терапии при ведении препаратов в 14:00 и 16:00. Вероятно, выигрыш был получен за счет пациентов, лечившихся в утренние и ранние дневные часы (до 12:00). Это на первый взгляд простое правило – лечи утром, чтобы достигнуть большего противоопухолевого эффекта, – не так просто внедрить в нашу клиническую практику дневных стационаров, которые и осуществляют большинство курсов химиоиммунотерапии. В условиях большого числа пациентов, бюрократических процедур получения препаратов и последующего их разведения многие больные начинают лечение во второй половине дня. Но даже в этих условиях следует стараться соблюсти первоочередность введения иммунотерапии при лечении всех нозологий, так это позволяет достигнуть лучших результатов терапии.
Источники:
- Karaboué A, Innominato PF, Wreglesworth NI, et al. Why does circadian timing of administration matter for immune checkpoint inhibitors’ efficacy? British Journal of Cancer. 2024, 131: 783-796.
- Huang Z, Zeng L, Ruan Z, et al. Time-of-day immunochemotherapy in nonsmall cell lung cancer: a randomized phase 3 trial. Nature Medicine. Published online: February 2, 2026.
НОВОСТИ ОНКОЛОГИИ / ДВУХСТОРОНЯЯ САЛЬПИНГЭКТОМИЯ КАК ЭФФЕКТИВНЫЙ МЕТОД ПРОФИЛАКТИКИ РАКА ЯИЧНИКОВ
Автор: Тюляндин Сергей Алексеевич
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
профессор, доктор медицинских наук, Москва
Рак яичников остается одним из самых смертельных гинекологических злокачественных новообразований, при этом, несмотря на достижения в лечении, за последние десятилетия наблюдается незначительное улучшение пятилетней выживаемости. В большинстве случаев диагноз ставится на поздней стадии из-за отсутствия эффективных стратегий скрининга. Появляющиеся данные свидетельствуют о том, что фаллопиевы трубы являются местом возникновения значительного количества серозных опухолей яичников высокой степени злокачественности, наиболее распространенной формы эпителиального рака яичников, поэтому их называют тубоовариальной карциномой. Это изменение парадигмы привело к разработке и внедрению оппортунистической сальпингэктомии – удаления фаллопиевых труб во время других показанных хирургических вмешательств – в качестве профилактического подхода. Хотя первоначально она предлагалась для групп высокого риска, таких как носители патологических вариантов генов BRCA1 и BRCA2, в настоящее время оппортунистическая сальпингэктомия более широко применяется у женщин со средним риском, которым проводятся операции на органах таза и отдельные операции на брюшной полости по другим показаниям. В опубликованном консенсусе Европейского общества гинекологической онкологии (ESGO) анализируются имеющиеся свидетельства об эффективности профилактической сальпингэктомии и даются рекомендации по ее дальнейшему изучению и более широкому внедрению в клиническую практику [1].
Многочисленные систематические обзоры и метаанализы демонстрируют, что сальпингэктомия связана со значительным снижением риска рака маточных труб и яичников, хотя большая часть данных носит ретроспективный характер, и рандомизированные контролируемые исследования отсутствуют. Крупнейший систематический обзор, опубликованный в 2023 году, включал 158 исследований с различными дизайнами и показал, что двусторонняя сальпингэктомия может снизить риск рака маточных труб и яичников до 80% по сравнению с отсутствием сальпингэктомии. Теоретически можно ожидать, что столь высокая превентивная способность сальпингэктомии при ее широком применении может снизить смертность от рака яичников в Соединенных Штатах на 15% [2]. Общенациональное популяционное исследование в Швеции, в котором анализировались данные о 5 452 170 женщинах, перенесших ранее операцию по поводу доброкачественного образования органов малого таза в период с 1973 по 2009 год, обнаружило среди них 3 051 женщину с выполненной двусторонней сальпингэктомией. Выполнение двухсторонней сальпингэктомии достоверно снизило риск развития рака яичников на 65% [3]. В только что опубликованном популяционном исследовании в провинции Британская Колумбия (Канада) были проанализированы результаты лечения 85 823 оперированных женщин, перенесших гистерэктомию (45 296 женщин) или двухстороннюю сальпингэктомию (40 527) с целью контрацепции в Британской Колумбии в период с 2008 по 2020 год [4]. За период наблюдения от 5 до 8 лет было диагностированы 26 случаев опухолей яичников у лиц после сальпингэктомии, при этом только у 6 (23,1%) из них они были представлены серозными карциномами высокой злокачественности по сравнению с 642 из 942 (68,1%) случаев в группе только гистерэктомии. Это соответствует достоверному снижению относительного риска развития серозной карциномы яичников высокой степени злокачественности на 78%.
Оппортунистическая сальпингэктомия получает все большую поддержку со стороны профессиональных сообществ по всему миру. Однако, несмотря на потенциал снижения частоты возникновения рака маточных труб и яичников без видимого значительного дополнительного риска, на практике этот метод не получил широкого распространения в лечении пациенток. Это осторожное отношение к эффективной профилактической стратегии объясняется продолжающимися дискуссиями относительно ее экономической эффективности, хирургической безопасности и долгосрочных результатов.
Важно отметить, что данные также свидетельствуют о том, что оппортунистическая сальпингэктомия не оказывает существенного влияния на краткосрочную функцию яичников. В рандомизированных контролируемых исследованиях и систематических обзорах гормональные маркеры, такие как АМГ и ФСГ, оставались стабильными после операции, и существенных различий в овариальном резерве не наблюдалось. Однако в некоторых наблюдательных исследованиях было отмечено повышение риска развития симптомов менопаузы после оппортунистической двухсторонней сальпингэктомии, в то время как другие не выявили влияния операции на сроки наступления менопаузы или необходимость гормональной терапии. Это подчеркивает сохраняющийся пробел в знаниях относительно долгосрочных эндокринных последствий оппортунистической сальпингэктомии, особенно у молодых женщин. С точки зрения периоперационной безопасности данные свидетельствуют о том, что сальпингэктомия является технически выполнимой процедурой с минимальным увеличением операционного времени и без значительного увеличения хирургических осложнений. Эти результаты согласуются как для гинекологических, так и для негинекологических процедур и подходов, таких как лапароскопические и открытые операции. Выполнение сальпингэктомии увеличивает время открытых операций на 10-15 минут, а лапароскопических на 15-20 минут.
Экономическая целесообразность выполнения оппортунистической сальпингэктомии была проанализирована на основании данных медицинского регистра Германии. Были смоделированы 4 модели использования оппортунистической билатеральной сальпингэктомии: 1-я модель предполагала ее выполнение при любой операции на брюшной полости, 2-я – выполнение при гинекологических операциях, 3-я – при операции стерилизации и 4-я модель (контрольная) предполагала невыполнение сальпингэктомии при любом оперативной вмешательстве. Подсчитано, что при 1-й модели ежегодная частота выполнения сальпингэтомии увеличится в 3,5 раза по сравнению с 3-й моделью (286 736 против 82 319). При сравнении с 4-й моделью снижение частоты возникновения рака яичника составит 15,34% при модели 1, 9,78% при 2-й и 5,48% при 3-й модели. При установлении стоимости сальпингэктомии на уровне 216,19 евро (рассчитанной на основе средней продолжительности операции и стоимости операционной минуты) ее внедрение приведет к ежегодной экономии затрат на здравоохранение Германии более 10 миллионов евро при численности женского населения около 42 миллионов человек и средней ожидаемой продолжительности жизни 85 лет.
На основании имеющихся данных эксперты ESGO считают, что оппортунистическая сальпингэктомия значительно снижает риск развития тубоовариального карциномы, не оказывает негативного влияния на краткосрочный овариальный резерв, минимально увеличивает время операции и не повышает периоперационные риски. Поэтому сальпингэктомию следует рассматривать при всех гинекологических операциях, а по возможности – и при плановых негинекологических операциях на органах таза и отдельных операциях на брюшной полости у женщин, подверженных общему риску развития рака маточных труб и яичников и не желающих иметь детей в будущем. В настоящее время многие международные общества, включая Международную федерацию гинекологии и акушерства (FIGO), рекомендуют сальпингэктомию в качестве предпочтительного метода стерилизации для женщин, а не перевязку маточных труб, учитывая ее потенциальную способность снизить риск рака маточных труб и яичников. Врачи должны предоставлять четкую и сбалансированную информацию о преимуществах снижения риска рака яичников и имеющихся на данный момент ограниченных данных о долгосрочном влиянии сальпингэктомии на функционирование яичников. Возраст сам по себе не должен использоваться для исключения пациенток из числа потенциальных преимуществ сальпингэктомии, хотя консультирование должно отражать существующую неопределенность в отношении ее влияния на сроки наступления менопаузы. В будущих исследованиях следует отдавать приоритет долгосрочным проспективным исследованиям со стандартизированной оценкой гормонального фона и последующим наблюдением за временем появления симптомов менопаузы и ее наступления, особенно в более молодых возрастных группах.
Источники:
- Piek JM, Schauwaert J, Ellis LB. et al. Opportunistic salpingectomy for prevention of tubo-ovarian carcinoma: the European Society of Gynaecological Oncology consensus statements. JAMA. Published online: February 2, 2026.
- Kahn RM, Gordhandas S, Godwin K, et al. Salpingectomy for the primary prevention of ovarian cancer: a systematic review. JAMA Surgery. 2023; 158: 1204-1211.
- Falconer H, Yin L, Grönberg H, et al. Ovarian cancer risk after salpingectomy: a nationwide population-based study. J. Natl. Cancer Inst. 2015; 107: dju410.
- Kather K, Habib A, Runnebaum ID, et al. Ovarian cancer prevention through opportunistic salpingectomy during abdominal surgeries: a cost-effectiveness modeling study. PLOS Medicine. Published: January 30, 2025.
- Sowamber R, Mei AJ, Kaur P, et al. Serous ovarian cancer following opportunistic bilateral salpingectomy. JAMA Network Open. 2026; 9: e2557267.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ЛОКАЛЬНАЯ ТЕРАПИЯ ОЛИГОМЕТАСТАЗОВ: ЕЩЕ ОДИН ПЛЮС К ДОКАЗАТЕЛЬНОЙ БАЗЕ
Олигометастатическое заболевание представляет собой проксимальный отрезок спектра метастазирования, и для лечения пациентов с олигометастазами различных опухолей все чаще используются локальные методы, вкупе получившие название metastasis-directed therapy (MDT), иными словами – таргетно направленная терапия метастазов. Подобных работ и публикаций имеется немало, однако многие авторы отмечают недостаток доказательств уровня 1.
В февральском номере журнала Lancet Oncology опубликованы результаты крупного систематического обзора и метаанализа индивидуальных данных WOLVERINE по оценке эффективности MDT у больных с олигометастатическим раком простаты в сравнении со стандартной поддерживающей терапией. Критериями включения были опубликованные рандомизированные проспективные исследования с участием пациентов с олигометастатическим (до пяти метастазов) раком предстательной железы, в которых исследователи собрали достаточно данных для оценки выживаемости без прогрессирования и общей выживаемости. Данный систематический обзор проводился с момента создания баз данных (Embase, PubMed, CENTRAL, MEDLINE, and ClinicalTrials.gov) до 3 ноября 2023 года и был обновлен 4 мая 2025 года.
Первичными конечными точками были выживаемость без прогрессирования заболевания и общая выживаемость. Вторичными конечными точками были выживаемость без рентгенологического прогрессирования и выживаемость без резистентности к кастрации. Первичный анализ проводился в подгруппе исследований, в которых пациенты были рандомизированы на группы, получавшие MDT плюс стандартное лечение (SOC) или только стандартное лечение (SOC).
Из 2975 исследований, отобранных для скрининга, в анализ были включены семь исследований фазы 2, в которых случайным образом были распределены 574 пациента. Для оценки эффективности MDT были использованы шесть исследований, в которых случайным образом 472 пациента были распределены в группы MDT плюс стандартная терапия (n=248) против стандартной терапии (n=224). Медиана времени наблюдения составила 40,7 мес. (межквартильный диапазон 25,6-53,7). MDT была связана с улучшением выживаемости без прогрессирования (ОР 0,44 [95% ДИ 0,35-0,56], p<0,0001; ОР на уровне пациента 0,45 [0,35-0,57], p<0,0001), выживаемости без рентгенологического прогрессирования (ОР на уровне исследования 0,60 [0,42-0,85], p=0,0039; ОР на уровне пациента 0,59 [0,46-0,76], p<0,0001) и выживаемости без резистентности к кастрации (ОР на уровне исследования 0,58 [0,37-0,92], p=0,019; ОР на уровне пациента 0,58 [0,37-0,91], p=0,017). Связь между MDT и общей выживаемостью показала HR 0,63 (95% ДИ 0,39-1,00; p=0,051) в анализе на уровне исследования и 0,64 (95% ДИ 0,40-1,01; p=0,057) в анализе на уровне пациента.
Рисунок 1.
Преимущества добавления MDT к стандартному лечению в отношении ВБП (А), выживаемости без радиологического прогрессирования (В), ОВ (С) и выживаемости без резистентности к кастрации (D).

Рисунок 2.
Кривые выживаемости по данным анализа.

Исследование WOLVERINE продемонстрировало эффективность MDT при олигометастатическом раке предстательной железы в отношении выживаемости без прогрессирования заболевания, выживаемости без радиологического прогрессирования и выживаемости без резистентности к кастрации. Улучшение общей выживаемости не было значимым, и необходимы дальнейшие исследования. При этом авторы отметили низкий уровень токсичности MDT, что делает данную опцию весьма привлекательной.
Источник: Chad Tang, et al. Metastasis-directed therapy and standard of care versus standard of care for oligometastatic prostate cancer (WOLVERINE): a systematic review and individual patient data meta-analysis from the X-MET collaboration. Lancet Oncol. 2026 Feb; Vol.27, Issue 2, P.181-190.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / SABR И ИММУНОТЕРАПИЯ ДЛЯ УВЕЛИЧЕНИЯ ЧАСТОТЫ PCR: ИССЛЕДОВАНИЕ 2 ФАЗЫ
Несмотря на уже имеющиеся отличные отдаленные результаты проспективных исследований по применению стереотаксической лучевой терапии при раннем раке легкого (в частности, обновленное исследование STARS [1]), скепсис в отношении этого метода все еще присутствует. Причина – более высокий процент регионарного и отдаленного прогрессирования, особенно при IB стадии, что, впрочем, не отразилось на общей выживаемости по данным STARS. Масла в огонь подлили результаты исследования MISSILE по неоадъювантному применению SABR: в нем показатель полного патоморфологического ответа составил только 60% [2]. Теоретически сочетание лучевой терапии и иммунотерапии может улучшить контроль над опухолью за счет нарушения микроокружения, содействующего разрушению опухолевых клеток, и запуска системной активации иммунной системы.
Бразильские авторы инициировали II фазу открытого одногруппового исследования, направленного на оценку эффективности и безопасности неоадъювантной терапии ниволумабом в сочетании со стереотаксической лучевой терапией (SABR) у пациентов с немелкоклеточным раком легкого (НМРЛ) размером до 4 см без поражения лимфатических узлов [3]. При этом пациенты должны были подходить для хирургического вмешательства, имея адекватную функцию легких и сердечно-сосудистой системы.
Дозы ЛТ варьировали от 50 Гр за 5 фракций (таких пациентов было большинство, n=21) до 54 Гр за 3 фракции. Ниволумаб вводился в дозе 360 мг каждые 21 день в течение трех доз в сочетании с SABR, которая начиналась одновременно с первым циклом. Впоследствии пациенты шли на хирургическую резекцию через 10 недель после последней дозы облучения. Первичной конечной точкой была частота патологического полного ответа (pCR) на момент операции. Вторичные конечные точки включали частоту выраженного патологического ответа (MPR), безопасность, выживаемость без событий и общую выживаемость через 12 месяцев, а также комплексный анализ биомаркеров.
Всего было включено 25 пациентов, преимущественно женщины (68%), средний возраст – 68 лет. Средний размер опухолей составил 2,47 см.
В общей сложности 24 пациента полностью завершили лечение в экспериментальной группе и приступили к хирургическому вмешательству. Первичная конечная точка – патологический полный ответ (pCR) – была достигнута у 19 из 24 пациентов (79,2%; 95% доверительный интервал 57-92%, p=0,0875 в анализе по протоколу). Максимальный ответ (MPR) наблюдался в 20 случаях (83,3%; 95% ДИ 61,8-94%). Четыре пациента не достигли MPR, при этом у одного из них наблюдалась полностью жизнеспособная опухоль. На сегодняшний день рецидивов не отмечено, локорегиональный и отдаленный контроль над опухолью составил 100%, 12-месячная выживаемость без событий и общая выживаемость составили 84%, при этом медиана для обоих показателей не была достигнута. Один пациент умер от алкогольного гепатита, не связанного с лечением, и не подвергался резекции. Два пациента умерли от хирургических осложнений.
Рисунок 1.
Результаты патоморфологического ответа в исследовании.
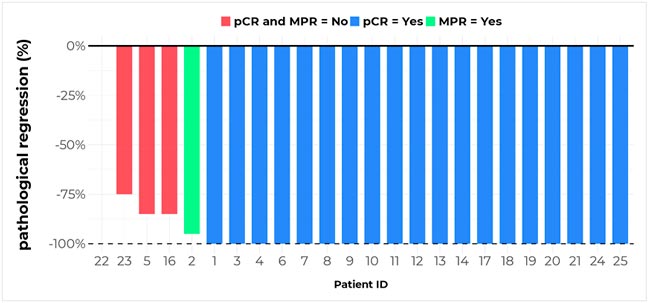
Токсичность лечения была преимущественно 1-2 степени, без зафиксированных случаев иммуноопосредованного пневмонита.
Неоадъювантная комбинация из трех доз ниволумаба и стереотаксической лучевой терапии (SABR) показала высокую частоту полного патологического ответа (pCR) при немелкоклеточном раке легкого I стадии. В отличие от исследования MISSILE, пациенты в бразильском исследовании получили еще одну дополнительную неделю для реализации эффекта проведенного исследования, что, возможно, сыграло позитивную роль в увеличении частоты pCR. Полное отсутствие изменений в опухоли после проведенного лечения у одного пациента, по мнению многих экспертов, выглядит странно. Возможно, этот больной являлся носителем мутации KEAP1, определяющей высокую радиорезистентность, но этой информации авторы не дали.
Безусловно, необходимы дальнейшие, более крупные и сравнительные проспективные исследования для оценки эффективности этой лечебной комбинации – SABR и иммунотерапии – у пациентов с неоперабельным по медицинским показаниям немелкоклеточным раком легкого и возможности безопасного отказа от хирургического вмешательства у пациентов, которым показана резекция.
Источники:
- Kleber T, et al. Ten-year outcomes of the revised STARS trial comparing radiation and surgery for early-stage non-small cell lung cancer. IJROBP. 2025; 123 (1): S119.
- Palma DA, Nguyen TK, Louie AV, et al. Measuring the integration of stereotactic ablative radiotherapy plus surgery for early-stage non-small cell lung cancer: a phase 2 clinical trial. JAMA Oncol. 2019; 5: 681-688.
- Schvartsman G, Amirato YM, Monfardini F, et al. Pathologic responses to stereotactic ablative radiotherapy in combination with nivolumab for early stage NSCLC: a phase 2 study. JTO Clin Res Rep. 2026; 7: 100940.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / О СТАРОМ ДОБРОМ ТАМОКСИФЕНЕ – В ДОЛГОСРОЧНОМ АНАЛИЗЕ STO
У пациенток с рецептор-положительным раком молочной железы (РМЖ) стандартом адъювантного лечения является гормональная терапия тамоксифеном; при этом сохраняется весьма значительный поздний риск отдаленного рецидива, однако долгосрочная польза тамоксифена в зависимости от люминального подтипа РМЖ остается недостаточно изученной.
Шведские авторы провели вторичный анализ рандомизированных исследований с применением тамоксифена в Стокгольме (STO, 1976-1997 гг., n=3930) с 20-летним периодом наблюдения. Блоки FFPE были доступны для 2250 пациенток. В итоге были проанализированы данные 952 больных с ER-положительными/
У пациентов с опухолями люминального типа А наблюдался низкий ранний риск и умеренная ранняя польза от терапии тамоксифеном (5-летняя DRFI у леченных пациентов по сравнению с контрольной группой: 93% против 89%, абсолютная разница 4%), которая увеличилась за 20-летний период наблюдения (20-летняя DRFI: 76% против 66%, абсолютная разница 10%), что подчеркивает долгосрочную пользу. Напротив, у пациентов с опухолями люминального типа B наблюдался больший ранний риск и польза от лечения (5-летняя частота отдаленных метастазов: 72% против 57%, абсолютная разница 15%), которые оставались стабильными с течением времени (20-летняя частота отдаленных метастазов: 55% против 37%, абсолютная разница 18%) (рис.1).
Рисунок 1.
Выживаемость без отдаленных рецидивов в группах люминальных А и В подтипов в зависимости от приема или отказа от тамоксифена.
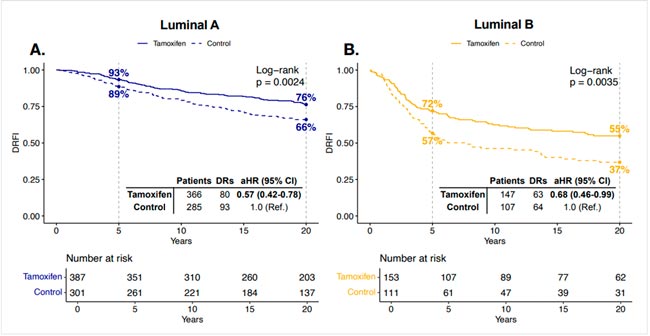
Многофакторный анализ показал, что пациенты с люминальными опухолями получали пользу от терапии тамоксифеном (скорректированное отношение рисков [aHR] для люминальных опухолей типа А = 0,57, 95% ДИ 0,42-0,78, а для люминальных опухолей типа В aHR = 0,68, 95% ДИ 0,46-0,99). Пациенты с благоприятными характеристиками опухоли получали пользу независимо от люминального подтипа.
Тамоксифен снижает долгосрочный риск отдаленных метастазов как при люминальных опухолях типа А, так и типа В, хотя время получения пользы варьирует в зависимости от подтипа. При В-подтипе выигрыш тамоксифена ранний и четкий, при А-подтипе разница в ранние сроки не выражена, но реальный протективный эффект проявляется спустя 10-15 лет. Даже после лечения у пациентов с люминальными опухолями сохраняется значительный отдаленный риск рецидива, который мы не можем игнорировать – что подчеркивает необходимость длительного наблюдения.
Источник: Danielsson O, Dar H, Nordenskjöld A, Perez-Tenorio G, Nordenskjöld B, Fornander T, Stål O, Tobin NP, Tutzauer J, Johansson A, Lindström LS. Tamoxifen therapy benefit in luminal A and B breast cancer with 20-year follow-up. J Natl Cancer Inst. 2026 Feb 19; djag049. doi: 10.1093/jnci/djag049. Epub ahead of print. PMID: 41712503.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / РМЖ И РЧА: АДЕКВАТНАЯ АЛЬТЕРНАТИВА?
Пока сложно представить себе, что лечение раннего рака молочной железы (РМЖ) может обойтись без хирургического вмешательства, когда для этого есть все условия. Тем не менее, варианты малоинвазивных или неинвазивных процедур изучаются многими авторами.
18 февраля в журнале Breast Oncology опубликованы 5-летние результаты японского мультицентрического проспективного исследования 3 фазы RAFAELO по оценке эффективности радиочастотной аблации в качестве возможной альтернативы резекции молочной железы при раннем РМЖ.
Пациенткам с единичным узлом в молочной железе, классифицированным как Tis-T1 (размер опухоли ≤1,5 см), N0M0, стадия 0-I, проводилась радиочастотная абляция (РЧА). Затем всем пациенткам проводилась лучевая терапия общей дозой 45-60 Гр. Первичной конечной точкой была 5-летняя выживаемость без рецидива опухоли в ипсилатеральной молочной железе (IBTRFS). Пороговое значение для клинически неприемлемой 5-летней выживаемости без рецидива опухоли было установлено на уровне 90% при одностороннем уровне значимости альфа 5%.
В общей сложности 370 пациентам была проведена РЧА, и 353 пациентки (медиана возраста 55 [47-65] лет) завершили 5-летнее наблюдение. По основному показателю, частота выживаемости без рецидива в молочной железе через 5 лет составила 98,6% (90% ДИ 97,1-99,3%; 95% ДИ 96,6-99,4%). Нижняя граница 90% ДИ была выше порогового значения 90%, что свидетельствует о не меньшей эффективности РЧА по сравнению с частичной мастэктомией в исторической контрольной группе. В ходе исследования было отмечено два рецидива в ипсилатеральной молочной железе. Изъязвление кожи 3-й степени и выше наблюдалось только у одного из 370 пациентов.
Авторы сделали вывод, что радиочастотная абляция является безопасным малоинвазивным методом лечения РМЖ на ранних стадиях, сопоставимым по эффективности с частичной мастэктомией. Маловероятно, что РЧА будет широко использоваться в качестве альтернативы в рутинной практике уже сейчас, скорее всего только в клинических исследованиях и у тщательно отобранных пациентов с люминальной опухолью и низкой опухолевой нагрузкой.
Источник: Kinoshita T, Takayama S, Fujisawa T, et al. Radiofrequency Ablation for Early Stage Breast Cancer as a Potential Alternative to Partial Mastectomy: 5-Year Results from the Multiple-Center, Single-Arm, Phase 3 RAFAELO Study (NCCH1409). Ann Surg Oncol. 2026. https://doi.org/
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ПОТЕРЯ ВКУСА ПРИ ОБЛУЧЕНИИ ОПУХОЛЕЙ ГОЛОВЫ И ШЕИ: ЧТО ПРОИСХОДИТ И ПОЧЕМУ
Автор: Черчик Алексей
Врач, радиационный онколог, Paul Scherrer Institute,
Швейцария
Нарушение вкуса – один из самых частых и недооцененных побочных эффектов лучевой терапии при опухолях головы и шеи. Большое проспективное исследование китайских авторов, инициированное в августе 2023 года и опубликованное в журнале Radiation Oncology, на 444 пациентах подробно показало, когда, почему и у кого эта проблема возникает чаще всего.
Насколько это распространено
- Потеря вкуса возникает у 86% пациентов в процессе лечения.
- У 60% она достигает средней или тяжелой степени.
- Максимальная выраженность обычно отмечается на 5-6 неделе лечения.
Иначе говоря: для большинства пациентов это не редкое осложнение, а ожидаемая реальность лечения.
Как развивается потеря вкуса
По мере накопления дозы лучевой терапии, особенно в сочетании с химиотерапией, симптомы нарастают: в начале лечения изменения минимальны, к середине курса проявление становится выраженным, а к 6 неделе до 90% пациентов имеют значимое нарушение вкуса. После завершения терапии часть симптомов уменьшается, но у многих сохраняется на длительный срок.
Кто в группе повышенного риска
Самый важный немодифицируемый фактор – низкий индекс массы тела. Пациенты с худшим нутритивным статусом теряют вкус чаще и тяжелее, вероятно из-за дефицита микроэлементов, включая цинк. При этом:
- возраст и пол роли не играют;
- стадия и локализация опухоли не критичны;
- химиотерапия не усиливает эффект.
Главный повреждающий фактор – сама доза ЛТ.
Китайские авторы показали, что острое нарушение вкуса было значительно связано с индексом массы тела (ИМТ) (ОР 0,936, P=0,029).
Ключевой орган риска
Главный «виновник» в развитии подобного осложнения – околоушные слюнные железы. Именно средняя доза на них лучше всего предсказывает вероятность потери вкуса:
- при дозе около 24 Гр риск острой потери вкуса достигает 50%, эта доза считается максимально допустимой;
- уменьшение количества и загустение слюны нарушает доставку вкусовых сигналов к рецепторам.
Также имеют значение дозы облучения на поднижнечелюстных железах и полости рта, поэтому они обязательно должны быть оконтурены как органы риска.
Средняя доза (Dmean) на околоушных железах была наиболее явным прогностическим фактором для развития острого нарушения вкуса. Dmean околоушных желез для прогнозируемых 10%, 30% и 50% вероятностей развития долгосрочной потери вкуса составляли 45, 78 и 94 Гр через 3 месяца и 80, 97 и 105 Гр через 6 месяцев соответственно.
Влияние на качество жизни
Потеря вкуса тесно связана с сухостью во рту, развитием мукозита, трудностями глотания, потерей аппетита, тревожностью и психологическим дистрессом, ухудшением питания и истощением. Это уже не «малое неудобство», а фактор, напрямую влияющий на переносимость лечения, его исходы и отдаленные результаты.
Практические выводы
- Защита слюнных желез должна быть одним из главных приоритетов при планировании лучевой терапии; существующие модели прогнозирования риска позволяют заранее оценить вероятность осложнений.
- Пациенты с низким индексом массы тела требуют особого внимания, для них адекватная нутритивная и психологическая поддержка так же важны, как и техника и технологии облучения.
Главная мысль
Потеря вкуса при лучевой терапии – дозозависимое и предсказуемое осложнение. Чем точнее планирование и чем бережнее отношение к слюнным железам, тем выше шанс сохранить не только вкус, но и качество жизни пациента.
Источник: Su-Man Zhang, et al. Dose-dependent taste dysfunction in head and neck cancer patients receiving radiotherapy. Radiat Oncol. 2025. https://doi.org/
НОВОСТИ ОНКОЛОГИИ / ФИНАЛЬНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ SONIA У БОЛЬНЫХ МЕТАСТАТИЧЕСКИМ ЛЮМИНАЛЬНЫМ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Автор: Тюляндин Сергей Алексеевич
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
профессор, доктор медицинских наук, Москва
Исследование SONIA не раз было предметом оживленных дискуссий и споров вследствие актуальности изучаемой проблемы: использовать ли назначение CDK4/6 ингибиторов в первой или во второй линии гормонотерапии у больных метастатическим гормоночувствительным (HR+) раком молочной железы (РМЖ). Эта группа препаратов показала свою эффективность в обеих линиях, и исследование ставило цель определить оптимальную последовательность с точки зрения эффективности, токсичности и экономики использования совместного применения гормонотерапии и ингибиторов CDK4/6.
Рисунок 1.
Дизайн исследования SONIA.
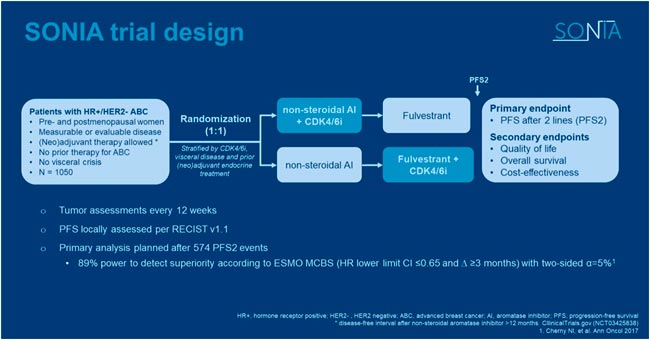
Дизайном исследования SONIA предполагалась рандомизация всех больных для проведения первой линии гормонотерапии ингибиторами ароматазы только или их комбинации с ингибиторами CDK4/6 (рис.1). При прогрессировании больным, получившим комбинацию, назначали фулвестрант, а получившим только ингибиторы ароматазы – комбинацию фулвестранта и ингибиторов CDK4/6. Основным критерием эффективности была PFS2, т.е. медиана времени от рандомизации до прогрессирования на фоне второй линии гормонотерапии фулвестрантом. Вторичными критериями были качество жизни, общая выживаемость и экономическая эффективность. В исследование разрешалось включать пре- и постменопаузальных больных с измеряемыми или оцениваемыми проявлениями метастатического процесса, не получавших лекарственной терапии по поводу метастатической болезни (разрешалась предшествующая нео- и/или адъювантная терапия) с отсутствием клинических признаков висцерального кризиса. Стратификация проводилась в зависимости от приема конкретного ингибитора CDK4/6, наличия висцеральных метастазов, предшествующей нео/адъювантной гормонотерапии. Статистическая гипотеза предполагала, что назначение CDK4/6 в первой линии на основании оценки PFS2 уменьшит относительный риск прогрессирования на 35% (HR<0,65), что потребовало включения в исследование 1040 больных с медианой возраста 63 года, в основном постменопаузальных (86%) с наличием висцеральных метастазов (56%). В качестве ингибиторов CDK4/6 у 91% больных назначали палбоциклиб, рибоциклиб, и абемациклиб был назначен 8% и 1% больных соответственно.
При первоначальном анализе исследования было показано, что назначение CDK4/6 в первой линии существенно увеличило медиану PFS1 c 16,1 до 24,7 мес., что соответствует достоверному снижению относительного риска прогрессирования на 41% (HR=0,59; p<0,0001). Однако при оценке PFS2 в зависимости от назначения CDK4/6 в первой и второй линиях (основная конечная точка исследования), разница между двумя группами потеряла свою достоверность и составила 31 и 26,8 мес. соответственно (HR=0,87; p=0,10). Подгрупповой анализ не позволил определить пациентов, у которых наблюдался выигрыш PFS2 от назначения CDK4/6 в первой линии. При оценке качества жизни получен одинаковый счет в обеих группах по опроснику FACT-B. Однако было отмечено, что при назначении ингибиторов CDK4/6 в первой линии зарегистрировано на 42% больше осложнений 3-4 степени, в основном за счет нейтропении, анемии, тромбоцитопении и нарушения функции печени. Авторы подсчитали, что продолжительность приема CDK4/6 при назначении в первой и второй линиях составила 24,6 и 8,1 мес. соответственно, что увеличило стоимость лечения примерно на 200 000 USD на каждого больного при использовании в первой линии. Но оставался неизвестным другой важный критерий – продолжительность жизни. В феврале 2026 года в журнале JAMA Oncology были представлены данные об общей выживаемости [1]. При медиане наблюдения 58,5 мес. медиана продолжительности больных, получавших ингибиторы CDK4/6 в первой линии, составила 47,9 мес., во второй – 48,1 мес., разница статистически недостоверна. При подгрупповом анализе выявлена разница в продолжительности общей выживаемости в зависимости от менопаузального статуса. У пременопаузальных больных при назначении CDK4/6 ингибиторов в первой линии медиана общей выживаемости не была достигнута и составила 35,3 мес. при назначении во второй, что соответствует снижению относительного риска смерти на 47% (HR=0,53). У постменопаузальных больных медианы общей выживаемости в зависимости от линии назначения CDK4/6 составили 46,9 и 49,7 мес. соответственно.
Были также обновлены результаты PFS2 – основного показателя эффективности двух стратегий. Медиана безрецидивной выживаемости после 2 линий терапии составила 31,9 мес. в группе первой линии и 26,7 мес. в группе второй линии, что соответствует достоверному снижению относительного риска прогрессирования на 18% (HR=0,82; P=0,01). Аналогично результатам общей выживаемости, подгрупповой анализ показал, что выживаемость без прогрессирования заболевания после 2 линий терапии улучшается при применении первой линии у пациенток в пременопаузе (31,5 и 19,4 мес.), но не у пациенток в постменопаузе (31,9 и 28,5 мес.). При прогрессировании заболевания 84,8% больных, получавших CDK4/6 в первой линии, и 84,2% во второй получали последующее лечение, преимущественно химиотерапевтическое. Частота серьезных побочных эффектов (gr. 3-4) на фоне первой-второй линий гормональной терапии составила 86,4% и 75,7% соответственно. Нейтропения была наиболее частым серьезным осложнением. Следует напомнить, что не было отмечено разницы в качестве жизни пациенток в сравниваемых группах, в то время как стоимость стратегии первой линии была на 200 000 евро дороже за счет более длительного приема ингибиторов CDK4/6 в первой линии.
Авторы этого академического исследования ответили на важный для клиницистов вопрос о месте комбинации ингибиторов ароматазы и CDK4/6 в лечении гормонозависимого HER2-негативного метастатического РМЖ. Полученные результаты свидетельствуют о том, что значительная часть пациентов с метастатическим ER-положительным раком молочной железы может быть успешно пролечена только эндокринной терапией в качестве начального лечения с обязательным комбинированием с ингибиторами CDK4/6 на более поздних стадиях заболевания. К этой группе относятся пациентки в постменопаузе, ранее не получавшие эндокринную терапию, или с индолентно протекающим заболеванием после ранее успешной адъювантной гормонотерапии, с умеренной опухолевой нагрузкой, где высока вероятность эндокринной чувствительности и возможности получения лечения при переходе на другую терапию. Напротив, у пациентов с более распространенным заболеванием или прогрессированием на фоне адъювантной эндокринной терапии, в пременопаузальном статусе целесообразно комбинированное лечение с ингибиторами CDK4/6 в первой линии. Именно такого подхода придерживаются сегодняшние клинические рекомендации RUSSCO.
При наличии множества вариантов лечения и множества линий терапии при распространенном раке молочной железы исследование SONIA подчеркивает важность анализа общей выживаемости и тщательной документации объема и адекватности лечения после прогрессирования заболевания. В рандомизированных глобальных исследованиях, где доступность последующих линий терапии может существенно различаться, существует риск дисбаланса в лечении после прогрессирования заболевания, который может легко повлиять на долгосрочные результаты, такие как выживаемость без прогрессирования (PFS2) или общая выживаемость (OS).
Исследование SONIA подчеркивает важность проведения рандомизированных исследований с перекрестным дизайном и оценкой не только PFS после первой линии, но и PFS2 и общей выживаемости. После того, как препарат продемонстрировал свою эффективность при более резистентных заболеваниях, остается важный вопрос: превосходит ли более раннее применение препарата более позднее с точки зрения долгосрочных результатов? Эти результаты, кроме PFS и OS, могут включать контроль симптомов, оценку стоимости терапии, поддержание качества жизни, а также время до других событий, связанных со значительным изменением состояния пациента, таких как диагностика метастазов в головном мозге, необходимость лучевой терапии или начало химиотерапии. И не всегда препарат, демонстрирующий большую противоопухолевую эффективность, нужно использовать на ранних этапах лечения. Примером этому служат уроки применения конъюгатов трастузумаба эмтанзина (T-DM1) и трастузумаба дерукстекана (T-DXd) при лечении метастатического HER2+ РМЖ. T-DXd продемонстрировал свою большую эффективность как в первой, так и второй линии лечения, в том числе и у больных после прогрессии на фоне TDM1. Поэтому в исследовании DESTINY-Breast03 медиана PFS2 при назначении T-DM1 в первой линии и T-DXd в случае прогрессирования составила 40,5 мес. и 25,7 мес. в случае обратной последовательности.
Источник: Wortelboer N, van Ommen-Nijhof A, Konings I, et al. Overall survival with first-line vs second-line CDK4/6 inhibitor use in advanced breast cancer: a randomized clinical trial. JAMA Oncol. Published online: February 19, 2026.
НОВОСТИ ASCO GU 2026 / РАК ПОЧКИ
Автор: Тимофеев Илья Валерьевич
Директор Бюро по изучению рака (Россия), член научного
комитета Колледжа Европейской Школы Онкологии (ESCO)
Итак, что же нового нам было представлено по раку почки на симпозиуме в этом году?
Во-первых – это адъювантная терапия, но уже с использованием комбинации пембролизумаба и белзутифана. Сама идея адъювантной терапии, как известно – снизить риск развития заболевания после хирургического лечения. Пемролизумаб является стандартом лечения в группе промежуточного и высокого риска. Есть некоторый скепсис в отношении промежуточного риска – но со стандартом не поспоришь.
Авторы проспективного рандомизированного исследования 3 фазы LITESPARK-022 добавили к адъювантному пембролизумабу препарат белзутифан у пациентов с промежуточным и высоким риском, чтобы улучшить результаты лечения. В исследование включались больные с гистологически подтвержденным почечно-клеточным раком (их было почти две тысячи), не получавшие никакого лечения, кроме хирургического. Все они были разделены на 2 подгруппы: промежуточно-высокого риска (рТ2N0, G4 или саркоматоидный вариант, или рТ3N0 и любая грейд) и высокого риска (рТ4N0, любая грейд, или любая рТ, любая грейд, но N+). Была и подгруппа пациентов с отдаленными метастазами, но условно излеченная путем резекции или стереотаксической лучевой терапии. Все включенные пациенты не позднее чем в течение 12 недель после операции рандомизировались либо в группу пембролизумаба с плацебо в течение года, либо пембролизумаба и белзутифана (препарата, ингибирующего фактор индукции гипоксии). Группы были хорошо сбалансированы, больше всего наблюдалось больных с промежуточным-высоким риском (более 80%), также большинство имели Grade 3-4.
Безрецидивная выживаемость была главным критерием в этом исследовании. Получено достоверное преимущество комбинации пембро и белзутифана в сравнении с монотерапией пембро; медиана ВБП не достигнута, однако статистические данные свидетельствуют о снижении риска прогрессирования при использовании комбинации на 28%. Кривые действительно расходятся, и вполне вероятно, что подобная комбинация может стать новым стандартом адъювантного лечения в группе промежуточно-высокого и высокого риска.
Рисунок 1.
Выживаемость без прогрессирования в группах

Подгрупповой анализ также показал преимущества ВБП для комбинации, однако они терялись в когорте пациентов с высоким риском и с М1 (отдаленными метастазами); впрочем, таких больных было мало, и сделать однозначные выводы мы не можем.
Данные по ОВ пока незрелые, и мы видим, что на данный момент более 90% пациентов живы в обеих группах, что демонстрирует сам факт высокой эффективности адъювантного лечения, но окончательные результаты будут сделаны после регистрации определенного числа событий.
Рисунок 2.
Общая выживаемость в группах

Добавление белзутифана увеличило риск развития НЯ 3 степени: 42% против 18% в группе монотерапии, однако это практически не сказалось на частоте отмены терапии в группах (10% против 7%). Наиболее часто встречаемая токсичность в группе комбинации – анемия (84%), а также утомляемость. Иммуноопосредованная токсичность была одинаковой в обоих рукавах. Еще одно важное НЯ, связанное с белзутифаном – гипоксия; все пациенты нуждались в регулярном измерении сатурации, но в реальности оксигенотерапия требовалась лишь 3% больных, в остальных случаях было достаточно активного наблюдения и коррекции дозы.
В итоге авторы сделали вывод, что комбинация п и Б в адъювантном режиме статистически и клинически значимо улучшили БРВ у больных ПКР промежуточно-высокого и высокого риска рецидива, что делает данный подход новым стандартом лечения подобной категории больных – однако нам всем нужен более длительный период наблюдения для окончательных выводов.
В отношении метастатического ПКР все давно уже ожидали результаты исследования CYTOSHRINK (РКИ 2 фазы по применению циторедуктивной стереотаксической ЛТ на неудаленную первичную опухоль в комбинации с ипилимумабом/ниволумабом у больных метастатическим ПКР). Основная гипотеза работы: разрушение первичной опухоли уменьшает опухолевую нагрузку, поддерживает локальный контроль, синергизм ЛТ с ИТ подразумевает высвобождение опухолевых антигенов при разрушении первичной опухоли, что позволяет иммунотерапии работать более эффективно.
В данном исследовании пациенты с метастатическим ПКР, подлежащие терапии ипилимумабом/ниволумабом, рандомизировались в соотношении 2:1 в 2 группы. В исследуемой группе пациенты получали 1 курс ипи/ниво, затем курс SBRT (35-40 Гр за 5 фракций) на первичную опухоль, затем продолжали еще 4 курса ИТ и ниволумаб в поддержке. В контрольной группе пациенты получали ипи/ниво 1-4 курса как стандартное лечение. Первичной конечной точкой стала 1-годичная ВБП.
Группы не были хорошо сбалансированы, возможно, это повлияло на результат. Так, опухоль Т3-4 наиболее часто встречалась в группе SBRT (70% против 46%). Разница (не в пользу SBRT) была отмечена и в количестве очагов, и в их локализации, т.е. некий дисбаланс в плане предиктивности был налицо.
Первичная конечная точка не была достигнута (рис.3), и авторами был сделан вывод, что исследование негативно.
Рисунок 3.
ВБП за 1 год в группах

По вторичным конечным точкам никакого выигрыша от добавления SBRT также получено не было, ни в отношении ВБП при промежуточном риске, ни при – тем более – высоком риске (где только ИТ продемонстрировала лучшие результаты), ни в отношении ОВ. Частота объективных ответов была выше в группе лучевой терапии, но это не отразилось в целом на результатах. При этом SBRT не увеличила токсичность лечения, что на самом деле радует, так как метод сейчас применяется действительно широко. На наш взгляд, требуются другие исследования, которые позволят соблюсти баланс между группами пациентов – и они идут, в том числе и в России, в частности пилотное исследование CARMENITA по сравнению результатов комбинации авелумаба с акситинибом или добавления циторедуктивной нефрэктомии с последующей комбинацией у больных с метастатическим ПКР, с неудаленной первичной опухолью, не получавшим ранее терапию. Предлагаем коллегам присоединиться к исследованию, которое лишь недавно было инициировано.
Наибольшей проблемой всегда был выбор лечения пациентов с метастатическим ПКР после уже проведенных нескольких линий терапии, прогрессирующих на иммунотерапии. Требовалось проспективное РКИ 3 фазы именно для таких больных – и оно было представлено на конгрессе под названием LITESPARK-011. В этом исследовании ленватиниб комбинировался с белзутифаном и сравнивался с кабозантинибом. В чем же суть? Ленватиниб и кабозантиниб – условно схожие ИТК 3 поколения. Белзутифан – препарат с принципиально новым механизмом воздействия на фактор, индуцирующий гипоксию, который показал эффективность в монотерапии. Его комбинация с ленватинибом логически оправданна.
В исследование включались больные с нерезектабельным или метастатическим ПКР, которые получили не менее 2 линий терапии и прогрессировали на предшествующей иммунотерапии. Рандомизация шла 1:1 в группы Б и Л в стандартных дозах (n=371) либо группу кабозантиниба (n=376). Первичные конечные точки – ВБП и ОВ. Пациенты имели в основном промежуточный и плохой прогноз, порядка 67-68% больных получили 1 предшествующую линию терапии.
В отношении первичной конечной точки – ВБП – комбинация достоверно превзошла кабозантиниб и снизила риск прогрессирования на 30%, это было отмечено на всех временных отрезках и также касалось и медианы ВБП.
Рисунок 4.
ВБП в группах

Подгрупповой анализ также продемонстрировал преимущества по всем параметрам, за исключением группы плохого прогноза – здесь отличий не было.
Данные по ОВ пока не зрелые, наблюдение за пациентами продолжается.
Рисунок 5.
ОВ в группах

Частота объективных ответов также показала преимущество комбинации: 52,6% на белзутифане с ленватинибом против 40,2% на кабозантинибе. Также отмечено преимущество комбинации в плане продолжительности ответа (рис.6), при этом токсичность в группах была схожей.
Рисунок 6.
Продолжительность ответа в группах

Качество жизни пациентов в группах было сопоставимым. С учетом всех данных авторы сделали вывод о клиническом преимуществе применения комбинации Б и Л у ранее предлеченных пациентов, и вероятнее всего, данная комбинация войдет в алгоритмы лечения и клинические рекомендации.
ТЕЗИСЫ КОНФЕРЕНЦИИ RUSSCO
ОСОБЕННОСТИ
ГИСТОЛОГИЧЕСКОЙ КАРТИНЫ И ИГХ-ПРОФИЛЕЙ МУЦИНОЗНОГО РАКА ШЕЙКИ МАТКИ, ОПИСАННЫЕ
В СЕРИИ СЛУЧАЕВ
Авторы: Т.А. Греян, А.Г. Кедрова, Ю.С. Константинова
Место работы: ФГБУ Федеральный научно-клинический центр специализированных
видов медицинской помощи и медицинских технологий ФМБА России
Эл.почта: greyantatev@gmail.com
Телефон: 89154514677
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель
Описать типичные морфологические признаки и иммуногистохимические (ИГХ) профили
муцинозного рака шейки матки (РШМ) на серии из 9 наблюдений, предложить
минимальную диагностическую панель для уверенной верификации относительного
редкого типа опухоли.
Материалы и
методы
Было проведено ретроспективное одноцентровое исследование (n = 9). Критериями
включения служили инвазивная аденокарцинома шейки матки с муцинозной
дифференцировкой, пересмотр гистопрепаратов двумя морфологами с верификацией по
ВОЗ 2020 (HPV‑associated vs HPV‑independent) и типизацией муцинозных вариантов
(intestinal‑type, iSMILE, signet‑ring predominant), стандартизованная оценка
инвазии по паттернам Силвы (A/B/C), наличию LVI, ассоциированных предраковых
изменений (AIS/HSIL) и краёв резекции, выполненное ВПЧ‑тестирование
(типоспецифическая ПЦР/ISHR). ИГХ панель включала p16, p53, PAX8, CK7, CK20,
MUC5AC, MUC2, MUC6, CDX2, p63/p40, Ki‑67, CEA. Пороговые значения
устанавливались следующим образом: p16 «block‑type» — диффузная ядерно‑цитоплазматическая
экспрессия ≥70% клеток; p53 — «дикого типа» vs аномальный паттерн; позитивность
для MUC/CDX2 — ≥10% клеток.
Результаты
Морфологические
варианты были представлены интестинальным типом (intestinal‑type) в 55,6%
случаев (5/9), для которого были характерны призматический эпителий с
апикальными «муциновыми шапками», очаги бокаловидных клеток, фокальная
CDX2/MUC2‑позитивность; iSMILE карциномой (invasive stratified mucin‑producing
carcinoma) в 33,3% случаев (3/9), в которой были описаны многоярусные слои
клеток со стратификацией и внутриклеточным муцином, отсутствие «истинных» желез
в части полей, очаговая p63/p40‑реактивность без формирования типичных
эластических «гнёзд»; а также один случай (11,1%; 1/9) с перстневидноклеточным
компонентом. Ассоциированные поражения шейки AIS и/или HSIL в прилежащей
слизистой были выявлены у 77,8% больных (7/9) и были сопряжены с
ВПЧ-позитивностью.
Паттерн инвазии по Силве распределялся равномерно: A — 3/9 (33,3%), B — 3/9 (33,3%), C — 3/9 (33,3%). LVI отмечалась в 33,3% случаев (3/9). ИГХ‑профиль характеризовался следующими особенностями: p16 — «block‑type» 9/9 (100%); p53 — «дикого типа» 9/9 (100%); PAX8 — 9/9 (100%); CK7 — 9/9 (100%); MUC5AC — 8/9 (88,9%); MUC6 — 0/9 (0%); MUC2 — 5/9 (все intestinal‑type); CDX2 очагово — 4/9; CK20 очагово — 3/9; p63/p40 — отрицательно или очагово слабо — 3/9 (при iSMILE); CEA положителен — 7/9. Ki‑67 был представлен высокими значениями во всех случаях, медиана составила ~50–70% (диффузно). ВПЧ (16/18/45) был выявлен в 8 из 9 случаев при выполнении молекулярного теста (88,9%).
Заключение
Типичными
«якорными» морфологическими признаками муцинозного РШМ в настоящей работе стали
апикальный муцин, бокаловидные клетки (intestinal‑type) и/или
стратифицированные муцинпродуцирующие пласты (iSMILE), частая связь с AIS/HSIL.
Минимальная ИГХ-панель для рутинной верификации муцинозного варианта РШМ должна
включать p16, p53, PAX8, CK7, MUC5AC, MUC6, CDX2±MUC2, p63/p40. Кроме того,
представляется критически важным обязательное тестирование ВПЧ, оценка паттерна
Силвы и LVI в морфологическом заключении.
Индукционная
стратегия при раке шейки матки: путь к хирургии или путь без преимущества?
Авторы: Троцик Е.В.
Место работы: ГБУЗ ММНКЦ им. С.П. Боткина ДЗМ.
Эл.почта: alena_t@myrambler.ru
Телефон: 89169114722
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель
Провести сравнительную оценку эффективности и безопасности комплексного
трёхэтапного подхода, включающего химиоэмболизацию (ХЭМА) для контроля рисков
кровотечения, индукционную химиотерапию на основе комбинации препаратов платины
и таксана и радикальное хирургическое лечение, в сопоставлении со стандартной
химиолучевой терапией у пациенток с местнораспространённым РШМ стадий IIB–IVA
Материалы и
методы
В ретроспективный анализ включены данные 30 пациенток, пролеченных в период с 01.2021
по 09.2022. Исследуемую группу (n=12) составили пациентки с верифицированным
плоскоклеточным РШМ (преимущественно ВПЧ-ассоциированным) стадий IIB–IVA в
возрасте до 60 лет, имевшие условно резектабельную опухоль с высоким риском
кровотечения или параметральной инфильтрацией. Лечебный алгоритм включал
химиоэмболизацию → 3–4 курса индукционной химиотерапии → радикальную
гистерэктомию с тазовой лимфаденэктомией. Группу сравнения (n=138) составили
пациентки, получившие стандартную ХЛТ.
Результаты
В исследуемой группе радикальное хирургическое лечение успешно выполнено у 10
из 12 пациенток (83,3%). Важно отметить, что на момент анализа все 10 пациенток
- без признаков рецидива заболевания. В послеоперационном материале у 6 из 10
пациенток (60%) был выявлен выраженный лечебный патоморфоз 3 степени, а у одной
из них зафиксирован полный патологический ответ. Несмотря на обнадеживающие
ранние результаты по локальному контролю и операбельности, сравнительный анализ
не выявил статистически значимых преимуществ комбинированной стратегии над
стандартом.
Заключение
Предложенный комплексный подход (ХЭМА → индукционная ХТ → радикальная операция) является технически выполнимым и позволяет достичь высокой частоты радикальных операций и значительного морфологического ответа у отдельных, тщательно отобранных пациенток с местнораспространенным РШМ. Однако на современном уровне доказательств он не продемонстрировал превосходства в показателях общей и безрецидивной выживаемости над стандартной химиолучевой терапией. В свете актуальных клинических рекомендаций и данных сравнительных исследований, данный подход не может рассматриваться в качестве рутинной альтернативы первой линии и требует дальнейшей оценки.
Комбинированная
мелкоклеточная нейроэндокринная р16-позитивная карцинома шейки матки:
особенности клинического течения и эффективность химиоиммунотерапии
Авторы: Стукань А.И., Ёлкин А.В., Антипова В.В., Бодня В.Н., Порханов В.А.,
Хорева Д.В.
Место работы: ФГБОУ ВО КубГМУ, г. Краснодар; ГБУЗ НИИ - ККБ1; Федеральная сеть
клиник экспертной онкологии Евроонко
Эл.почта: jolie86@bk.ru
Телефон: 79654668086
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель.
Продемонстрировать
особенности клиники и эффективность химиоиммунотерапии при мелкоклеточной
нейроэндокринной карциноме (МНЭК) шейки матки
Материалы и методы. Клинический случай МНЭК шейки матки р16 с
паранеопластическим синдромом – смешанное заболевание соединительной ткани
Результаты. У пациентки 42 лет в ноябре 2024 обнаружено новообразование шейки матки. По гистологии (г. Краснодар) – HPV плоскоклеточная карцинома. Сопутствующий диагноз: смешанное заболевание соединительной ткани с проявлениями ревматоидного артрита и иммунологическими элементами системной красной волчанки. С января 2025 проведено ХЛТ на фоне цисплатина. При контрольном осмотре МР-картина полного ответа Bl шейки матки TRG1. По МРТ от 24.10.2025: возникшее новообразование влагалища. В НМИЦ имени А.Ф. Цыба - трепан-биопсия новообразования влагалища. ПГИ ИГХ: Комбинированная МНЭК шейки матки р16-позитивная/смешанная МНЭК и эндоцервикальная аденокарцинома р16, Ki 67-90%. Пересмотр первичной опухоли: комбинированная МНЭК шейки матки р16-позитивная/смешанная МНЭК и эндоцервикальная аденокарцинома р16. В декабре по ПЭТ-КТ с 18-ФДГ- мтс в области корня левого легкого с повышенной фиксацией ФДГ; мтс в ВГЛУ неопластического генеза; очаговых образований легких неопластического генеза; мтс в области преддверия влагалища неопластического генеза с гиперфиксацией ФДГ. В краснодарском филиале клиники Евроонко при осмотре: на входе во влагалище - округлое образование до 3 см плотноэластическое, несмещаемое, болезненное при пальпации. С учетом актуальных рекомендаций (NCCN) в качестве 1 линии инициирована схема химиоиммунотерапии (ХИТ): карбоплатин AUC 5 в/в в 1-й день и этопозид 100 мг/м2 в/в в 1, 2, 3-й дни атезолизумаб 1200 мг в 1-й день. После первого курса отмечается улучшение самочувствия, уменьшение образования и болевых ощущений в области влагалища, отсутствие скованности и болезненности суставов как проявления заболевания соединительной ткани. Ревматологическое заболевание расценено как паранеопластический синдром с отменой терапии. После 2 курса ХИТ выполнено ПЭТ-КТ: частичный ответ мтс-очагов со снижением фиксации ФДГ, полный метаболический ответа мтс во влагалище. Запланировано проведение профилактического облучения головного мозга, продолжение курсов ХИТ с последующей поддерживающей анти-PD-L1 терапией.
Заключение. МНЭК шейки матки является редкой патологией, установление диагноза может быть сложной проблемой с необходимостью консультации в специализированном центе. Клиника характеризуется ранними рецидивами и отдаленным метастазированием. Оптимальным методом первичной терапии является мультимодальный подход с включением хирургии. Терапия метастатического заболевания может включать химиоиммунотерапию по аналогии с мелкоклеточным раком легкого. Также следует рассмотреть профилактическое облучение головного мозга.
Первый опыт
выполнения органосохраняющих операции у пациенток с инвазивным раком шейки
матки IAI стадии в объеме ампутации шейки матки с биопсией сигнальных
лимфатических узлов методом ICG- флуоресценции лапароскопическим доступом.
Авторы:
Е.А Леванова , С.А Суркова
Место работы: Клинический онкологический центр г. Саратов
Эл.почта: elena.levanova@bk.ru
Телефон: 89271006466
Являюсь членом Комитета молодых онкологов RUSSCO: нет
Цель
Оценить результаты выполнения органосохраняющих операций у пациенток с
инвазивным раком шейки матки начальной стадии с определением сигнальных.
Материалы и
методы
Проанализированы
первые результаты органосохраняющих операций у пациенток с раком шейки матки
IАI стадии в объеме ампутации шейки матки с выполнением биопсии сигнальных
лимфатических узлов методом ICG- флуоресценции лапароскопическим доступом.
Первый опыт выполнения операций в вышеуказанном объеме связан открытием в
апреле 2025 года нового Клинического онкологического центра г. Саратова и с внедрением
в использование видеокамеры высокого разрешения с функцией инфракрасного
свечения с детекцией СЛУ ф луоресцентным методом с ICG.
Результаты
В
период с апреля 2025 по декабрь 2025 года выполнено 8 органосохраняющих
операций в объеме ампутации шейки матки с БСЛУ методом ICG – флуоресценции
лапароскопическим доступом у пациенток с верифицированным раком шейки матки IAI
стадии. У 7 из 8 при выполнении первичной конизации шейки матки морфологически
диагностирована лимфоваскулярная инвазия, что являлось показанием к выполнению
БСЛУ. У всех 8 пациенток морфологически отсутствовали метастазы в сигнальных
лимфатических узлах. У 1 пациентки после выполнения ампутации с БСЛУ объем
оперативного лечения был расширен до расширенной экстирпации матки с маточными
трубами ввиду наличия значимой сосудистой инвазии и наличия фокуса
плоскоклеточного неороговевающего рака G3 в крае резекции. Следует отметить,
что из 8 пациенток именно у этой пациентки отмечалась значимая лимфоваскулярная
инвазия при выполнении первичной конизации.
Заключение
Пациенткам с верифицированным инвазивным раком шейки матки IAI стадии, заинтересованным в сохранении репродуктивной функции, рекомендовано выполнение органосохраняющих операций в объеме ампутации шейки матки с биопсией сигнальных лимфатических узлов методом ICG- флуоресценции лапароскопически. Идентификация сигнальных лимфатических узлов с гистологическим исследованием позволяет точно оценить статус регионарных лимфатических узлов и значительно снизить осложнения, которые возможны при выполнении тазовой лимфаденэктомии. Наличие значимой лимфоваскулярной инвазии при выполнении первичной конизации шейки матки и верификации диагноза является плохим прогностическим фактором при планировании тактики и выборе объема оперативного лечения.
Гетерогенность
рецидивов рака шейки матки: от ангиогенеза и молекулярного профиля к
персонализированной терапии
Авторы: Шумейкина А.О., Красильников С.Э.
Место работы: ФГБУ "НМИЦ им.ак. Е.Н. Мешалкина", ФИЦ ФТМ,
Новосибирский Государственный Университет
Эл.почта: nashum99@mail.ru
Телефон: 79994640163
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель. Оптимизировать тактику ведения пациенток с рецидивами рака шейки матки на основе комплексной оценки клинических, морфологических и молекулярно-генетических предикторов течения заболевания.
Материалы и методы. В исследование включены ретроспективная и проспективная группы пациенток с РШМ. Ретроспективно проанализированы отдалённые результаты лечения 100 пациенток с рецидивами РШМ с выявлением предикторов различных типов рецидивов и летальности. В проспективное исследование включены 294 пациентки (157 - первичный РШМ без рецидива, 137 - рецидивный РШМ). Выполнены морфологическое и морфометрическое исследование ангиогенеза (CD34), иммуногистохимическая оценка PD-L1, HER2, MSI, p16, Ki-67 и анализ экспрессии интегринов α3, α5, β1. Проанализированы отдаленные результаты лечения (общая выживаемость, одногодичная летальность, пятилетняя выживаемость). Для диагностики ранних рецидивов (FIGO 0–IA1), локализованных в цервикальном канале, разработан нами эндоцервикальный резектор и метод эндоцервикальной резекции. Использованы одно- и многофакторные статистические модели.
Результаты. Выявлены
клинико-морфологические предикторы различных типов рецидивов и летальности,
подтверждающие гетерогенность механизмов рецидивирования РШМ.
Установлено, что ангиогенез при рецидивном РШМ носит индивидуальный и
нелинейный характер: у одной и той же пациентки в рецидиве возможно как
увеличение, так и снижение сосудистой плотности по сравнению с первичной
опухолью. Показано, что молекулярно-генетический профиль рецидивного РШМ
характеризуется выраженной гетерогенностью экспрессии PD-L1, HER2, MSI, p16,
Ki-67 и интегринов α3, α5, β1, отражающей биологическое разнообразие рецидивных
опухолей и ассоциацию с клиническим вариантом рецидивирования.
Применение эндоцервикального резектора позволяет проводить раннюю диагностику
рецидивов РШМ ранних стадий (FIGO 0–IA1) и обоснованно выбирать
органосохраняющий либо радикальный объём хирургического лечения. На основе
совокупной оценки клинических, морфологических, молекулярных характеристик
разработан алгоритм лечебно-диагностического ведения пациенток с рецидивами
РШМ.
Заключение. Рецидивный рак шейки матки является биологически гетерогенным заболеванием, при котором тип рецидива, прогноз и ответ на терапию определяются сочетанием клинико-морфологических, ангиогенных и молекулярно-генетических факторов. Полученные данные обосновывают персонализированный подход к ведению пациенток с рецидивами РШМ, включая выбор хирургической тактики и направлений системной, в том числе антиангиогенной таргетной терапии.
Иммунотерапия
рака шейки матки – опыт клиники им. А.С. Логинова
Авторы: Давыдова Ирина Юрьевна, Валиев Рамиз Камраддинович, Гордиенко Ксения
Анатольевна
Место работы: МКНЦ им. А.С. Логинова
Эл.почта: davydova06@mail.ru
Телефон: 89031990746
Являюсь членом Комитета молодых онкологов RUSSCO: нет
Цель
Оценить эффективность иммунотерапии у больных с прогрессированием рака шейки
матки с позитивным иммунным статусом опухоли (PD-L1, MSI)
Материалы и
методы
В
МКНЦ им. А.С. Логинова проанализированы результаты лечения 8 больных с
прогрессированием рака шейки матки с позитивным иммунным статусом опухоли
(PD-L1, MSI). Период наблюдения достигает 6 лет.
Результаты
Лечение распространенного рака шейки матки и прогрессирования рака шейки матки
по-прежнему является крайне трудной и зачастую неразрешимой задачей. По данным
исследования GOG 240 добавление бевацизумаба к химиотерапии привело к
увеличению общей выживаемости с 13,3 до 17 мес., а добавление пембролизумаба к
стандартной терапии первой линии у больных с PD-L1-позитивной опухолью
увеличило ОВ с 16,5 мес. до 28,6 (исследование KEYNOTE-826).
В МКНЦ им. Логинова иммунотерапия проводится в зависимости от статуса PD-L1 и
MSI у больных с распространенным РШМ и прогрессированием РШМ.
В данном сообщении мы представляем 8 случаев иммунотерапии при прогрессировании
рака шейки матки. Во всех наблюдениях гистологическая форма была представлена
плоскоклеточным раком. Первоначальные стадии заболевания были в диапазоне от IB
до IIIА. У 5 больных с поражением тазовых л/у, у 1 пациентки - парааортальных л/у,
у 2 больных мтс в л/у по данным КТ не наблюдалось. Прогрессирование заболевания
отмечено в сроки от 4 месяцев до 3 лет. У 3 пациенток определялась первичная
неизлеченность (продолженный рост) после химиолучевого лечения. У 5 больных –
отдаленные метастазы в легкое, регионарные и отдаленные лимфоузлы. В силу того,
что представленные наблюдения касаются настоящего времени, у 4 больных
иммунотерапия начата недавно и оценка эффекта преждевременна. У пациентки с
PD-L1 CPS 90 отмечается выраженная эффективность, связанная с резорбцией
метастатических очагов по брюшине малого таза и метастатически измененных
лимфоузлов. Срок наблюдения 2 года.
Наиболее длительный эффект отмечен у больной с метастазами РШМ в легкое и
лимфоузлы таза, в опухоли выявлена микросателлитная нестабильность. Эффект
продолжается более 6 лет и прогрессирования заболевания в настоящее время не
наблюдается.
Заключение
Иммунотерапия
у больных с прогрессированием рака шейки матки с позитивным иммунным статусом
опухоли (PD-L1, MSI) в ряде случаев позволяет достичь выраженной эффективности
и добиться увеличения продолжительности жизни на годы.
Влияние
лучевой терапии рака шейки матки и медицинской реабилитации на качество жизни
пациенток
Авторы: Созаева Л.Г., Евстигнеева И.С., Козырева В.О.
Место работы: ФГБОУ ДПО РМАНПО Минздрава России, г. Москва
Эл.почта: kvo03@yandex.ru
Телефон: 79156395216
Являюсь членом Комитета молодых онкологов RUSSCO: нет
Актуальность:
Лучевая
терапия (ЛТ) злокачественных новообразований женской половой системы
эффективна, но сопровождается побочными реакциями. Ранние: общая лучевая
реакция, лучевой цистит, ректит, катаральный эпителиит влагалища. Поздние:
лимфедемы нижних конечностей, стриктуры мочевыделительной и ЖКТ систем, стеноз
влагалища, вульводиния, диспареуния. Это ухудшает психическое состояние и
качество жизни пациенток, требуя междисциплинарного подхода.
Цель: оценить качество жизни пациенток на этапе лучевой терапии ЗНО женской
половой системы.
Материалы и
методы
Участие приняли 30 пациенток (основная группа n=15; группа сравнения n=15) на
этапе ЛТ рака шейки матки согласно действующим КР МЗ РФ. В ходе основного
лечения пациенткам основной группы (n=15) проводился курс из 10 процедур
локальной магнитотерапии, ЛФК и психологической поддержки. Оценка качества
жизни осуществлялась посредством анализа жалоб, интенсивности боли (ВАШ),
анкеты SF-36.
Результаты
К концу курса ЛТ у всех пациенток отмечены жалобы на болевой синдром, дизурию,
дисфункцию кишечника (диарея, тенезмы), диспепсию, общую слабость, нарушения
сна, тревожность, плаксивость, апатию. Интенсивность боли (ВАШ): основная
группа: до ЛТ — 1,5 [1,0–2,0]; конец ЛТ — 3,5 [2,5–4,0]; через 3 мес — 1,8
[1,0–2,5]; группа сравнения: до ЛТ — 1,4 [1,0–2,0]; конец ЛТ — 4,5 [3,5–5,0];
через 3 мес — 3,0 [2,5–3,5] (p<0,05 между группами на конец ЛТ; p<0,05
между группами на 3 мес). Жалобы через 3 месяца: тенезмы: основная — 40% (n=6),
сравнение — 73,3% (n=11); дизурия: основная — 20% (n=3), сравнение — 60% (n=9);
нарушения трофики кожных покровов: основная — 46,67% (n=7), сравнение — 66,67%
(n=10); слабость: основная — 40% (n=6), сравнение — 60% (n=9) (p<0,05).
SF-36 к концу ЛТ: «Интенсивность боли»: обе группы ухудшение (p<0,001), но основная группа — менее выраженное (p=0,03); «Ролевое эмоциональное функционирование»: основная — стабильное; сравнение — ухудшение (p<0,001); «Физическое функционирование», «Жизненная активность»: стабильны в обеих группах. «Социальное функционирование», «Психологическое здоровье»: улучшение в основной группе (p<0,001).
Заключение
Проведение
лучевой терапии рака шейки матки ассоциируется с выраженным болевым синдромом,
снижением показателей качества жизни и формированием комплекса жалоб,
сохраняющихся в отдалённые сроки наблюдения, что подчёркивает необходимость
мультидисциплинарного подхода с включением программ медицинской реабилитации
как на этапе проведения ЛТ, так и в последующие периоды восстановления.
АНАЛИЗ
ЭФФЕКТИВНОСТИ ПРОГРАММЫ СКРИНИНГА РАКА ШЕЙКИ МАТКИ В КРАСНОЯРСКОМ КРАЕ
Авторы: Иванова Е.Е., Комиссарова В.А., Сафонцев И.П., Зуков Р.А.
Место работы: ФГБОУ ВО КрасГМУ им. проф. В.Ф.Войно-Ясенецкого Минздрава России,
КГБУЗ «КККОД им. А.И. Крыжановского»
Эл.почта: elena.ivanova01@bk.ru
Телефон: 89135668195
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель
Оценка
эффективности реализации региональной программы скрининга рака шейки матки
(РШМ) в Красноярском крае за период 2021-2025 гг.
Материалы и
методы
Материалом для исследования послужила форма отраслевой статистической
отчетности N 131/о "Сведения о проведении профилактического медицинского
осмотра и диспансеризации определенных групп взрослого населения" за
2021-2025 гг. по ключевым показателям: число исследований, охват целевой
популяции, выявление случаев РШМ в рамках профилактических медицинских осмотров
(ПМО) и диспансеризации определенных групп взрослого населения (ДОГВН).
Методология включала применение методов сравнительного и структурного анализа.
Результаты
Установлен
значительный рост объема цитологических исследований на 246,3% (с 82 256 в 2021
г. до 284 833 в 2025 г.) и охвата целевой группы женщин 18-69 лет с 14,2% в
2021 г. до 45,3% в 2025г. Стабильный рост суммарного охвата целевой популяции
сопровождается волнообразной динамикой выявления новых случаев. Это указывает
на то, что достигнут он преимущественно за счет многократного обследования
одного и того же контингента женщин, что не соответствует подходу ежегодной
сменяемости контингента. Так же при анализе проведения ПМО и ДОГВН для
прикреплённого населения в медицинские организации края выявлены системные
проблемы, влияющие на эффективность скрининга: использование несоответствующих
цервикальных щеток для забора материала, нарушение технологии фиксации и
окрашивания мазка, отсутствие преемственности между специалистами смотрового
кабинета, отделения профилактики и акушерско-гинекологической службы в части
отслеживания пути пациента с патологическим мазком.
Заключение
Региональная
программа скрининга РШМ в Красноярском крае демонстрирует высокое выполнение
объемных показателей при низкой эффективности в достижении главной цели –
активного выявления новых случаев злокачественных новообразований на ранних
стадиях. Для повышения эффективности необходим системный подход, включающий
переход от учета числа мазков к контролю охвата уникальных женщин за три года.
Разработка и внедрение единого стандарта работы смотрового кабинета как первого
этапа ранней диагностики; формирование подходов стимулирования медицинских
работников за выявление предраковых заболеваний и ранних стадий на этапе
смотрового кабинета.
Эффективность
иммунотерапии Пембролизумабом во 2 линии лекарственного лечения пациенток с
рефрактерным течением рака шейки матки
Авторы: Гилева М.С.
Место работы: НМИЦ онкологии им. Н.Н. Блохина
Эл.почта: gileva.rita@gmail.com
Телефон: 89137620520
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель
Оценить
результаты лечения пациенток с рефрактерным течением местно-распространенного и
метастатического рака шейки матки с рефрактерным течением, получавших
иммунотерапию Пембролизумабом во 2 линии лекарственного лечения.
Материалы и
методы
В ретроспективное нерандомизированное многоцентровое исследование были включены
пациентки с рефрактерным течением РШМ. Рефрактерное течение онкологического
процесса определяется рентгенологически подтвержденным прогрессированием на
фоне химиотерапии 1-й линии или в течение 3 месяцев после его завершения.
Пациентки, включенные в эту группу, имели позитивную экспрессию PD-L1 в опухоли
и получали иммунотерапию Пембролизумабом во 2-й линии лечения. Была оценена
общая выживаемость в этой когорте больных.
Результаты
В
исследование было включено 18 пациенток с рефрактерным течением рака шейки
матки. Все 18 пациенток в качестве 1 линии лекарственного лечения получили
химиотерапию по схеме: паклитаксел + карбоплатин, а далее во всех случаях было
отмечено рентгенологическое прогрессирование опухолевого процесса в течение 3
месяцев после последнего курса химиотерапии. Все пациентки, включенные в
исследование, имели CPS>1 в опухолевом материале и получили в
моноиммунотерапию пембролизумабом во 2 линии лекарственного лечения. Медиана
общей выживаемости составила 14 месяцев.
Заключение
В исследовании KEYNOTE 158, изучавшем применение Пембролизумаба у больных
метастатическим раком шейки матки после одной или более линий химиотерапии,
имеющих PD-L позитивные опухоли, ОВ составила 11 месяцев. Однако в этой работе
было рассмотрено применение Пембролизумаба не только во 2 линии лекарственного
лечения, но и в последующих.
В нашей работе, в которую было включено 18 пациенток с рефрактерным течением
PD-L-позитивного рака шейки матки, медиана общей выживаемости составила 14
месяцев. Дальнейший набор пациенток в эту исследуемую когорту позволит лучше
оценить клинический прогноз и выживаемость пациенток, не ответивших на
стандартную химиотерапию 1 линии.
Рак шейки матки во время беременности: перинатальные исходы, опыт ФГБУ НМИЦ им.В.А.Алмазова
Авторы: Ульрих Е.А., Калинина Е.А., Чекина Ю.А., Осипова Н.А., Первунина Т.М.,
Ли О.А., Зазерская И.Е., Загородникова К.А., Дикарева Е.Л., Комличенко Э.В.,
Зорина Е.Ю., Копылов В.В.
Место работы: ФГБУ «НМИЦ им. В.А. Алмазова»
Эл.почта: elenaulrikh@mail.ru
Телефон: 79217400618
Являюсь членом Комитета молодых онкологов RUSSCO: нет
Цель
Оценить воздействие злокачественных опухолей шейки матки, выявленных во время
беременности, на исходы для детей, рожденных данной когортой пациенток.
Материалы и
методы
Проанализировано состояние десяти новорожденных, матерям которых рак шейки
матки диагностирован на фоне беременности (2021-2024гг, ФГБУ НМИЦ им В.А.
Алмазова).
Результаты
У
7 пациенток опухоль шейки матки выявлена во II триместре (14/15 – 27/28
недель), у 2 пациенток - в III триместре (30 и 37 недель) и только в одном
случае – в I триместре (7/8 недель) беременности. Распределение по стадиям
опухолевого процесса: IB стадии были у 5 пациенток, IIB стадии – у 5 пациенток.
Пятерым пациенткам начато лечение во время беременности: четырем - только
лекарственное лечение от 2 до 4 циклов по схеме ТСb (карбоплатин паклитаксел),
еще одной пациентке было проведено комбинированное лечение (ампутация шейки
матки, лимфаденэкт омия химиотерапия). В остальных пяти случаях лечение начато
сразу после родоразрешения. В трех случаях опухоли были выявлены в доношенном
сроке, в четвертом случае в связи с критическим нарушением кровотоков плода
(НППК) пациентка родоразрешена в недоношенном сроке гестации. В пятом случае
сразу после установления диагноза (29 недель) пациентка была родоразрешена в
связи с наличием мукоэпидермоидного рака шейки матки и невозможностью лечения
во время беременности.
Из 10 родов 4 произошли преждевременно. Из этих 4 пациенток 2 получали
химотерапию: в одном случае пациентка была родоразрешена в 36 недель в связи с
прогрессированием опухоли, во втором – пациентке было проведено кесарево
сечение в 27 недель по показаниям со стороны плода (ангидрамнион, НППК).
В результате
проанализированных беременностей родилось 10 живых детей. Семь новорожденных
родились с высокими оценками по шкале Апгар (7/8, 8/9 баллов). В 2 случаях 6/7
баллов было у детей, родившихся при сроке 29 недель и 1/3 баллов - девочка,
родившаяся в 27 недель.
Шесть детей соответствовали своему гестационному сроку. Один из детей был
маловесным, трое имели задержку внутриутробного развития плода по типу
гипостатуры. Средний вес детей от матерей, получавших химиотерапию, составил
2508±1067г и варьировал от 790 г до 3590 г. В группе детей, чьи матери не получали
химиотерапию во время беременности, данный показатель составил 1882±848 г и
варьировал от 940 г до 2800 г.
Девять детей были выписаны домой в удовлетворительном состоянии. Одна
новорожденная (родившаяся в 27 недель) умерла на 9 сутки в результате осложнений,
возникших в результате глубокой недоношенности.
Заключение
Перинатальные
исходы у пациенток со злокачественными опухолями шейки матки, выявленными во
время беременности, зависят от срока выявления новообразования,
морфологического типа, стадии опухоли. Лечение рака является относительно
безопасным для плода, абсолютно необходимым для лучшего прогноза для матери,
однако не всегда возможно. Большинство осложнений новорожденных связано с
ранним родоразрешением и недоношенностью.
Использование мультипараметрической МРТ для ранней диагностики эндоцервикальной аденокарциномы шейки матки
Авторы: Придорогина Е.В. Антонова И.Б.Аксенова С.П. Нуднов Н.В
Место работы: ФГБУ «РНЦРР» Минздрава России
Эл.почта: pridorogina_katerina@mail.ru
Телефон: 79131310994
Являюсь членом Комитета молодых онкологов RUSSCO: да
Цель
Повысить точность ранней диагностики и клинического стадирования
эндоцервикальной аденокарциномы шейки матки (АКШМ) эндометриоидного типа с
учетом особенностей визуализации при проведении мультипараметрической
магнитно-резонансной томографии (мпМРТ).
Материалы и
методы:
Объект исследования: пациентки с впервые выявленной и гистологически
верифицированной эндоцервикальной аденокарциномой шейки матки эндометриоидного
гистотипа
Группы сравнения:
• Пациентки с плоскоклеточным раком шейки матки Ib1-3 ст;
• Пациентки с эндометриоидной аденокарциномой тела матки с переходом на
перешеек, II ст
Проведена
мультипараметрическая МРТ малого таза по единому протоколу согласно требованиям
ESUR (European Society of Urogenital Radiology):
a. Высокоразрешающие T2-TSE в трех плоскостях;
b. Диффузионно-взвешенная визуализация (DWI) с расчетом карт ADC (b=0, 800-1000
с/мм²);
c. Динамическое контрастное усиление (DCE-MRI) с болюсным введением
гадолиниевого контраста и построением кривых «сигнал-время» и параметрических
карт.
Результаты
При проведении мультипараметрической МРТ при АКШМ эндометриоидного гистотипа
отмечен локально инвазивный характер роста очагов отсева в эндометрии и в
перешейке, и в средней трети эндоцервикального канала, с формированием
«питающей ножки» и визуализацией питающих сосудов (41%). Отмеченный
неоангиогенез в опухоли, при котором она получает питание от аркуатных и
крупных интрамуральных сосудов миометрия, визуализируемых методом МРТ, как мы
полагаем, говорит об агрессивном характере роста опухоли, высокой вероятности лимфоваскулярной
инвазии, повышению вероятности метастазирования в лимфатические узлы и
неблагоприятном прогнозе.
Способность АКШМ давать отсевы в эндометрий отмечена рядом исследователей, которые объясняют это теорией «seed and soil» (теория «семени и почвы») — отсоединением части раковых клеток от первичного очага опухоли, их миграцией в полость матки и имплантацией в эндометрий. Факт имплантации клеток с развитием впоследствии питающих сосудов и преобладанием роста очага отсева в матке, как мы полагаем, может быть объяснён лучшим кровоснабжением миометрия в сравнении с шейкой матки, где в строме преобладает фиброзная ткань. Использование диффузионно-взвешенных изображений и анализ ИКД-карт повышают эффективность метода по сравнению со стандартными режимами МРТ. В исследовании F. Kuang и соавт. показано, что значения коэффициента ИКД являются надёжным маркёром для дифференциации РШМ от нормальной шейки матки с высокой диагностической точностью (значения ИКД при РШМ были значительно ниже, чем у нормальной шейки матки: 0,81±0,13×10-3 мм2 /сек против 1,41±0,10×10-3 мм2/сек). Значения ИКД также могут быть использованы для указания степени дифференцировки и гистологического типа РШМ, хотя существует некоторое перекрытие значений.
В нашем исследовании средний показатель ИКД в опухоли при измерении в выбранном участке (region of interest, ROI) составил 0,833×10-3 мм2 /сек (min 440×10-3 мм2 /сек, max 1282×10-3 мм2/сек), что в целом совпадает с данными литературы. Изучением семиотических различий между АКШМ и плоскоклеточной карциномой шейки матки занимались исследователи Е.В. Тарачкова и соавт. У 90 пациенток с гистологически верифицированным РШМ выявлено, что для аденокарциномы по сравнению с плоскоклеточным раком характерны более высокая интенсивность и меньшая неоднородность сигнала на Т2-ВИ с подавлением сигнала от жировой ткани. Ключевым моментом в дифференциальной диагностике аденокарциномы матки по данным МРТ являлась установка локализации первичной опухоли.
Так, эндоцервикальная аденокарцинома матки с поражением эндометрия и аденокарцинома эндометрия с распространением на шейку матки по сигнальным характеристикам в большинстве случаев неотличимы друг от друга. И, как показало данное исследование, однозначно не стоит полагаться только на анализ локализации большего объёма опухоли. В нашем исследовании лишь в 65% (13 из 20) случаев гистологически подтверждённая эндоцервикальная АКШМ локализовалась исключительно в шейке матки. В 35% случаев (7 из 20) опухоль имитировала рак эндометрия, при этом опухолевые массы определялись как в полости матки, так и по ходу цервикального канала. А в случаях с очагами отсева эндоцервикальной аденокарциномы в эндометрий (3 из 20, 15%) у 2 пациенток размеры опухолевого импланта в эндометрии превышали размеры первичной опухоли шейки матки.
Заключение
В связи с инфильтративным ростом опухоли и частым её расположением в верхних
отделах цервикального канала и области слизистой перешейка матки,
эндоцервикальная АКШМ диагностируется на поздних стадиях. В равной степени это
связано и с трудностями забора адекватного цитологического материала при
ПАП-тесте и отсутствием визуализации изменений шейки матки при гинекологическом
осмотре, что не позволяет своевременно выявить наличие опухоли. Поздняя
диагностика эндоцервикальной АКШМ приводит к выявлению уже
местнораспространённого процесса с частым прямым или метастатическим поражением
эндометрия, которые имитирует первичный рак эндометрия.
Настоящее исследование показало, что МРТ является "золотым стандартом" визуализации с высокими показателями диагностической информативности метода в выявлении опухолевой патологии матки. Выделенные в ходе анализа данных МРТ 4 типа макроструктуры опухолевого роста АКШМ указывают на местноагрессивный рост опухоли и высокую частоту отсевов в эндометрий. Имеющиеся ограничения в выявлении малых опухолей АКШМ методом МРТ связаны с преимущественно инфильтративным и стелющимся характером ростом опухоли, без увеличения размеров матки и изменения сигнальных характеристик эндоцервикса. В то же время неоднородное расширение и гиперплазия цервикального канала по данным МРТ позволяют заподозрить опухолевую патологию и своевременно направить женщину к онкогинекологу.
Лекарственная терапия в лечение местно-распространенного рака шейки матки с N-позитивным статусом: небольшой опыт одного центра.
Дудина И.А.1, Рахманова П.А. 1, Нестерова Н.А. 1, Волконский М.В. 1, Куликова С.Е. 1, Строяковский Д.Л. 1
1ГБУЗ "Московская городская онкологическая больница №62 Департамента здравоохранения города Москвы", Москва
Цель: оценить эффективность лекарственной терапии (карбоплатин + паклитаксел + пембролизумаб +/- бевацизумаб) у пациенток с CPS-позитивным местно-распространенным раком шейки матки (РШМ) IIIC1, IIIC2 и IVA стадий по FIGO 2018.
Материалы и методы:
Для представления данных применялись методы описательной статистики. Для оценки ВБП и ОВ использовался метод Каплана-Мейера. Статистическая обработка результатов проведена при помощи программы Jamovi 2.6.44.
Результаты: в ретроспективный анализ включено 11 пациенток, проходивших лечение в ГБУЗ «МГОБ №62» ДЗМ, характеристики представлены в таблице 1. Медиана наблюдения – 16.9 мес. Частота объективного ответа по RECIST 1.1 составила 100%: 1 – полный ответ, 10 – частичный. Все пациенты получали химиотерапию по схеме карбоплатин + паклитаксел (допускалось как трехнедельное, так и еженедельное введение химиопрепаратов). Медиана числа курсов химиотерапии – 5 (от 2 до 6). Из 11 пациенток 9 получили локальное лечение после курсов лекарственной терапии: 4 – хирургическое лечение, 4 – ДЛТ + брахитерапия, 1 – только брахитерапия. У 2 из 4 пациенток диагностирован полный патоморфологический ответ при послеоперационном гистологическом исследовании, у 2 – выраженный неполный патоморфологический регресс (ypT1b1N0 у обеих). Причинами отсутствия локального лечения у 2 пациенток стали: отказ от ДЛТ в связи с распространенной IVА стадией и выраженного частичного ответа, аутоиммунные осложнения (пульмонит 2 ст.) и следующее за ним прогрессирование. Прогрессирование заболевания выявлено у 4 из 11 пациенток (1 – VIA ст. на момент установки диагноза, 3 – IIIC2 ст.). 1-летняя ВБП (время от гистологического подтверждения диагноза до прогрессирования и\или смерти) составила 81,8%. По характеру прогрессирования у 2 пациенток наблюдался продолженный рост первичной опухоли и патологических лимфоузлов, у 2 пациенток – системное прогрессирование. Смерть по причине прогрессирования произошла у 2 из 11 пациенток: 1-летняя ОВ составила также 81,8%. Тенденции к лучшему ответу при более высоком CPS (60 и выше) в данной группе не наблюдалось.
Заключение: Химио-иммуно-таргетная терапия имеет высокую эффективность в лечении местно-распространенного РШМ, при этом адекватное локальное лечение также обязательно. Каждой 3 пациентке (4/11) в данной когорте с N+ РШМ проведено хирургическое лечение без необходимости в последующей лучевой терапии. Данный подход требует дальнейшего изучения, проведения рандомизированного проспективного исследования.
Таблица 1.
Характеристики пациентов.
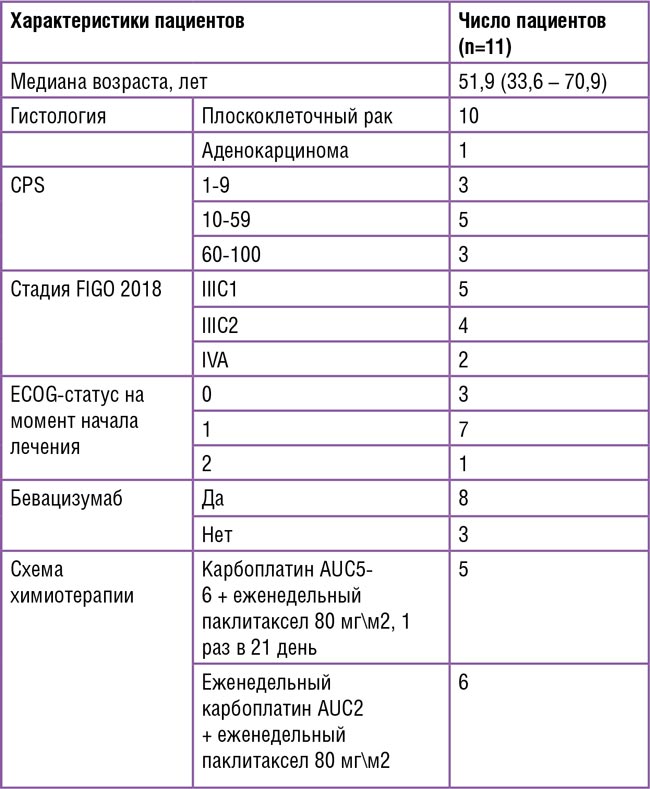
Скрининг ВИЧ-инфицированных женщин: возможности профилактики запущенных случаев рака шейки матки
1Зиновьев С.В., 1Локоткова М.И., 3Мкртчян Л.С., 1Сметанина С.В., 1Колесникова Е.А., 2Уткин О.В., 1Гурьянова А.В, 1Белоглазова Н.А. 1Гамаюнов С.В., 1Поташова Л.А.,
1Государственное автономное учреждение здравоохранения Нижегородской области научно-исследовательский институт клинической онкологии «Нижегородский областной клинический онкологический диспансер»,. г. Нижний Новгород
2ФБУН ННИИЭМ им. ак. И.Н. Блохиной Роспотребнадзора, г. Нижний Новгород
3Медицинский радиологический научный центр им. А.Ф. Цыба - филиал ФГБУ «НМИЦ радиологии» Минздрава России, г. Обнинск
Актуальность. Рак шейки матки (РШМ) продолжает занимать первое место в мире среди злокачественных новообразований (ЗНО) женских половых органов с неуклонной тенденцией к росту у женщин молодого возраста. Совершенствование методов скрининга и внедрение программ вакцинации в развитых странах позволяют значительно улучшить показатели выявляемости начальных стадий заболевания. В настоящее время >85% случаев смерти от РШМ приходится на страны со средним и низким уровнем дохода, где ЗНО данной локализации являются основной причиной смертности от рака среди женщин. Использование математического моделирования показало, что широкий охват населения программами скрининга РШМ и вакцинации против ВПЧ, начиная с 2020 года, может предотвратить 12,5–13,4 миллиона новых случаев заболевания к 2070 году и достичь почти полной ликвидации в большинстве стран к концу столетия. В настоящее время разработаны новые технологии, позволяющие проводить более быстрый, экономически эффективный и чувствительный скрининг РШМ, однако остается контингент пациентов, у которых, даже при соблюдении сроков скрининговых мероприятий, со временем выявляются запущенные формы заболевания.
Цель работы: оценить провести скрининг рака шейки матки целевой группы ВИЧ-инфицированных, курильщиков.
Материалы и методы. Целевую группу составили 130 женщин с положительным ВИЧ-статусом, содержащихся в исправительной колонии. Скрининговые мероприятия реализованы у 90 женщин (40 - отказалась от прохождения скрининга). Средний возраст женщин составил 37,5 лет, до 30 лет – 15 (16,6%), до 45 лет – 50 (55,5%). Сочетание ВИЧ-инфекции и гепатита С отмечено в 64 (71,2%) случаях. О вредных привычках (курение табака) сообщили 84 (93,3%) женщины. В анамнезе эрозия шейки матки диагностирована у 32 (32,2%) женщин. Скрининг предполагал ко-тестирование: взятие соскоба с поверхности шейки матки и соскоба из цервикального канала на цитологическое исследование, а также соскоба из цервикального канала для ПЦР-анализа на вирус папилломы человека (ВПЧ), а при его выявлении – генотипирование онкогенных и неонкогенных типов.
Результаты. ВПЧ-инфекция выявлена у 74 (82,2%) женщин, из них в 41 (45,5%) случаях - ВПЧ 16/18 типа. Множественная ВПЧ-инфекция (наличие 2-х и более генотипов) зарегистрирована у 63 (70 %) женщин, причем одновременно 3 и более генотипов - у 25 (28,3%), шесть – у 7 (7,7 %). Атипические изменения (ASCUS, LSIL, HSIL) по цитологическому исследованию были диагностированы в 26 (28,8%) случаев. Проведенный многофакторный анализ показал, при сочетании факторов риска ВИЧ, курение и ВПЧ в случаях с атипичной цитологической картине статистически значимо чаще встречались ВПЧ 6 и 33 типов (р<0,05), причем при ВПЧ 6 типе встречались все виды цитологической атипии, в том числе тяжелые поражения, при ВПЧ 33 типе - только LSIL.
Заключение. У ВИЧ-инфицированных женщин для снижения риска выявления РШМ на запущенных стадиях целесообразно рассмотреть возможность оптимизации скрининга в виде ко-тестирования и сокращения сроков этапности с учетом агрессивного развития и течения ВПЧ-ассоциированных форм заболевания у данного контингента. Необходимо детальное изучение структуры ВПЧ у женщин с ВИЧ инфекцией.
Анализ результатов применения иммунотерапии в 2-й и последующих линиях терапии у больных метастатическим и рецидивирующим раком шейки матки.
А.А. Дацюк1, М.А. Осипов3, С.В. Гамаюнов1,2.
1.ГАУЗ НО «Научно-исследовательский институт клинической онкологии «Нижегородский областной клинический онкологический диспансер». г.Нижний Новгород.
2. Медицинский радиологический научный центр им.А.Ф.Цыба-филиал ФГБУ «НМИЦ Радиологии» Минздрава России. г.Обнинск.
3. ГБУЗ «Ленинградская областная клиническая больница». г.Санкт-Петербург.
Автор ответственный за переписку: Дацюк Арина Андреевна, doc70doc@yandex.ru.
Значение: Рак шейки матки занимает пятое место по заболеваемости среди женщин во всем мире и шестое место по смертности (данные GLOBALCAN). Особую сложность представляют рецидивирующие формы, которые практически не поддаются первичному лечению в виде стандартной платиносодержащей химиотерапии с или без анти-VGFR агентом, следовательно, имеющие неблагоприятный прогноз. Внедрение иммунотерапии в лечение данной нозологии позволило улучшить отдалённые результаты.
Цель: сравнить выживаемость без прогрессирования у пациентов, получающих иммунотерапию в 2-й и последующих линиях терапии при метастатическом и рецидивирующем раке шейки матки. Поиск предикторов ответа на иммунотерапию рака шейки матки, влияющих на отдалённые результаты.
Материалы и методы: это проспективное многоцентровое исследование, куда включено 53 пациентки с исходно метастатическим или рецидивирующим раком шейки матки. Источником информации являлась ведущаяся база пациентов с раком шейки матки 2 клиник РФ: ГАУЗ НО «НИИКО «НОКОД» г.Нижний Новгород –n=35 (66%), ГБУЗ «Ленинградская областная клиническая больница» г.Санкт-Петербург –n=18 (34%). Средний возраст составил 56 лет (диапазон: 31-72г). Распределение по возрастным группам: до 60 лет- 33 пациентки (62%), старше 60 лет-20 пациенток (38%).
Распределение пациенток в зависимости от исходной стадии заболевания: II – 15 (28%), III – 27 (51%) и IV – 11 (21%). Основным иммунотерапевтическим агентом, назначаемым в обоих центрах, был Пембролизумаб. Известен статус курения пациенток c раком шейки матки: 25% (n=13) продолжают курить, никогда не курили 66% (n=35), бросили на момент проведения анализа всего 9% (n=5). Проведена оценка уровня экспрессии PD-L1 в биопсийном материале: низкий уровень - 42% (n=22), высокий - 38% (n=20), отсутствие экспресии - 17% (n=9), уровень не определён - у 2 пациенток (13%).
Иммунотерапия прервана по причине прогрессирования заболевания у 40% включенных в анализ пациенток. Частота иммуноопосредованных нежелательных явлений составила до 25%, что не потребовало отмены терапии. Наиболее частыми видами нежелательных явлений были тиреоидиты-54%, нефриты и дерматиты по 23%. В качестве предикторов ответа на терапию оценены: уровень тромбоцитов и лейкоцитов до начала терапии (норма или выше нормы), объём опухоли (>100 мм и <100 мм), а также линия назначения иммунотерапевтических препаратов. Период наблюдения с января 2023г. по настоящее время.
Результаты.
В ходе статического анализа собранных данных общая медиана выживаемости без прогрессирования (ВБП) составила 20,6 месяцев. С помощью log rank test оценивалась выживаемость до прогрессирования в зависимости от предикторов ответа. При нормальном уровне лейкоцитов и выше нормы медиана составила 23,7 и 13,4 месяца соответственно, выявлена разница в 10 месяцев, но нет статической значимости (p=0,7). В зависимости от размера опухоли: >100 мм и <100 мм - 8,63 и 56 мес. соответственно (p=0,04). Медиана ВБП по возрасту: до 60лет и старше 60 лет - 14 и 20,6 месяцев соответственно (p=0,81). При назначении пембролизумаба в 2-й линии после прогрессирования медиана ВБП составила 56 месяцев, а в 3-й и последующих линиях до 11,8 месяцев (р=0,024).
В многофакторном анализе с помощью регрессии Кокса статистически значимых различий в отношении медианы ВБП выявлено не было, что, на наш взгляд, связано с малым объёмом выборки и пока недостаточным количеством событий.
Заключение: исследование показало эффективность и безопасность пембролизумаба у пациенток с рецидивирующим раком шейки. Размер опухоли (менее 100 мм в диаметре) и интенсификация иммунотерапевтических агентов в более ранние линии терапии, а не высокий уровень экспрессии PD-L1, являются основными предикторами, определяющими ответ на терапию и улучающими отдаленные результаты.
Детекция сигнальных лимфатических узлов при раке шейки матки с использованием гибридного трейсера
Малютина С.А. врач-онколог ФГБУ НМИЦ онкологии им.
Н.Н.Блохина Минздрава России
Цель: Оценка эффективности детекции сигнальных лимфатических узлов (СЛУ)
при раке шейки матки (РШМ) с помощью гибридного трейсера (ГТ).
Актуальность: В настоящее время в онкогинекологии для картирования СЛУ
активно применяются флуоресцентный и радиоизотопный методы, каждый из которых
обладает известными достоинствами и недостатками. В данном исследовании
представлен новый способ детекции СЛУ на основе использования гибридного
препарата, сочетающий в себе преимущества указанных методов.
Материалы и методы: В НМИЦ онкологии им. Н.Н. Блохина с апреля по
декабрь 2025 г. было выполнено 40 расширенных оперативных вмешательств
пациенткам с верифицированным РШМ и клиническими стадиями IA1–IB2
(классификация FIGO, 2011 г.). Всем пациенткам на предоперационном этапе за
3–27 часов (медиана — 20,5 ч.) в строму шейки матки вводился гибридный препарат
(ICG-99mTc-альбумин). Спустя 1–2 часа для визуализации накопления препарата в
СЛУ выполнялась однофотонная эмиссионная компьютерная томография (ОФЭКТ).
Интраоперационно СЛУ визуализировались с помощью инфракрасного излучения и
гамма-датчика. Все удалённые СЛУ были направлены на срочное гистологическое
исследование.
Результаты: Оперативные вмешательства выполнялись как лапаротомным (65%,
26/40), так и малоинвазивным доступом (37,5%, 15/40). Расширенная гистерэктомия
была выполнена 65% (26/40) пациенткам, органосохраняющая операция — 25%
(10/40). В связи с выявленными метастазами в СЛУ 7,5% (3/40) пациенткам была
выполнена прерванная гистерэктомия с с парааортальной лимфаденэктомией.
По данным предоперационной ОФЭКТ односторонняя детекция СЛУ имела место в 35%
(14/40) случаев, двусторонняя — в 65% (26/40). Локализация СЛУ по данным ОФЭКТ
совпала с интраоперационными данными в 88,6% (31/40) случаев. Всего у 40
пациенток было удалено 82 СЛУ: 43 (52,4%) справа и 39 (47,6%) слева. С помощью
ГТ интраоперационная визуализация СЛУ была успешной у всех пациенток.
Одностороннее картирование отмечено в 7,5% (3/40) случаев, двустороннее — в
92,5% (37/40). По результатам срочного гистологического исследования метастазы
в СЛУ были обнаружены у 7,5% (3/40) пациенток. У одной пациентки
метастатический узел не являлся сторожевым. При плановом гистологическом
исследовании метастазы были выявлены ещё у двух пациенток. Таким образом, общая
частота метастатического поражения тазовых лимфоузлов составила 12,5% (5/40).
Точность детекции СЛУ с помощью ГТ достигла 97,5% (39/40), специфичность —
100%, чувствительность — 80%.
Качество таргетной визуализации СЛУ превосходит таковое при использовании
только флуоресцентного метода, а наглядность и простота обнаружения
оптимизируют процесс по сравнению с применением радиоизотопного метода.
Заключение: Методика детекции СЛУ с помощью ГТ доказала свою
эффективность, позволив выявить СЛУ у 100% пациенток. К её ключевым
преимуществам относятся: 1) возможность предоперационной визуализации; 2)
сокращение времени на интраоперационный поиск СЛУ; 3) превосходная
интраоперационная визуализация, в том числе при длительной экспозиции
препарата, в отличие от использования только ICG. Для определения
окончательного места метода в клинической практике необходимы дальнейшие
исследования, направленные на прямое сравнение его эффективности со
стандартными флуоресцентной и радиоизотопной методиками.
ДОВЕРИТЕЛЬНЫЙ ИНТЕРВАЛ / НА ЧТО МЫ ДЕЙСТВИТЕЛЬНО ДОЛЖНЫ СМОТРЕТЬ В АНАЛИЗЕ ВЫЖИВАЕМОСТИ?
Автор: Шило Полина Сергеевна
Врач-онколог клиники Лахта, исполнительный директор Высшей школы онкологии,
исполнительный директор Центра инновационных кооперированных
клинических исследований в онкологии, Санкт-Петербург
Кривые Каплана-Майера и связанные с ними показатели – медиана, отношения рисков, p-value – во многом определяют наш выбор тактики лечения в онкологии. Однако эти показатели нередко интерпретируются изолированно: из контекста выхватывается одно число, и на его основании делаются некорректные выводы.
На что же нужно смотреть в анализе выживаемости? На медианы? На отношение рисков? На p-value? На то, разошлись ли кривые в конце? В этой статье попробуем понять, на что действительно стоит ориентироваться.
На медианы выживаемости?
Медиана – самый цитируемый показатель в онкологической литературе. Она понятна, легко воспроизводима и удобна для сравнения. Однако медиана – это точечная оценка, описывающая ровно один момент на кривой: время, к которому у 50% пациентов произошло событие. Всё, что происходит до и после этой точки, медиана игнорирует.
Отличной иллюстрацией служит финальный анализ общей выживаемости в исследовании CLEAR (ленватиниб + пембролизумаб vs сунитиниб при мПКР первой линии) [1]. Медианы ОВ практически идентичны: 53,7 месяца в группе ленватиниба с пембролизумабом и 54,3 месяца в группе сунитиниба. Если ограничиться этим показателем, можно заключить, что разницы между препаратами нет.
Однако при анализе кривых Каплана-Майера мы видим совершенно иное (рис.1). На протяжении первых 48 месяцев кривая комбинации ленватиниб + пембролизумаб располагается значительно выше кривой сунитиниба. Landmark-анализ показывает: 24-месячная выживаемость составляет 80,4% vs 69,6%, 36-месячная – 66,4% vs 60,2%. То есть на протяжении первых трех лет наблюдения комбинация обеспечивает устойчивое и клинически значимое преимущество, ОР=0,79 (95% ДИ 0,63-0,99; p=0,0424).
Рисунок 1.
Исследование CLEAR: финальный анализ ОВ. Медианы практически равны (53,7 vs 54,3 мес.), но кривые расходятся на протяжении первых 4 лет наблюдения.

Почему медианы сошлись? Потому что кривые пересекаются именно вблизи отметки 50% – к 54 месяцам обе группы достигают медианы практически одновременно. Но это не означает, что результаты эквивалентны: тысячи пациенто-месяцев до этой точки были прожиты с разной вероятностью быть живым.
Резюме: медиана – полезный ориентир, но она не заменяет анализ формы кривой целиком. Необходимо оценивать выживаемость в нескольких временных точках (landmark analysis на 12, 24, 36 месяцах) и обращать внимание на форму кривых, их взаимное расположение и наличие плато.
На то, разошлись ли кривые в самом конце?
Ошибка, обратная первой, – чрезмерное внимание к правой части кривой. Утверждения вроде «кривые пересеклись в конце, значит эффект утрачен» могут не соответствовать действительности, если не учитывать число пациентов, остающихся под наблюдением.
Вернёмся к тому же исследованию CLEAR (рис.1). Обратите внимание на правый край кривой сунитиниба: после 60 месяцев наблюдается резкое ступенчатое падение. Это не свидетельство катастрофической поздней токсичности, а скорее артефакт: к этому моменту в группе сунитиниба под наблюдением оставалось всего 3 пациента. Смерть одного из них «сдвигает» кривую сразу на ≈17 процентных пунктов. Таблица number at risk наглядно демонстрирует: при 5 и 3 пациентах под наблюдением каждое единичное событие создаёт иллюзию масштабных изменений.
Ещё один наглядный пример – финальный анализ ОВ в исследовании адъювантного дабрафениба с траметинибом при BRAF-мутированной меланоме III стадии (COMBI-AD) [2]. На протяжении первых 100 месяцев кривая дабрафениба + траметиниба расположена выше плацебо, с landmark-оценками 3 года: 86% vs 77%, 5 лет: 79% vs 70%, 7 лет: 73% vs 66%. H=0,80 (95% ДИ 0,62-1,01; p=0,06). Однако после 108-110 месяцев кривые начинают сближаться, а на самом хвосте – практически пересекаются.
Рисунок 2.
COMBI-AD: финальный анализ ОВ (адъювантный дабрафениб + траметиниб vs плацебо). Обратите внимание на сближение кривых после 108 месяцев при NaR <30.

Означает ли это, что эффект адъювантной терапии «исчез»? Нет. К моменту пересечения под наблюдением остаётся менее 30 пациентов в каждой группе (из исходных ≈435). При таком number at risk доверительный интервал оценки выживаемости чрезвычайно широк, и любая оценка становится крайне неточной.
Резюме: прежде чем интерпретировать хвосты кривых, необходимо оценить number at risk. При маленьком объеме выборки в «хвостах кривых» любые расхождения или пересечения могут быть статистическим артефактом. Ширина доверительного интервала в этой зоне наглядно демонстрирует неточность оценки.
На отношение рисков?
Отношение рисков (ОР) или Hazard ratio (HR) – мера относительного эффекта. ОР=0,70 означает снижение риска события на 30% в каждый момент времени. Однако абсолютная клиническая значимость одного и того же ОР может быть очень разной в разных исследованиях.
На рисунке 3 представлены две симуляции (по 300 пациентов в каждой группе) с одинаковым HR=0,70. На панели A – агрессивная опухоль с медианой выживаемости около 3 месяцев: абсолютный выигрыш составляет всего 1,1 месяца. На панели B – опухоль с медианой выживаемости около 25 месяцев: тот же HR=0,70 даёт уже 8,3 месяца абсолютной разницы. Одна и та же относительная мера – восьмикратная разница в абсолютных числах.
Рисунок 3.
Смоделированный пример: один и тот же HR=0,70,
но абсолютная разница 1,1 мес. (A) vs 8,3 мес. (B).

Яркий клинический пример – исследование PA.3 при распространённом раке поджелудочной железы (гемцитабин + эрлотиниб vs гемцитабин + плацебо). ОР для ОВ составил 0,82 (95% ДИ 0,69-0,99; p=0,038) – формально статистически значимый результат. Однако абсолютная разница медиан составила 10 дней: 6,24 vs 5,91 месяца [3]. Несмотря на формальную значимость, клиническая релевантность этого результата остаётся дискуссионной.
Для сравнения: в исследовании MONALEESA-2 (рибоциклиб + летрозол vs плацебо + летрозол при HR+/HER2– мРМЖ первой линии) ОР для ОВ составил 0,76 (95% ДИ 0,63-0,93; p=0,008) – казалось бы, сопоставимый с PA.3. Однако абсолютная разница медиан – 12,5 месяца (63,9 vs 51,4 мес.) [4]. При похожем относительном эффекте абсолютный выигрыш отличается на порядки.
Резюме: ОР – относительная мера. Чтобы понять истинный эффект, необходимо анализировать и абсолютные цифры: разницу медиан и landmark-оценок выживаемости. Абсолютные цифры разницы в выживаемости при одинаковых значениях ОР могут оказаться абсолютно разными.
На p-value?
P-value показывает, насколько наблюдаемые данные несовместимы с заданной статистической моделью – как правило, с нулевой гипотезой об отсутствии различий между группами. Чем меньше p-value, тем сильнее эта несовместимость. Однако p-value не является ни вероятностью того, что нулевая гипотеза верна, ни вероятностью того, что результат обусловлен случайностью. А ещё р-value ничего не сообщает о размере эффекта и его клинической значимости.
На рисунке 4 смоделирована ситуация: исследование с 4000 пациентами (по 2000 в каждой группе). Кривые практически сливаются, разница медиан менее 1 месяца, HR=0,95. Тем не менее, p≈0,03 – результат формально «статистически значимый». При столь большой выборке мощность исследования достаточна для выявления различий, не имеющих практического значения.
Рисунок 4.
Смоделированный пример: статистическая
значимость при минимальной клинической разнице (n=4000,
Δ медиан <1 мес.).

Обратная ситуация не менее важна: клинически значимая разница может не достичь статистической значимости при недостаточной мощности. Вспомним тот же COMBI-AD (рис.2): HR=0,80 при p=0,06 – формально результат «незначимый», хотя 20%-ное снижение риска смерти выглядит клинически релевантным.
Резюме: p-value – пороговый фильтр, а не мера величины эффекта. Необходимо оценивать HR с доверительным интервалом и абсолютную разницу в выживаемости.
Так на что же смотреть?
Каждый из описанных примеров – следствие одной и той же ошибки: попытки свести многомерную картину к единственному числу. Медиана без формы кривой, HR без абсолютных цифр, p-value без доверительного интервала, хвосты без number at risk – любой из этих показателей в изоляции способен привести к неверному выводу. Поэтому самый правильный ответ на вопрос «на что смотреть?» – на всё сразу.
Список литературы:
- Motzer RJ, Porta C, Alekseev B, et al. Lenvatinib plus pembrolizumab versus sunitinib as first-line treatment of advanced renal cell carcinoma: final prespecified overall survival analysis of CLEAR. J Clin Oncol. 2024.
- Long GV, Hauschild A, Santinami M, et al. Final overall survival for adjuvant dabrafenib plus trametinib versus placebo in resected stage III BRAF-mutant melanoma (COMBI-AD). N Engl J Med. 2025.
- Moore MJ, Goldstein D, Hamm J, et al. Erlotinib plus gemcitabine compared with gemcitabine alone in patients with advanced pancreatic cancer: a phase III trial of the National Cancer Institute of Canada Clinical Trials Group. J Clin Oncol. 2007; 25 (15): 1960-1966.
- Hortobagyi GN, Stemmer SM, Burris HA, et al. Overall survival with ribociclib plus letrozole in advanced breast cancer. N Engl J Med. 2022; 386 (10): 942-950.