Дорогие коллеги, дорогие друзья!
Январь сродни началу новой главы книги, которую пишет каждый из нас. Кто-то четко представляет себе ее содержание, двигаясь строго по намеченному плану, а кто-то спонтанно и рутинно заполняет страницы, похожие одна на другую, не

Петер Мерк Менстед. В снежном пейзаже. Холст, масло, 1915
Петер Мерк Менстед. В снежном пейзаже.
Борис Пастернак. 1956 г.
*** Быть знаменитым некрасиво. Не это подымает ввысь. Не надо заводить архива, Над рукописями трястись. Цель творчества — самоотдача,

ОЦЕНИВАЕМ ОТЛОЖЕННЫЙ РИСК КАРДИОТОКСИЧНОСТИ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Успехи в лечении операбельного рака молочной железы сделали возможным для большинства пациенток быть излеченными и жить долго. Большинство из них для достижения этого результата получают в пред- и/или послеоперационном периодах...
ОДОБРЕНИЯ FDA В ОНКОУРОЛОГИИ В 2024 ГОДУ
Немышечно-инвазивный рак мочевого пузыря: ногапендикин альфа инбакицепт (НАИ) в комбинации с БЦЖ-терапией в лечении пациентов, не ответивших на БЦЖ...
В ДЕКАБРЕ 2024 ГОДА FDA ПРЕДОСТАВИЛО НЕСКОЛЬКО УСКОРЕННЫХ ОДОБРЕНИЙ ДЛЯ ЛЕЧЕНИЯ СОЛИДНЫХ ОПУХОЛЕЙ И МИЕЛОДИСПЛАСТИЧЕСКОГО СИНДРОМА
Суть ускоренного одобрения состоит в том, чтобы дать возможность использовать в практике лекарственные препараты, в отношении которых есть «намек» на эффективность, но «полноценные» доказательства эффективности еще не получены. При
ОДОБРЕНИЯ FDA В ЛЕЧЕНИИ ОПУХОЛЕЙ ЖКТ
Энкорафениб с цетуксимабом и mFOLFOX6 для первой линии терапии метастатического колоректального рака с мутацией BRAF V600E (20 декабря 2024)...

УГОЛОК РАДИОТЕРАПЕВТА / ПОВТОРНОЕ ОБЛУЧЕНИЕ ГЛИОБЛАСТОМЫ. ВСЕ ЛИ ВОПРОСЫ РЕШЕНЫ?
Поиск возможностей лечения глиобластомы уже несколько десятилетий является сверхзадачей ученых и практических врачей. И если в первичном лечении опухоли за последние 20 лет ничего нового не предложено, то в лечении рецидива или...
УГОЛОК РАДИОТЕРАПЕВТА / NCCN ОБНОВИЛИ РЕКОМЕНДАЦИИ ПО СКРИНИНГУ РАКА ЛЕГКОГО
Рак легкого является одной из ведущих причин смертности в мире, а у большинства пациентов этот диагноз обнаруживается на поздних стадиях. Успех скрининга в улучшении результатов выживаемости у пациентов с раком шейки матки, толстой...
УГОЛОК РАДИОТЕРАПЕВТА / SBRT: ЦЕЛЬ – ГОРТАНЬ
Можно себе представить негодование хирургов: какая еще SBRT при маленькой, легко досягаемой скальпелем опухоли голосовых связок?? Тем не менее, радиационных онкологов остановить сложно, и уже немалое количество успехов, достигнутых...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / АДЕНОКАРЦИНОМА ЛЕГКОГО С МУЦИНОЗНЫМ КОМПОНЕНТОМ: ХАРАКТЕРИСТИКА И ВОЗМОЖНОСТИ ЛЕЧЕНИЯ
Среди всех железистых форм немелкоклеточного рака легкого на долю аденокарциномы с муцинозным компонентом приходится не более 3-10%. Данный морфологический подтип представлен бокаловидными или столбчатыми клетками с...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / 2 ЛИНИЯ ТЕРАПИИ EGFR-МУТИРОВАННОГО НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО: ОБНОВЛЕННЫЕ ДАННЫЕ
Исследования, изучающие возможности лечения пациентов с EGFR-мутантным НМРЛ, прогрессирующих на фоне терапии осимертинибом, несколько меркнут на фоне более успешных и заметных работ по 1 линии, таких как, например, FLAURA,
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НИВОЛУМАБ И ИПИЛИМУМАБ В НЕОАДЪЮВАНТНОМ РЕЖИМЕ ПРИ НЕМЕЛКОКЛЕТОЧНОМ РАКЕ ЛЕГКОГО: ОБНОВЛЕННЫЕ РЕЗУЛЬТАТЫ CHECKMATE 816
8 января 2025 года в JCO были представлены обновленные результаты эксплораторного анализа исследования CheckMate 816, сравнившего эффективность платиносодержащей химиотерапии и комбинации ниволумаба и ипилимумаба без ХТ при...
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ОЦЕНКА ЧАСТОТЫ КОСТНЫХ ПЕРЕЛОМОВ В ИССЛЕДОВАНИИ PEACE-3 (223-RA + ЭНЗАЛУТАМИД VS ЭНЗАЛУТАМИД)
На ESMO 2024 было представлено исследование PEACE-3 [1], в котором сравнивалась комбинация 223-радия и энзалутамида с монотерапией энзалутамидом среди мало- и асимптомных пациентов с мКРРПЖ и костными метастазами. Исследование
НОВОСТИ ОНКОЛОГИИ / ОЛИГОПРОГРЕССИРУЮЩИЙ МЕТАСТАТИЧЕСКИЙ УРОТЕЛИАЛЬНЫЙ РАК – ВЫБОР ТАКТИКИ ПО МНЕНИЮ РОССИЙСКИХ ОНКОЛОГОВ
В отличие от других опухолей, концепция олигометастатического и, тем более, олигопрогрессирующего метастатического уротелиального рака не сформирована. В ретроспективных исследованиях и описаниях клинических случаев приводятся...
Анонс
-

20-21 МАРТА 2025
IX КОНФЕРЕНЦИЯ RUSSCO ОНКОУРОЛОГИЯ
Красноярск
-

20-21 МАРТА 2025
XI КОНФЕРЕНЦИЯ RUSSCO ОНКОГИНЕКОЛОГИЯ
Москва
Дорогие коллеги, дорогие друзья!
Январь сродни началу новой главы книги, которую пишет каждый из нас. Кто-то четко представляет себе ее содержание, двигаясь строго по намеченному плану, а кто-то спонтанно и рутинно заполняет страницы, похожие одна на другую, не задумываясь о том, что напишет завтра. Какой будет эта Книга Нового Года – во многом зависит от возможностей, желания и трудолюбия ее автора. Мы с вами - онкологи, диагносты, морфологи – изо дня в день пишем интереснейшие главы нашей жизни, касающиеся нашей непосредственной и любимой работы с пациентами. И Российское общество клинической онкологии готово помочь каждому сделать их максимально насыщенными, предлагая немалое количество вебинаров, дискуссионных клубов и крупных конференций, первая из которых – «Опухоли ЖКТ» - встречает своих участников уже в январе. Следите за календарем событий на сайте RosOncoWeb, программы конференций будут доступны минимум за 2 месяца до их начала, чтоб каждый из вас смог спланировать поездку или участие онлайн. И уже совсем скоро Программный комитет Российского онкологического конгресса начнет подготовку уже XXVIIII крупнейшего онкологического мероприятия года. Ждем ваших предложений, заявок, идей!
Перо в руке готово писать наш новый 2025 год, и пусть он будет максимально ярким и насыщенным добрыми, запоминающимися событиями!
Ваша команда RUSSCO
Петер Мерк Менстед. В снежном пейзаже. Холст, масло, 1915
Холст, масло, 1915

Борис Пастернак. 1956 г.
***
Быть знаменитым некрасиво.
Не это подымает ввысь.
Не надо заводить архива,
Над рукописями трястись.
Цель творчества — самоотдача,
А не шумиха, не успех.
Позорно, ничего не знача,
Быть притчей на устах у всех.
Но надо жить без самозванства,
Так жить, чтобы в конце концов
Привлечь к себе любовь пространства,
Услышать будущего зов.
И надо оставлять пробелы
В судьбе, а не среди бумаг,
Места и главы жизни целой
Отчеркивая на полях.
И окунаться в неизвестность,
И прятать в ней свои шаги,
Как прячется в тумане местность,
Когда в ней не видать ни зги.
Другие по живому следу
Пройдут твой путь за пядью пядь,
Но пораженья от победы
Ты сам не должен отличать.
И должен ни единой долькой
Не отступаться от лица,
Но быть живым, живым и только,
Живым и только до конца.
ОЦЕНИВАЕМ ОТЛОЖЕННЫЙ РИСК КАРДИОТОКСИЧНОСТИ У БОЛЬНЫХ РАКОМ МОЛОЧНОЙ ЖЕЛЕЗЫ
Автор: Тюляндин Сергей Алексеевич
Заслуженный деятель науки РФ, главный научный сотрудник
отделения противоопухолевой лекарственной терапии №2
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России,
член правления RUSSCO, профессор, доктор медицинских наук, Москва
Успехи в лечении операбельного рака молочной железы сделали возможным для большинства пациенток быть излеченными и жить долго. Большинство из них для достижения этого результата получают в пред- и/или послеоперационном периодах лучевую терапию, адъювантную химиотерапию, таргетную терапию в случае HER2 фенотипа и гормонотерапию при наличии гормональных рецепторов. Для этих больных становится важным качество жизни после окончания лечения, отсутствие симптомов хронической токсичности или возникновение различных заболеваний, обусловленных проведенной терапией. Вот почему мы сегодня активно дискутируем деэскалацию лечебных подходов за счет возможного отказа у отдельных больных от проведения лучевой терапии и химиотерапии или исключения отдельных противоопухолевых препаратов из схем нео- или адъювантной терапии. Работа, опубликованная в январском номере JCO, является еще одним свидетельством потенциально опасной токсичности, в данном случае – кардитоксичности противоопухолевого лечения. Антрациклины являются важнейшим компонентом химиотерапевтических схем лечения рака молочной железы с 1970-х годов. К сожалению, лечение антрациклинами сопровождается дозозависимым риском развития сердечной недостаточности. Трастузумаб используется более 25 лет при раке молочной железы с гиперэкспрессией HER2 и способен индуцировать раннюю сердечную дисфункцию, которая считается преходящей, обратимой и не указывает на будущую сердечную недостаточность. Кроме того, примерно 60% больных раком молочной железы получают лучевую терапию, которая также сопровождается дозозависимым риском сердечной дисфункции, когда сердце находится в поле облучения.
Несмотря на проведенные исследования, имеется лишь ограниченная информация о частоте и факторах риска сердечной дисфункции среди больных раком молочной железы, подвергшимся воздействию кардиотоксической терапии, прошедших лечение в реальных условиях и наблюдавшихся в течение длительного времени. Не было полностью изучено влияние традиционных сердечно-сосудистых факторов риска до и после постановки диагноза рака молочной железы (гипертония, дислипидемия, курение, диабет и ожирение) на частоту возникновения сердечной дисфункции, связанной с кардиотоксической терапией. Наконец, остается неизученным, является ли сердечная дисфункция, связанная с трастузумабом, действительно преходящей и ограниченной временем получения лечения. Устранению этих пробелов и посвящена опубликованная работа.
Авторы включили в исследование 829 женщин, больных раком молочной железы, которые закончили лечение более 1 года (за исключением возможной гормонотерапии), у которых было проведено кардиологическое обследование с выполнением эхокардиографии до начала лечения, не выявившее дисфункции сердечной деятельности. Этим пациенткам проводилось кардиологическое обследование с выполнением эхокардиографии каждые 2 года. Критериями оценки стало появление признаков сердечной дисфункции (ранней – в течение первых 2 лет и поздней – после двух лет) по данным эхокардиографии (снижение LVEF менее 50%).
Медиана возраста включенных пациенток в момент постановки диагноза составила 54,2 (20,3- 86,3) года, 29% принадлежали черной расе. Примерно 40% больных получили антрациклины с или без лучевой терапии, 16% получили трастузумаб и пертузумаб с или без лучевой терапии и 6% получили антрациклины с двойной HER2 блокадой с или без лучевой терапии. Еще 38% больных раком левой молочной железы получили только лучевую терапию, когда в зону облучения могла попадать сердечная мышца. Медиана кумулятивной дозы доксорубицина составила 240 мг/ м2, 95% больных получили кумулятивную дозу доксорубицина менее или равную 250 мг/м2. В популяции пациентов были зафиксированы следующие факторы риска для сердечно-сосудистых заболеваний: ожирение (20,4%), дислипидэмия (17%), гипертензия (12,1%), сахарный диабет (3,7%), курение (24.5%).
Таблица 1.
Частота снижения LVEF <50% при длительном наблюдении больных раком
молочной железы, получивших кардиотоксическую терапию

При медиане наблюдения 8,6 лет снижение сократительной способности миокарда менее 50% зарегистрировано у 86 (10,4%) пациенток с постепенным увеличением частоты с 1,8% при обследовании в 2 года до 15,3% на отметке 15 лет (Табл. 1). Основным драйвером увеличения частоты сердечной недостаточности было лечение антрациклинами. На отметке 15 лет в группе больных, получивших антрациклины без лучевой терапии, частота снижения LVEF менее 50% достигла 19,5%, а в комбинации с лучевой терапией – 22%. Добавление антрациклинов к анти-HER2 терапии увеличила частоту сердечной недостаточности с 8,2% до 17,3%. Проведение только лучевой терапии сочеталось с умеренным повышением частоты сердечной недостаточности с 0,3% до 7% на отрезке 15 лет. При использовании двойной анти-HER2 блокады отмечали как раннее развитие сердечной недостаточности в течение первых 2 лет (3%), так и позднее (8,2%). При оценке сердечно-сосудистых факторов риска по данным многофакторного анализа достоверное влияние на частоту развития сердечной недостаточности оказывало только наличие у пациентки артериальной гипертензии в момент постановки диагноза (HR=3,15; p=0,0004). Повышение артериального давления после окончания адъювантной терапии достоверно не влияло на частоту снижения сократительной способности миокарда (HR=1,16; p=0,55). В то время как возраст пациентки в момент постановки диагноза не играл достоверно негативной роли, принадлежность больной к черной расе достоверно увеличивало риск развития сердечной недостаточности (HR=2,42; p=0,0001).
Данное исследование демонстрирует, что при назначении относительно низкой кумулятивной дозы антрациклинов (250 мг/м2 и менее) у каждой пятой пациентки наблюдается снижение LVEF менее 50%. Кардиологи трактуют это состояние как сердечную недостаточность с умеренно низкой сократительной способностью миокарда, которая требует проведения медикаментозного лечения. Это существенно большие цифры в сравнении с 2-3% сердечной недостаточности, которыми мы ранее характеризовали кардиотоксичность антрациклинов. Эти цифры справедливы для 5-летнего наблюдения. На этом сроке, как правило, оканчивается период наблюдения онкологами, и в дальнейшем пациентка получает медицинскую помощь за пределами онкологической службы. При длительном наблюдении регистрируются значительно большие цифры сердечной недостаточности.
Добавление лучевой терапии к лечению антрациклинами увеличивает частоту сердечной недостаточности на 2-3%. Данное исследование также не подтверждает утверждение о преходящей природе сердечной недостаточности при назначении анти-HER2 терапии, что не исключает возможные различные механизмы реализации ранней и поздней дисфункции миокарда при ее назначении. Очевидна необходимость тщательного купирования и контроля артериальной гипертензии перед началом и в процессе противоопухолевой терапии, которая повышает риск развития сердечной недостаточности.
Но столь высокая частота кардиотоксичности при длительном наблюдении требует переосмысления назначения антрациклинов даже в относительно низкой кумулятивной дозе при проведении адъювантной химиотерапии. Понятна позиция тех, кто ратует за их отмену там, где можно без особой потери эффективности обойтись без них, заменив платиносодержащими комбинации при лечении HER2 фенотипа или таксансодержащими (например доцетаксел-циклофосфан) при гормоночувствительных опухолях. У отдельных больных (например, с гормоночувствительной опухолью или у пациенток пожилого возраста) возможно отказаться без негативного влияния на отдаленные результаты от проведения химиотерапии и лучевой терапии, назначив эффективную гормональную терапию. Это исследование подчеркивает необходимость выполнения эхокардиографии каждые 2-3 года для тех, кто получил антрациклины при проведении нео- и адъювантной химиотерапии. Раннее выявление снижения сократительной функции миокарда с инициацией лечения будет способствовать предупреждению развития клинически значимой сердечной недостаточности.
P.S. После прочтения данной статьи не стоит удивляться, почему у кардиологов появилась новая субспециальность – кардионкология. Мы с вами являемся ее творцами.
Источник:
Bostany J., Chen Y., Francisco L. et al. Cardiac dysfunction among breast cancer survivors: role of cardiotoxic therapy and cardiovascular risk factors. J. Clin. Oncol. 2025, 43:32-45.
ОДОБРЕНИЯ FDA В ОНКОУРОЛОГИИ В 2024 ГОДУ
Немышечно-инвазивный рак мочевого пузыря: ногапендикин альфа инбакицепт (НАИ) в комбинации с БЦЖ-терапией в лечении пациентов, не ответивших на БЦЖ
До сих пор не разработаны четкие алгоритмы лечения пациентов после прогрессирования на БЦЖ, опция радикальной цистэктомии (РЦЭ) является предпочтительной согласно многим клиническим рекомендациям [1-4], хотя для некоторых пациентов резервируется возможность ИТ пембролизумабом [5] или внутрипузырной ХТ GemTax [6, 7].
В патогенезе прогрессирования на БЦЖ нарушения в Т-клеточном и цитотоксическом клеточном ответах играют немалую роль. НАИ – суперагонист ИЛ-15 – представляет из себя химерный белок человеческого ИЛ15, связанного с димерным доменом рецептора ИЛ-15 альфа и IgG1 Fc, и приводит к активации NK-клеток и T-клеток памяти, в то же время обладает синергизмом с БЦЖ (рис.1).
Рисунок 1.
Строение ногапендикина альфа инбакицепта
и механизм его действия].
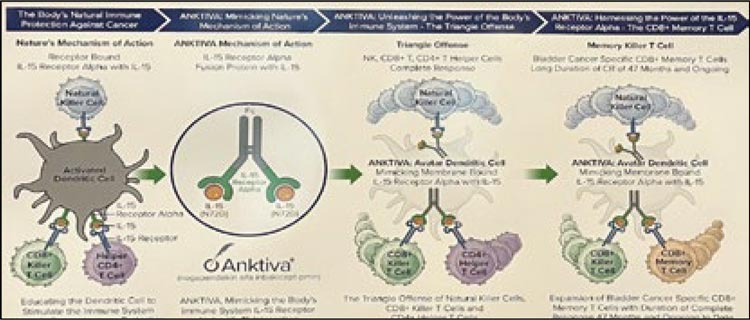
В исследовании QUILT-3.032 было предусмотрено включение пациентов в 3 когорты: когорта А – НАИ + БЦЖ в подгруппе CIS ± Ta/T1, когорта В – НАИ + БЦЖ в подгруппе Та/Т1 HG, когорта С – монотерапия НАИ в подгруппе CIS ± Ta/T1. Стоит отметить, что конечные точки в зависимости от когорты различались: для когорт А и С – 3- и 6-месячная частота полных ответов (ПО), для когорты В – выживаемость без признаков болезни (ВПБ) [8].
В когорте А частота ПО составила 71% (59/83 пациентов), медиана длительности ответа – 24,1 мес., частота РЦЭ составила 10,8% среди пациентов с ПО.
В когорте В однолетняя ВПБ составила 55,4%, медиана ВБП – 19,3 мес., частота РЦЭ – 7%.
Набор в когорту С остановлен независимым надзорным комитетом в связи с неудовлетворительными результатами (частота ПО – 20%) (рис.2).
Рисунок 2.
Когорты пациентов, включенные в исследование
QUILT-3.032, и основные результаты.
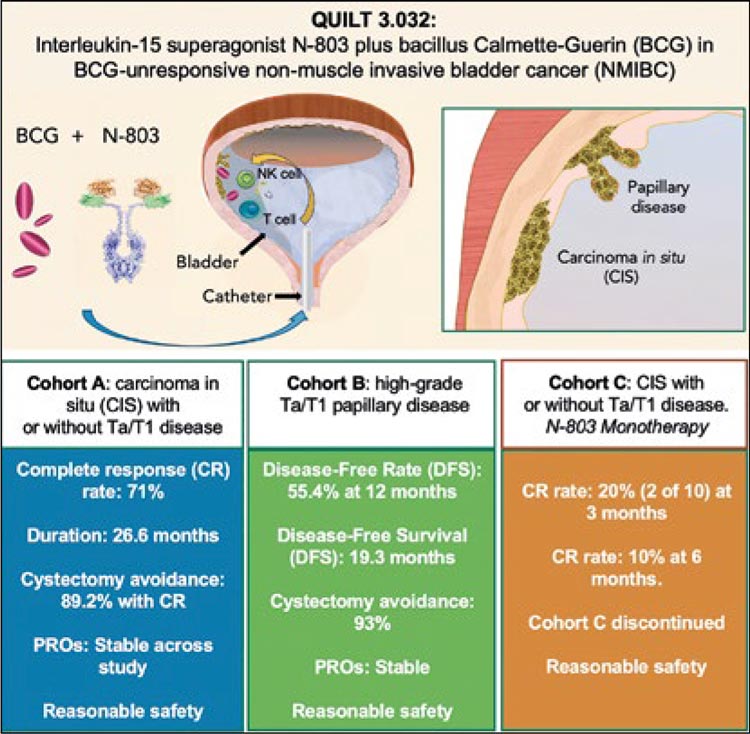
Немаловажно, что НАИ + БЦЖ не оказывают значимого негативного влияния на качество жизни пациентов [9].
Результаты данного исследования довольно значимы для реальной клинической практики, позволяя отказаться от РЦЭ для весомой части пациентов. FDA мимо не прошла и одобрила использование данного агента вместе с БЦЖ [10]. Выбранные первичные конечные точки для каждой из когорт удовлетворяют рекомендациям международной группы по изучению РМП [11], что также добавляет уверенности в эффективности этой опции. Один минус (и нет, это не длинное название) – отсутствие препарата в РФ. Очень будем ждать его появление!
Диссеминированный рак мочевого пузыря: комбинация ниволумаба с гемцитабином/цисплатином (GC) в 1 линии терапии распространенного уротелиального рака
На ESMO в 2023 году были представлены 2 исследования, посвященные 1 линии терапии диссеминированного уротелиального рака – EV-302 (энфортумаб ведотин/пембролизумаб vs гемцитабин/платина) [12] и CheckMate-901 (ниволумаб/GC vs GC) [13]. Оба исследования являются позитивными по своим первичным конечным точкам – ВБП и ОВ, и если первая работа, вызвавшая бурные овации на конгрессе, была одобрена FDA еще 15 декабря 2023 года [14], то химиоиммунотерапия (ХИТ) оставалась в тени вплоть до 6 марта 2024 года [15].
Результаты данных исследований стали поводом к смене рекомендаций всех профессиональных сообществ касательно 1 линии [1-4], отодвинув платиносодержащую ХТ с последующей поддержкой авелумабом на вторую роль (рис.3). Напомним, в исследование CM-901 включались пациенты с местнораспространенным нерезектабельным/ метастатическим уротелиальным раком (УР), не имеющие противопоказаний к цисплатину, и были рандомизированы в 2 группы – ниволумаб + GC vs GC. Первичные конечные точки – ВБП и ОВ.
Рисунок 3.
Рекомендации ESMO, RUSSCO, NCCN и EAU по лекарственной терапии 1 линии диссеминированного РМП.
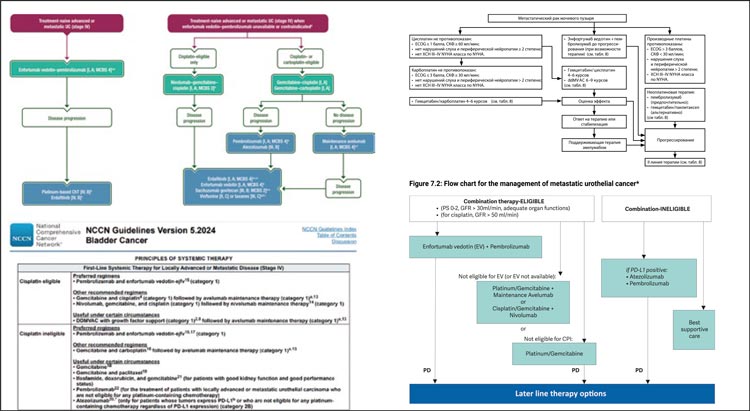
Медиана ОВ составила 21,7 и 18,9 мес. в группах ХИТ и ХТ соответственно (ОР=0,78; 95% ДИ 0,63-0,96; р=0,02) (рис.4А). Медиана ВБП равнялась 7,9 и 7,6 мес. в группах ХИТ и ХТ соответственно (ОР=0,72; 95% ДИ 0,59-0,88; р=0,001) (рис.4В). В то время как опция поддержки авелумабом после завершения платиновой ХТ и отсутствия прогрессирования уже стала стандартом 1 линии, исследование СМ-901 было в самом ходу. Лишь 14,5% пациентов из 87,2%, у которых не отмечено прогрессирования заболевания в группе GC, получили какую-либо ИТ в поддержке. Почему стоит сделать акцент на этом вопросе? Обратите внимание, в каком тесном контакте идут кривые до отметки в 6 мес., а далее начинают расходиться: ибо одни получают поддерживающую иммунотерапию, а другие нет. Так какова действительно роль ниволумаба, если не было четкого сравнения с текущим стандартом? Вопрос остается открытым…
Рисунок 4.
Общая выживаемость и выживаемость без
прогрессирования в исследовании СМ-901.

Диссеминированный РМП: эрдафитиниб во 2 и последующей линиях терапии
Несмотря на большое количество рандомизированных исследований в метастатическом РМП (мРМП), что делать после прогрессирования на всех новомодных опциях 1 линии – большой вопрос. Монохимиотерапия (паклитаксел, доцетаксел, винфлунином) обладает низкой частотой объективных ответов и ВБП, реиндукция ИТ не работает вовсе. Однако у 15% пациентов выявляется таргетируемая альтерация в генах FGFR2/3, к которой существует специфический ингибитор – эрдафитиниб.
В исследование THOR включались пациенты с обнаруженными альтерациями в генах FGFR2/3 и были разделены на 2 когорты: когорта 1 – эрдафитиниб vs моноХТ в группе пациентов с прогрессированием после предшествовавшей как минимум 1 линии системной терапии, включая анти-PD-1 или антиPD-L1 агенты, но не более 2 линий терапии [16]; когорта 2 – эрдафитиниб vs пембролизумаб среди пациентов с прогрессированием после как минимум 1 линии системной терапии, без предшествовавшей ИТ [17]. Первичная конечная точка – ОВ.
Результаты в когорте 1: ОВ в экспериментальной и контрольной группах составила 12,1 и 7,8 мес. соответственно (OP 0,64; 95% ДИ 0,47-0,88; р=0,005), ЧОО – 45,6% vs 11,5% в пользу эрдафитиниба (p<0,001) (рис.5).
Рисунок 5.
Когорта 1 исследования THOR и данные по общей
выживаемости.
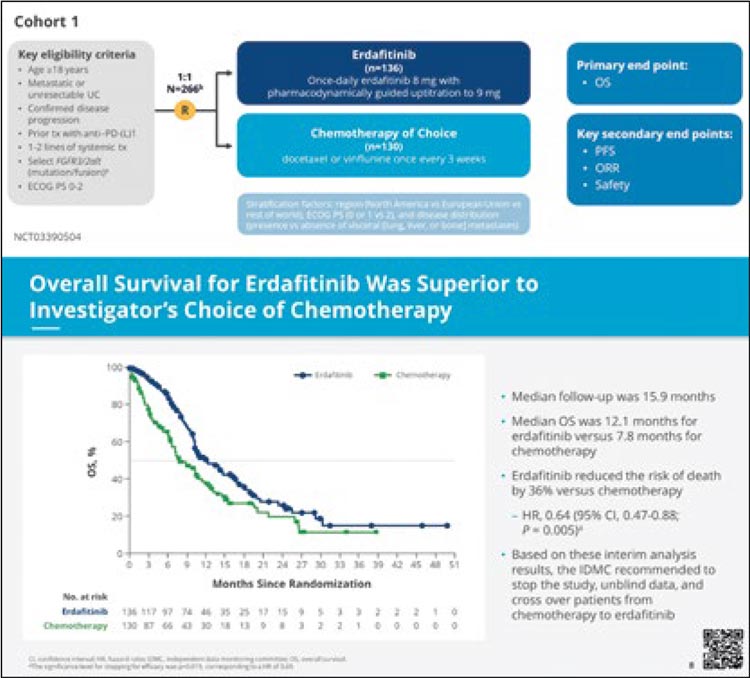
Результаты в когорте 2: ОВ в подгруппе эрдафитиниба и пембролизумаба составила 10,9 и 11.1 мес. (ОР 1,18; 95% ДИ 0,9-1,5; р=0,18), ЧОО – 40% vs 21,6% соответственно (р<0,001) (рис.6).
Рисунок 6.
Когорта 2 исследования THOR и данные по общей
выживаемости.
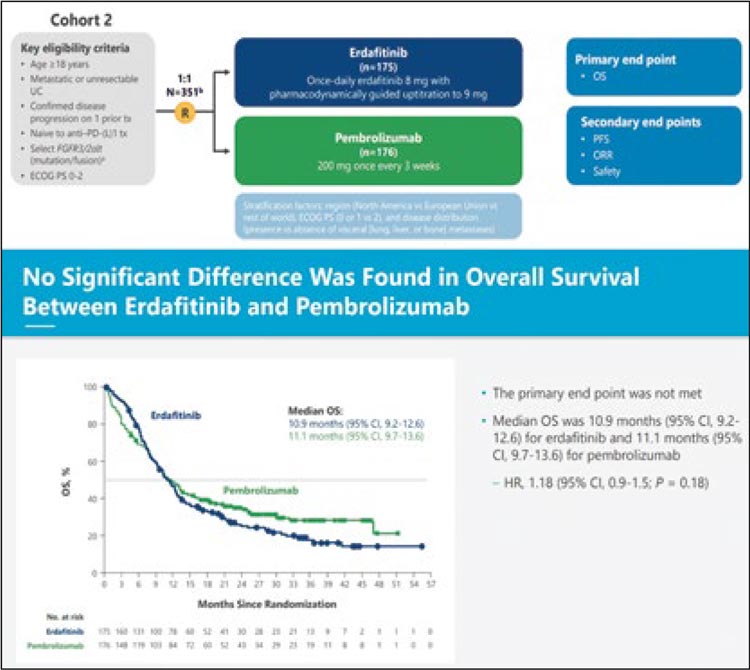
FDA в январе 2024 года одобрило использование эрдафитиниба во 2 и последующих линиях согласно критериям включения в когорту 1, т.е. после прогрессирования как на ХТ, так и ИТ [18]. Очень важно тестировать пациентов с мРМП на альтерации в генах FGFR2/3 и HER2/neu (но это совсем другая история) еще в 1 линии системной терапии для определения дальнейших возможностей лечения.
Диссеминированный РМП: отзыв одобрения FDA для сацитузумаба говитекана
Ранее в 2021 году FDA в ускоренном режиме одобрила сацитузумаб говитекан (СГ) для пациентов с мРМП – анти-TROP-2 конъюгат моноклонального АТ с цитостатиком (КМА) – на основе однорукавного исследования TROPHY-U-01 [19, 20], в котором данный КМА продемонстрировал достижение первичной конечной точки – частоты объективного ответа в 28% (при закладываемой в стат. гипотезе 24%) в группе пациентов с прогрессированием после платиносодержащей ХТ и ИТ.
Рисунок 7.
Дизайн исследования TROPiCS-04.
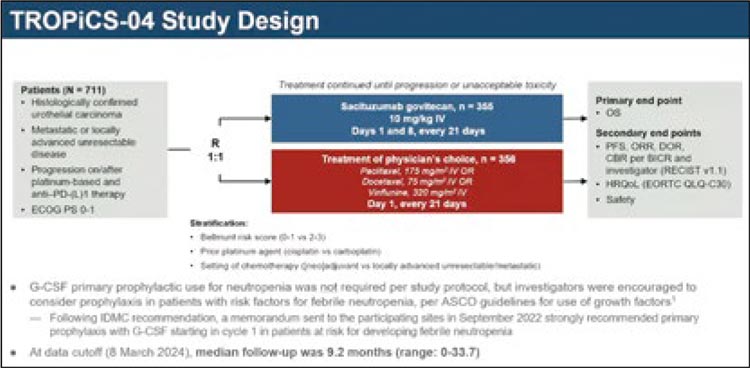
На ESMO 2024 представлены финальные результаты рандомизированного исследования TROPiCS-04 [21], в котором СГ сравнивался с ХТ по выбору врача (паклитаксел/ доцетаксел/винфлунин) среди пациентов с прогрессированием после химио- и иммунотерапии. Первичная конечная точка – ОВ (рис.7). При медиане наблюдения 9,2 мес. первичная конечная точка не была достигнута: медиана ОВ составила 10,3 vs 9,0 мес. в группах СГ и ХТ соответственно (ОР 0,86; 95% ДИ 0,73-1,02; р=0,087) (рис.8). В подгрупповом анализе не отмечено преимуществ в какой-либо из подгрупп. Терапия СГ ассоциирована с большим числом НЯ G3, особенно нейтропенией (35%; 12% – фебрильная нейтропения) и диареей (15%).
Рисунок 8.
Общая выживаемость в исследовании TROPiCS-04.
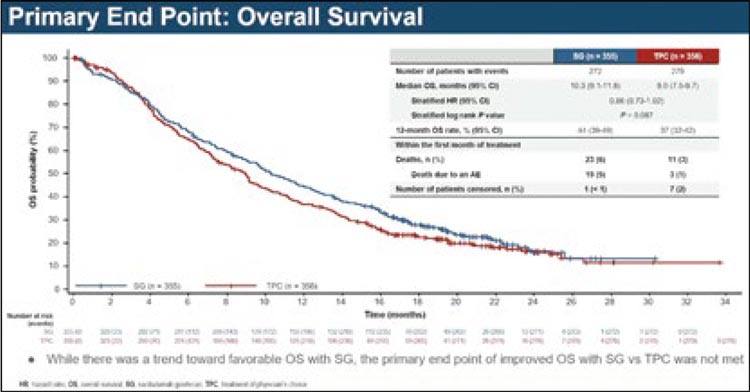
Полученные результаты послужили причиной к пересмотру собственного решения регулятором и отзыву СГ из терапии мРМП [22]. Как это часто бывает, успех во II фазе однорукавного исследования не транслируется в выигрыш в рандомизированной работе.
С интересом будем следить за тем, что готовит нам 2025 год, тем более что ASCO GU не за горами!
Источники:
- Powles T, et al. ESMO Clinical Practice Guideline interim update on first-line therapy in advanced urothelial carcinoma. Annals of Oncology. Jun. 2024; Vol.35, no.6, P.485-490. doi: 10.1016/j.annonc.2024.03.001.
- Румянцев А.А., Булычкин П.В., Волкова М.И. и соавт. Рак мочевого пузыря. Практические рекомендации RUSSCO, часть 1.2. Злокачественные опухоли. 2024; 14(3s2): 221-241. doi: 10.18027/2224-5057-2024-14-3s2- 1.2-09.
- Flaig TW, et al. NCCN Guidelines Version 5.2024. Bladder Cancer. 2024. Accessed: Jan. 12, 2025 [online].
- Muscle-invasive and Metastatic Bladder Cancer EAU Guidelines on. 2024.
- Necchi A, et al. Pembrolizumab monotherapy for high-risk non-muscleinvasive bladder cancer without carcinoma in situ and unresponsive to BCG (KEYNOTE-057): a single-arm, multicentre, phase 2 trial. Lancet Oncol. Jun. 2024; Vol.25, no.6, P.720-730. doi: 10.1016/S1470-2045(24)00178-5.
- Ben-David R, et al. Induction and maintenance of sequential intravesical gemcitabine/docetaxel for intermediate and high-risk non-muscle invasive bladder cancer with different dosage protocols. World J Urol. Dec. 2024; Vol.42, no.1. doi: 10.1007/S00345-024- 04992-5.
- Chevuru PT, et al. Long-term follow-up of intravesical gemcitabine and docetaxel as rescue therapy for nonmuscle-invasive bladder cancer. Journal of Clinical Oncology. Feb. 2022; Vol.40, no.6_suppl, P.573-573. doi: 10.1200/JCO.2022.40.6_ SUPPL.573.
- Chamie K, et al. IL-15 Superagonist NAI in BCG-Unresponsive NonMuscle-Invasive Bladder Cancer. NEJM Evidence. Nov. 2022; Vol.2, no.1. doi: 10.1056/EVIDOA2200167.
- Chamie K, et al. Quality of Life in the Phase 2/3 Trial of N-803 Plus Bacillus Calmette-Guérin in Bacillus CalmetteGuérin-Unresponsive NonmuscleInvasive Bladder Cancer. Urol Pract. Mar. 2024; Vol.11, no.2, P.367-375. doi: 10.1097/UPJ.0000000000000517.
- FDA approves nogapendekin alfa inbakicept-pmln for BCG-unresponsive non-muscle invasive bladder cancer. FDA. Accessed: Jan. 12, 2025 [online].
- Kamat AM, et al. Definitions, End Points, and Clinical Trial Designs for Non–Muscle-Invasive Bladder Cancer: Recommendations From the International Bladder Cancer Group. Journal of Clinical Oncology. Jun. 2016; Vol.34, no.16, P.1935-1944. doi: 10.1200/ JCO.2015.64.4070.
- Powles T, et al. Enfortumab Vedotin and Pembrolizumab in Untreated Advanced Urothelial Cancer. New England Journal of Medicine. Mar. 2024; Vol.390, no.10, P.875-888. doi: 10.1056/ NEJMOA2312117/SUPPL_FILE/ NEJMOA2312117_DATA-SHARING. PDF.
- van der Heijden MS, et al. Nivolumab plus Gemcitabine-Cisplatin in Advanced Urothelial Carcinoma. New England Journal of Medicine. Nov. 2023; Vol.389, no.19, P.1778-1789. doi: 10.1056/ NEJMOA2309863/SUPPL_FILE/ NEJMOA2309863_DATA-SHARING. PDF.
- FDA approves enfortumab vedotinejfv with pembrolizumab for locally advanced or metastatic urothelial cancer. FDA. Accessed: Jan. 12, 2025 [online].
- FDA approves nivolumab in combination with cisplatin and gemcitabine for unresectable or metastatic urothelial carcinoma. FDA. Accessed: Jan. 12, 2025 [online].
- Loriot Y, et al. Erdafitinib or Chemotherapy in Advanced or Metastatic Urothelial Carcinoma. New England Journal of Medicine. Nov. 2023; Vol.389, no.21, P.1961-1971. doi: 10.1056/NEJMOA2308849/SUPPL_ FILE/NEJMOA2308849_DATASHARING.PDF.
- Siefker-Radtke AO, et al. Erdafitinib versus pembrolizumab in pretreated patients with advanced or metastatic urothelial cancer with select FGFR alterations: cohort 2 of the randomized phase III THOR trial. Annals of Oncology. Jan. 2024; Vol.35, no.1, P.107- 117. doi: 10.1016/j.annonc.2023.10.003.
- FDA approves erdafitinib for locally advanced or metastatic urothelial carcinoma. FDA. Accessed: Jan. 12, 2025 [online].
- Loriot Y, et al. TROPHY-U-01, a phase II open-label study of sacituzumab govitecan in patients with metastatic urothelial carcinoma progressing after platinum-based chemotherapy and checkpoint inhibitors: updated safety and efficacy outcomes. Annals of Oncology. Apr. 2024; Vol.35, no.4, P.392-401. doi: 10.1016/j.annonc.2024.01.002.
- Tagawa ST, et al. TROPHY-U-01: A Phase II Open-Label Study of Sacituzumab Govitecan in Patients With Metastatic Urothelial Carcinoma Progressing After Platinum-Based Chemotherapy and Checkpoint Inhibitors. Journal of Clinical Oncology. Aug. 2021; Vol.39, no.22, P.2474- 2485. doi: 10.1200/JCO.20.03489/ ASSET/363320C0-C143-4EB8-B329- DA84FD9E735B/ASSETS/IMAGES/ LARGE/JCO.20.03489APP2.JPG.
- ESMO Asia Congress 2024. OncologyPRO. Accessed: Jan. 12, 2025 [online].
- FDA grants accelerated approval to sacituzumab govitecan for advanced urothelial cancer. FDA. Accessed: Jan. 12, 2025 [online].
Материал подготовил
Э.Р. Исраелян
В ДЕКАБРЕ 2024 ГОДА FDA ПРЕДОСТАВИЛО НЕСКОЛЬКО УСКОРЕННЫХ ОДОБРЕНИЙ ДЛЯ ЛЕЧЕНИЯ СОЛИДНЫХ ОПУХОЛЕЙ И МИЕЛОДИСПЛАСТИЧЕСКОГО СИНДРОМА
Суть ускоренного одобрения состоит в том, чтобы дать возможность использовать в практике лекарственные препараты, в отношении которых есть «намек» на эффективность, но «полноценные» доказательства эффективности еще не получены. При этом производитель препарата в рамках ускоренного одобрения должен продолжить дальнейшие клинические исследования, а уже по их результатам должен решаться вопрос о выдаче или, наоборот, отказе в выдаче «полноценного» разрешения FDA.
Таким образом, в теории ускоренное разрешение является временным и оговорено условием необходимости безоговорочного подтверждения эффективности. А на практике все может быть, конечно, по-другому…
1. R289 при миелодиспластическом синдроме (МДС)
2 декабря Rigel Pharmaceuticals Inc. объявила, что FDA предоставило fast track для R289 для использования у пациентов с ранее леченным МДС, зависящим от переливания крови.
R2891, селективный двойной ингибитор IRAK1 и IRAK4, в настоящее время исследуется в рамках исследования фазы 1b, оценивающего его безопасность, переносимость, фармакокинетику и предварительную активность у пациентов с МДС низкого риска, у которых произошел рецидив или которые невосприимчивы к предшествующей терапии.
2. LP-184 при тройном негативном раке молочной железы
3 декабря Lantern Pharma Inc. объявило, что FDA предоставило fast track для LP-184 у пациентов с тройным негативным раком молочной железы (TNBC). Это второе ускоренное одобрение, полученное для LP-184 в 2024 году, поскольку ранее оно было одобрено для глиобластомы.
Последние данные продемонстрировали способность LP-184 повышать чувствительность опухолей TNBC, которые не реагируют на ингибиторы контрольных точек, потенциально расширяя возможности лечения пациентов с ограниченным выбором терапии. LP184 в настоящее время проходит оценку в рамках исследования фазы 1A,оценивающего его безопасность и переносимость при широком спектре солидных опухолей, включая TNBC.
3. CRB-701 при рецидивирующем или рефрактерном метастатическом раке шейки матки
3 декабря Corbus Pharmaceuticals Holdings Inc. объявила, что FDA присвоило ускоренное одобрение CRB-701 (SYS6002), конъюгату антитело-лекарственное средство, нацеленному на нектин-4, для лечения рецидивирующего или рефрактерного метастатического рака шейки матки.
4. PT217 при раке предстательной железы
4 декабря биотехнологическая компания Phanes Therapeutics Inc. объявила, что ее первое в своем классе биспецифическое антитело к иммуноглобулину G-подобному PT217 получило от FDA fast track для лечения пациентов с метастатическим de novo нейроэндокринным раком предстательной железы.
Это второй fast track, которое FDA присвоило PT217, нацеленному на DLL3 и CD47. Ранее FDA уже одобрила PT217 для лечения мелкоклеточного рака легкого с прогрессированием после платиновой химиотерапии с ингибитором контрольной точки или без него. В многоцентровом исследовании SKYBRIDGE 1/2 фазы в настоящее время оценивается безопасность, эффективность, переносимость и фармакокинетика PT217 при запущенных или рефрактерных формах рака, экспрессирующих DLL3.
5. AdAPT-001 при рецидивирующей или рефрактерной саркоме мягких тканей
5 декабря EpicentRx объявила, что FDA предоставило ускоренное одобрение ингибитору бета-фактора роста, трансформирующего онколитический аденовирус (TGFβ), AdAPT-001, а также ингибитору PD-1 ниволумабу или ингибитору PD-L1 атезолизумабу для лечения рецидивирующей или рефрактерной прогрессирующей или метастатической саркомы мягких тканей (STS) с прогрессированием заболевания по крайней мере после одной предшествующей линии терапии.
Fast track был основан на данных КИ 1 и 2 фазы, оценивающих активность, безопасность и длительность ответа (ВБП приблизительно 8,5 мес.) у пациентов с STS и другими типами опухолей, либо отдельно, либо в комбинации с ингибитором контрольной точки.
6. IMM-1-104 при прогрессирующей меланоме
12 декабря корпорация Immuneering объявила об ускоренном одобрении своего ингибитора MEK, IMM-1- 104, для лечения пациентов с неоперабельной или метастатической меланомой с мутацией NRAS, которые прогрессировали или имели непереносимость чек-поинт ингибиторов. IMM-1-104 в настоящее время оценивается в рамках клинического испытания фазы 2a при запущенных солидных опухолях, включая меланому.
Материал подготовила
А.В. Фатеева
ОДОБРЕНИЯ FDA В ЛЕЧЕНИИ ОПУХОЛЕЙ ЖКТ
Энкорафениб с цетуксимабом и mFOLFOX6 для первой линии терапии метастатического колоректального рака с мутацией BRAF V600E (20 декабря 2024)
Рисунок 1.
Дизайн исследования BREAKWATER.
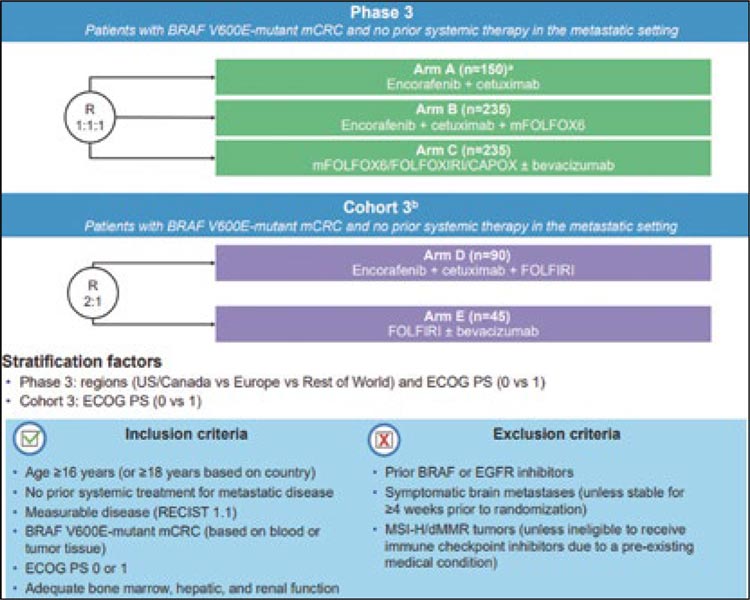
Эффективность оценивалась в BREAKWATER (NCT04607421) [1]. Пациенты изначально были рандомизированы 1:1:1 в одну из следующих групп лечения (рис.1):
- энкорафениб перорально один раз в день с внутривенной инфузией цетуксимаба каждые 2 недели (группа энкорафениб + цетуксимаб);
- энкорафениб перорально один раз в день с внутривенной инфузией цетуксимаба каждые 2 недели и mFOLFOX6 каждые 2 недели (группа энкорафениб + цетуксимаб + mFOLFOX6);
- mFOLFOX6, FOLFOXIRI (обе каждые 2 недели) или CAPOX (каждые 3 недели) – каждая с бевацизумабом или без него (контрольная группа).
Впоследствии исследование было изменено, чтобы ограничить рандомизацию (1:1) группой энкорафениб + цетуксимаб + mFOLFOX6 и контрольной группой. Лечение во всех группах продолжалось до прогрессирования заболевания, неприемлемой токсичности, отзыва согласия, потери для последующего наблюдения или смерти. Результаты послужили основой для этого ускоренного одобрения и описаны ниже.
Основным показателем эффективности был подтвержденный показатель объективного ответа (ORR): 61% (95% ДИ 52-70%) в группе энкорафениб + цетуксимаб, + mFOLFOX6 и 40% (95% ДИ 31-49%) в контрольной группе. Медиана продолжительности ответа (DoR) составила 13,9 мес. (95% ДИ 8,5 – не поддается оценке) и 11,1 мес. (95% ДИ 6,7-12,7) в соответствующих группах. Рекомендуемая доза энкорафениба составляет 300 мг (четыре капсулы по 75 мг) перорально один раз в день в сочетании с цетуксимабом и mFOLFOX6 (фторурацил, лейковорин и оксалиплатин) до прогрессирования заболевания или неприемлемой токсичности. Полная информация о дозировке приведена в инструкции по применению.
В исследовании BREAKWATER в отдельном рукаве также была оценен режим FOLFIRI в первой линии терапии у таких пациентов в сочетании с энкорафенибом и цетуксимабом. Продемонстрирована эффективность такого варианта лечения: ORR – 83%, медиана ВБП не достигнута.
Зенокутузумаб для терапии метастатического рака поджелудочной железы и немелкоклеточного рака легкого у предлеченных пациентов с NRG1 (нейрегулин 1) fusions (4 декабря 2024)
Это биспецифическое антитело, связывающее HER2 и HER3, что предотвращает их димеризацию и последующее связывание HER3 и NRG1.
Эффективность оценивалась в исследовании eNRGy (NCT02912949) [2]. В исследовании приняли участие 64 взрослых с прогрессирующим или метастатическим положительным по слиянию NRG1 НМРЛ и 30 взрослых с прогрессирующей или метастатической положительной по слиянию NRG1 аденокарциномой поджелудочной железы, у которых наблюдалось прогрессирование заболевания после стандартного лечения. Выявление положительного статуса слияния гена NRG1 было проспективно определено с помощью NGS (рис.2).
Рисунок 2.
Дизайн исследования eNRGy.
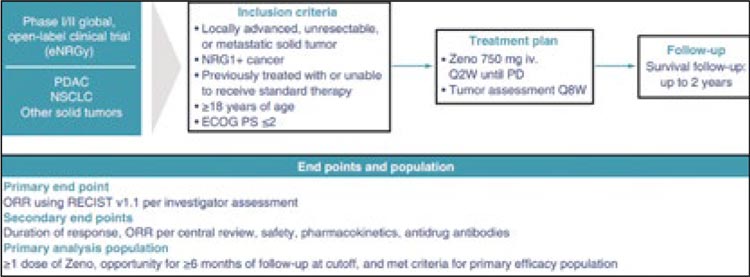
Основными показателями эффективности были ORR и DoR. Для аденокарциномы поджелудочной железы ORR составил 40% (95% ДИ 23-59%), а диапазон DOR составил от 3,7 до 16,6 мес. Среди пациентов с НМРЛ – 33% и 7,4 мес. соответственно. Компания-разработчик должна провести подтверждающее исследование. Рекомендуемая доза зенокутузумаба составляет 750 мг в виде внутривенной инфузии каждые 2 недели до прогрессирования заболевания или непереносимой токсичности. В объединенной популяции безопасности наиболее распространенными побочными реакциями (≥10%) были диарея, миалгии, астения. Наиболее распространенными лабораторными отклонениями 3 или 4 степени (≥10%) были повышение уровня гамма-глутамилтрансферазы, снижение гемоглобина, снижение натрия и снижение тромбоцитов.
Адаграсиб с цетуксимабом для лечения колоректального рака с мутацией KRAS G12C (21 июня 2024)
Эффективность оценивалась в KRYSTAL-1 [3]. Пациенты, соответствующие критериям, должны были иметь местнораспространенный или метастатический КРР с мутацией KRAS G12C, ранее получавшие стандартную терапию. Пациенты получали адаграсиб 600 мг два раза в день и цетуксимаб, вводимый либо два раза в неделю (500 мг/м2 каждые две недели), либо еженедельно (400 мг/ м2 начальная доза, затем 250 мг/м2 еженедельно). Оценки опухоли проводились каждые 6 недель. Прекращение приема адаграсиба требовало прекращения приема цетуксимаба, однако пациенты могли продолжать прием адаграсиба, если прием цетуксимаба был прекращен.
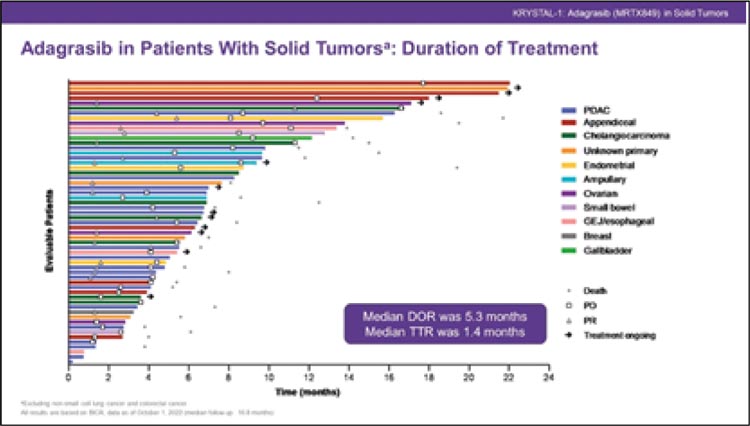
Основными показателями эффективности были ORR и DOR. У 94 включенных пациентов ORR составил 34% (95% ДИ 25-45%), а медиана DOR составила 5,8 мес. (95% ДИ 4,2- 7,6). У тридцати одного процента ответивших пациентов DOR составлял не менее 6 месяцев. Наиболее частыми побочными реакциями (≥20%) были сыпь, тошнота, диарея, рвота, гепатотоксичность (рис.3).
Рисунок 3.
Результаты исследования Krystal-1.
Липосомы иринотекана для лечения первой линии метастатической аденокарциномы поджелудочной железы (13 февраля 2024)
Эффективность оценивалась в NAPOLI 3 (NCT04083235) [4]. Пациенты были рандомизированы (1:1) для получения одного из следующих видов лечения:
- NALIRIFOX: иринотекан липосомы 50 мг/м2, оксалиплатин 60 мг/м2, лейковорин 400 мг/м2, фторурацил 2400 мг/м2 внутривенно в течение 46 часов, каждые 2 недели;
- Gem+NabP: Nab-паклитаксел 125 мг/м2, гемцитабин 1000 мг/м2 на 1, 8 и 15 день каждого 28-дневного цикла.
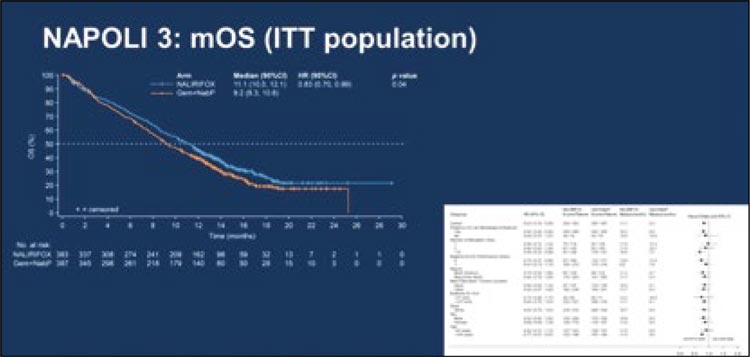
Основным показателем эффективности была общая выживаемость (OS). Дополнительными показателями эффективности были выживаемость без прогрессирования (PFS) по оценке исследователя и ORR. NAPOLI 3 продемонстрировал статистически значимое улучшение OS и PFS для группы NALIRIFOX по сравнению с группой Gem+NabP. Медиана OS составила 11,1 мес. (95% ДИ 10,0-12,1) в группе NALIRIFOX и 9,2 мес. (95% ДИ 8,3-10,6) в группе Gem+NabP (HR 0,84; 95% ДИ 0,71-0,99; p=0,0403) (рис.4). Медиана PFS составила 7,4 мес. в группе NALIRIFOX и 5,6 мес. в группе Gem+NabP, также статистически достоверно. ORR составила 41,8% в группе NALIRIFOX и 36,2% в группе Gem+NabP.
Однако учитывая эффективность режима mFOLFIRINOX, роль липосомального иринотекана в первой линии остается неясной.
Рисунок 4.
Общая выживаемость в исследовании NAPOLI 3.
Золбетуксимаб – моноклональное антитело к клаудину 18.2 (CLDN18.2) – в сочетании с химиотерапией в первой линии терапии метастатического HER2-негативного рака желудка/ пищеводно-желудочного перехода (18 октября 2024)
Эффективность золбетуксимаба была продемонстрирована в рандомизированных исследованиях III фазы SPOTLIGHT (NCT03504397) [5] и GLOW (NCT03653507) [6].
Рисунок 5.
График выживаемости без прогрессирования.
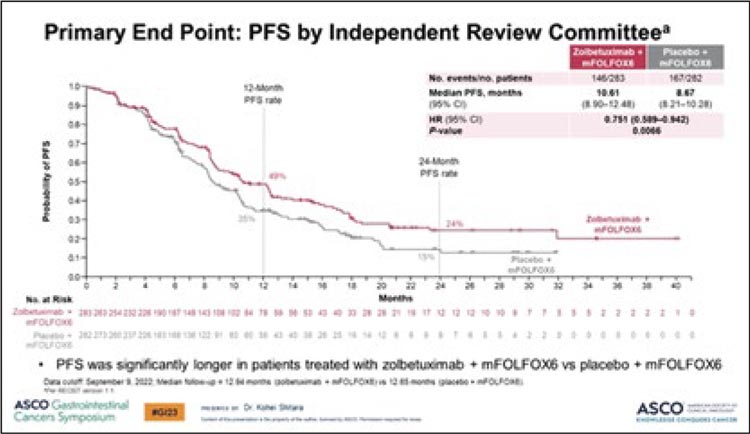
Рисунок 6.
График общей выживаемости.
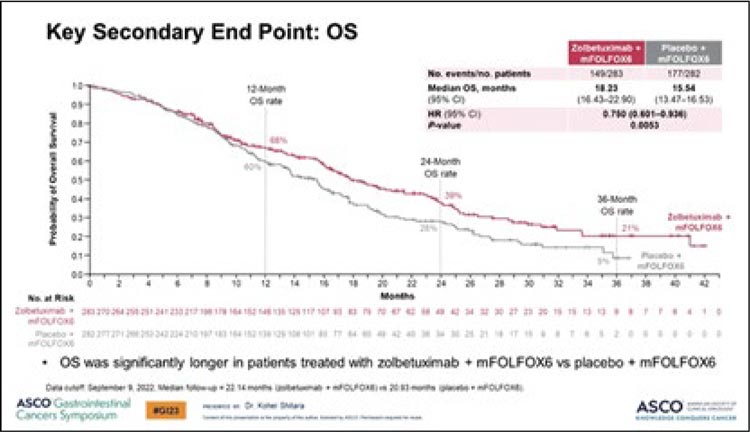
В исследование SPOTLIGH было включено 565 пациентов, которые были рандомизированы 1:1. Пациенты в 1 группе получали mFOLFOX6 в комбинации с золбетуксимабом, во 2 группе – FOLFOX с плацебо. ВБП при добавлении золбетуксимаба составила 10,6 мес. в сравнении с группой плацебо – 8,67 мес. (p=0,0066) (рис.5), а медиана ОВ в группе с золбетуксимабом составила 18,2 мес., в группе контроля – 15,5 мес. (p=0,0053) (рис.6). В исследовании GLOW приняли участие 507 пациентов, которые были рандомизированы 1:1 для получения золбетуксимаба с химиотерапией в режиме к CAPOX и получения плацебо в комбинацией с химиотерапией в режиме CAPOX. Добавление золбетуксимаба увеличило ВБП с 6,8 до 8,2 мес. (p=0,0007) (рис.7), а медиану ОВ с 12,2 до 14,4 мес. (p=0,0118) (рис.8).
Рисунок 7.
График выживаемости без прогрессирования.
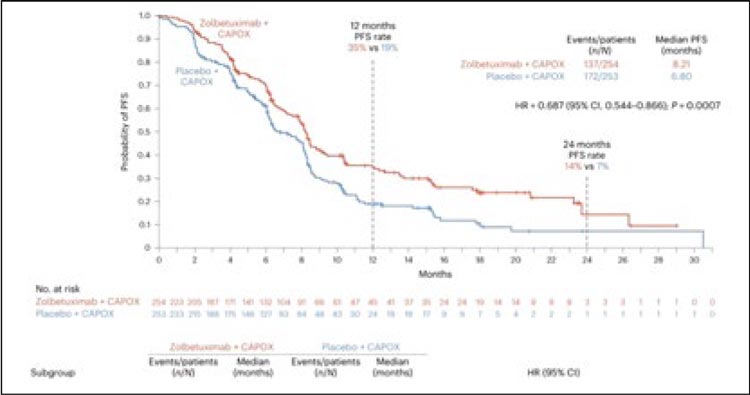
Рисунок 8.
График общей выживаемости.
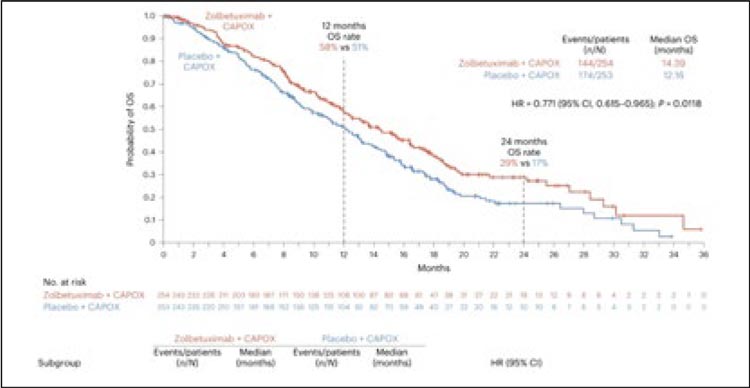
Тислелизумаб в качестве терапии второй линии при метастатическом плоскоклеточном раке пищевода (14 марта 2024)
Эффективность тислелизумаба была продемонстрирована в многоцентровом рандомизированном исследовании III фазы RATIONALE-302 [7], в котором приняли участие 512 пациентов, получивших ранее терапию первой линии по поводу метастатического плоскоклеточного рака пищевода. Исследование проводилось в 132 медицинских центрах в 11 странах Азии, Европы и США. Пациенты были рандомизированы 1:1 для получения тислелизумаба или химиотерапии (по выбору исследоваРисунок 3. Результаты исследования Krystal-1 Рисунок 4. Общая выживаемость в исследовании NAPOLI 3 теля паклитаксел, доцетаксел или иринотекан). Первичной конечной точкой была ОВ у всех пациентов. При применении тислелизумаба, по сравнению с химиотерапией, медиана ОВ составила 8,6 мес. против 6,3 мес. (р=0,0001) (рис.9).
Рисунок 9.
График общей выживаемости.
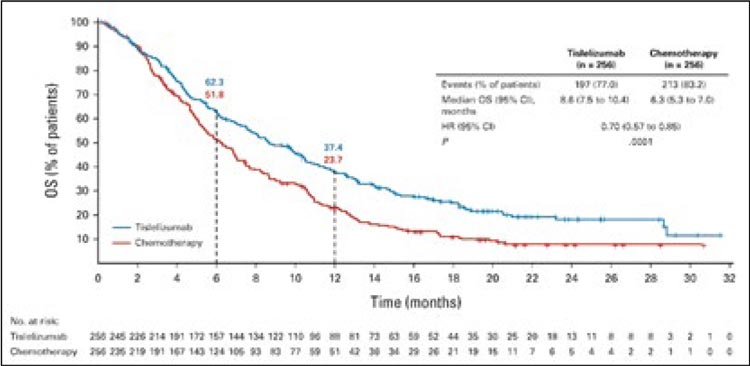
Занидатамаб в лечении метастатического HER2-положительного рака желчных желчевыводящих путей (20 ноября 2024)
Занидатамаб – биспецифическое моноклональное антитело к двум доменам рецептора HER2. Данный препарат продемонстрировал эффективность в исследовании II фазы HERIZON-BTC-01 [8]. В исследовании приняли участие 80 пациентов с HER2-позитивным диссеминированным раком желчных протоков, ранее получившие химиотерапию гемцитабином либо в комбинации с гемцитабином. Первичной конечной точкой исследования была ЧОО.
При медиане времени наблюдения в 12,9 мес. объективный ответ был достигнут у 41,3% пациентов при КРО 67,5% (рис.10). КРО более 6 мес. был отмечен у 47,5% больных при медиане длительности ответа 12,9 мес. Медина ВБП составила 5,5 мес.
Рисунок 10.
Показатель частоты объективных ответов.
Источники:
- Kopetz S, Bräcker M, George S, et al. BREAKWATER: an open-label, multicenter, randomized, phase 3 study, with a safety lead-in (SLI), of first-line (1L) encorafenib (E) + cetuximab (C) ± chemotherapy (CT) vs standard-of-care (SOC) CT for BRAF V600E-mutant metastatic colorectal cancer (mCRC). Journal of Clinical Oncology. 2023; 41: TPS3627-TPS3627. DOI: 10.1200/ JCO.2023.41.16_suppl.TPS3627.
- Kim DW, Schram AM, Hollebecque A, Nishino K, Macarulla T, Rha SY, Duruisseaux M, Liu SV, Al Hallak MN, Umemoto K, Wesseler C, Cleary JM, Springfeld C, Neuzillet C, Joe A, Jauhari S, Ford J, Goto K. The phase I/II eNRGy trial: Zenocutuzumab in patients with cancers harboring NRG1 gene fusions. Future Oncology. 2024; 20 (16): 1057-1067. DOI: 10.2217/fon-2023-0824.
- Pant S, Keng W, Hoffman P, et al. KRYSTAL-1: Activity and safety of adagrasib (MRTX849) in patients with advanced solid tumors harboring a KRASG12C mutation. Journal of Clinical Oncology. 2023; 41: 425082-425082. DOI: 10.1200/JCO.2023.41.36_suppl.425082.
- Wainberg ZA, Lawrence S, Van der Kloot M, et al. NAPOLI-3: A randomized, open-label phase 3 study of liposomal irinotecan + 5-fluorouracil/leucovorin + oxaliplatin (NALIRIFOX) versus nabpaclitaxel + gemcitabine in treatmentnaïve patients with metastatic pancreatic ductal adenocarcinoma (mPDAC). Journal of Clinical Oncology. 2023; 41: LBA661-LBA661. DOI: 10.1200/ JCO.2023.41.4_suppl.LBA661.
- Shitara K, Lordick F, Bang YJ, et al. Zolbetuximab + mFOLFOX6 as firstline (1L) treatment for patients (pts) with claudin-18.2+ (CLDN18.2+)/HER2- locally advanced (LA) unresectable or metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma: primary results from phase 3 SPOTLIGHT study. Journal of Clinical Oncology. 2023; 41 (suppl), abstr LBA292. DOI: 10.1200/ JCO.2023.41.3_suppl.LBA292.
- Xu R-H, et al. Zolbetuximab + Capox in 1L Claudin-18.2+ (CLDN18.2+)/HER2-Locally Advanced (LA) or Metastatic Gastric or Gastroesophageal Junction (mG/GEJ) Adenocarcinoma: Primary Phase 3 Results from Glow. 2023 ASCO Annual Meeting. Abstract 405736.
- Shen L, et al.; RATIONALE-302 Investigators. Tislelizumab Versus Chemotherapy as Second-Line Treatment for Advanced or Metastatic Esophageal Squamous Cell Carcinoma (RATIONALE-302): A Randomized Phase III Study. Journal of Clinical Oncology. 2022 Sep 10; 40 (26): 3065- 3076. DOI: 10.1200/JCO.21.01926. Epub 2022 Apr 20. Erratum in: Journal of Clinical Oncology. 2024 Feb 1; 42 (4): 486. DOI: 10.1200/JCO.23.02629. PMID: 35442766. PMCID: PMC9462531.
- Pant S, et al. Results from the pivotal phase (Ph) 2b HERIZON-BTC-01 study: Zanidatamab in previously-treated HER2- amplified biliary tract cancer (BTC). 2023 ASCO Annual Meeting. Abstract 4008.
Материал подготовили
Р. Ш. Абдулаева, Г. Г. Макиев
УГОЛОК РАДИОТЕРАПЕВТА / ПОВТОРНОЕ ОБЛУЧЕНИЕ ГЛИОБЛАСТОМЫ. ВСЕ ЛИ ВОПРОСЫ РЕШЕНЫ?
Автор: Панкратов Александр Евгеньевич
Ассистент кафедры онкологии и ТХ ГБУЗ МО МОНИКИ им. М.Ф. Владимирского,
ведущий эксперт по радиотерапии, врач-радиотерапевт ООО «ПЭТ-Технолоджи»,
Балашиха
Поиск возможностей лечения глиобластомы уже несколько десятилетий является сверхзадачей ученых и практических врачей. И если в первичном лечении опухоли за последние 20 лет ничего нового не предложено, то в лечении рецидива или продолженного роста отмечается определенная активность. В том числе она коснулась и лучевой терапии. В декабре 2024 года в «Зеленом журнале» Radiotherapy and Oncology опубликованы Рекомендации ESTRO/EANO по повторному облучению глиобластомы на основе состоявшегося консенсуса экспертов [1].
Интересно отметить, что руководство, построенное на консенсусе DELPHI, включило 18 рекомендаций и 9 утверждений, которые основаны на систематическом обзоре и на мнении экспертов. Причем 13 (48%) из них основаны на проспективных исследованиях и 14 (52%) – на мнении экспертов.
Основные рекомендации следующие:
- повторная лучевая терапия по поводу глиобластомы должна выполняться у отдельных отобранных пациентов;
- биологически эффективная доза должна составлять не менее 36 Гр при стандартном фракционировании или 35 Гр за 10 фракций;
- отсутствует необходимость делать отступ от GTV на CTV, а отступ на PTV не должен превышать 3 мм.
А теперь рассмотрим основные вопросы, возникающие при принятии решения о возможности повторной лучевой терапии, а также ответы, которые дает на них руководство, и наши комментарии к ответам.
1. Какого пациента можно рассматривать в качестве кандидата на повторную лучевую терапию?
– Пациента с KPS не менее 60 и интервалом после предыдущей лучевой терапии более 6 месяцев. Комментарий. Это, наверное, самый простой вопрос, который не нуждался бы в комментариях, если бы не случаи небольшой остаточной опухоли после хирургии и первичной химиолучевой терапии. Стоит ли их наблюдать, ожидая прогрессии или ответа на химиотерапию, или в ближайшее время выполнить радиохирургический буст?
2. Каким методом визуализации выявить рецидив?
– МРТ в последовательностях Т1 с контрастом, Т2, Т2 FLAIR и для дифференциальной диагностики с лучевым некрозом и псевдопрогрессией – МР-перфузия, МР-спектроскопия и ПЭТ-КТ с аминокислотами.
Комментарий. Никаких новых методов диагностики рецидива не предложено.
3. Как определить целевой объем облучения?
– Рекомендуется использовать для топометрии КТ в условиях иммобилизации пациента термопластической маской и МРТ с выполнением жесткого совмещения (fusion) изображений. В качестве GTV рассматриваются мишени, не превышающие 5-6 см в наибольшем диаметре. Отступ на CTV необязателен или по желанию делать его не более 3-5 мм, при этом обязательно делать отступ на PTV, равный 3 мм. Признано недопустимым выполнять повторное облучение при очагах более 5-6 см, множественных очагах и лептоменингеальном поражении.
Комментарий. Как известно, глиобластома чаще всего рецидивирует по краю послеоперационной полости/кисты. Осталось непонятным, стоит ли включать всю полость, по краю которой стелется рецидивная опухоль, или выбирать только солидный компонент? Исключить отступ на CTV, конечно, возможно, но не приведет ли это к продолженному росту по периферии еще до завершения курса повторного облучения?
4. Какова рекомендуемая доза при повторном облучении?
– Предлагается использовать режимы фракционирования с биологически эквивалентной дозой 36 Гр, получаемой за 18 фракций при облучении по 2 Гр за фракцию, или умеренного гипофракционирования с общей дозой 35 Гр за 10 фракций для крупных, но не превышающих 6 см рецидивных опухолей. Для небольших опухолей до 3 см предлагается использовать радиохирургию.
Комментарий. Основные вопросы по режимам фракционирования – достаточно ли будет 36 Гр на рецидивную опухоль, учитывая, что, скорее всего, она будет представлена наиболее радиорезистентными клонами клеток, выживших после первичной радиотерапии?
Отсутствуют рекомендации по выбору дозы для радиохирургии в зависимости от размера опухоли. Вероятно, предполагается использовать алгоритмы, применяемые при радиохирургии метастазов.
5. Какой метод планирования и проведения повторного облучения предпочесть?
– Рекомендуются технологии SRS, VMAT/IMRT с обязательным использованием IGRT. Настоятельно рекомендуется рассмотреть возможность протонной терапии.
Комментарий. С подобным акцентированием внимания на использовании протонной терапии, конечно, хотелось бы видеть более четкие рекомендации по показаниям для ее применения.
6. Как оценивать кумулятивные дозы на органы риска с точки зрения безопасности?
– Эксперты честно сообщают, что в настоящее время исследования в этом направлении еще продолжаются. Предлагается использование ограничений на органы риска, как и при первичном облучении, но со скидкой на ранее полученную дозу.
7. Использовать ли повторное облучение в комбинации с лекарственной терапией?
– Ответ на этот вопрос в рекомендациях не нашел консенсуса.
8. Использовать ли поддерживающую системную терапию после повторного облучения?
– Как и в случае сопутствующей терапии, доказательств в преимуществе назначения поддерживающей терапии после повторного облучения не получено.
9. Каков график последующего наблюдения после повторной лучевой терапии?
– Рекомендуется контрольная традиционная МРТ каждые три месяца. Таким образом, с одной стороны, мы получили достаточно четкие ответы на основные вопросы радиотерапевтов – о режиме фракционирования и дозировании, показаниях и противопоказаниях. Но некоторые вопросы остались незаданными и, следовательно, неотвеченными. Например, возможность повторной лучевой терапии при глиобластоме у детей или при поражении спинного мозга. Но самое главное, пока отсутствует достоверная информация о преимуществах повторной лучевой терапии при рецидиве по сравнению с системной лекарственной терапией. Возможно, на этот вопрос даст ответ рандомизированное исследование III фазы LEGATO, сравнивающее системную терапию ломустином с или без повторной лучевой терапией при рецидиве глиобластомы [2].
Источники:
- Andratschke N, Heusel A, Albert N, Alongi F, Baumert B, Belka C, Castellano A, Dhermain F, Erridge S, Grosu A-L, Lagerwaard F, Lukacova S, Per Munck af Rosenschold, Niyazi M, Nieder C, Preusser M, Smits M, Weber D, Weber W, Weller M, Williamson A, Minniti G. ESTRO/EANO recommendation on reirradiation of glioblastoma, Radiotherapy and Oncology. 2025; Vol.204, 110696. ISSN 01678140. doi: 10.1016/j.radonc.2024.110696.
- Preusser M, Kazda T, Le Rhun E, Sahm F, Smits M, Gempt J, Koekkoek JA, Monti AF, Csanadi M, Pitter JG, Bulbek H, Fournier B, Quoilin C, Gorlia T, Weller M, Minniti G; European Organisation for Research, Treatment of Cancer (EORTC) Brain Tumor Group. Lomustine with or without reirradiation for first progression of glioblastoma, LEGATO, EORTC-2227- BTG: study protocol for a randomized phase III study. Trials. 2024 Jun 7; 25(1): 366. doi: 10.1186/s13063-024- 08213-7. PMID: 38849943. PMCID: PMC11157762.
УГОЛОК РАДИОТЕРАПЕВТА / NCCN ОБНОВИЛИ РЕКОМЕНДАЦИИ ПО СКРИНИНГУ РАКА ЛЕГКОГО
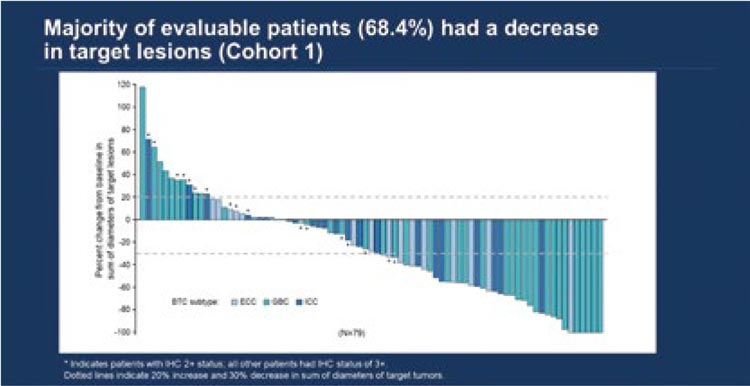
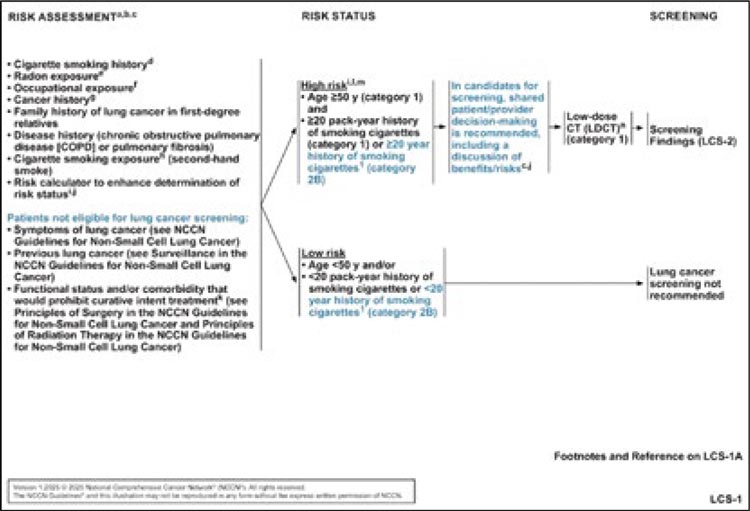
Рак легкого является одной из ведущих причин смертности в мире, а у большинства пациентов этот диагноз обнаруживается на поздних стадиях. Успех скрининга в улучшении результатов выживаемости у пациентов с раком шейки матки, толстой кишки и молочной железы вдохновил на разработку эффективного скрининга рака легких.
Первая рекомендация по проведению скрининга рака легкого появилась в 2013 году и была разработана целевой группой по профилактическим услугам США (USPSTF). Последующие исследования, в том числе исследование NELSON [1], продемонстрировали высокую эффективность низкодозной КТ грудной клетки среди пациентов высокого риска, к которым относятся курильщики. Целью любого скрининга рака стоящее время, либо бросили курить) и имевшие по крайней мере один дополнительный фактор риска, такой как профессиональное воздействие канцерогенов. Важно учесть, что, согласно предыдущим рекомендациям, скрининг рекомендовался лицам от 55 до 74 лет, со стажем курения более 30 лет. А в рекомендациях USPSTF и CMS скринингу не подлежали лица, которые не курят уже 15 лет. Хоть отказ от курения и снижает риск развития рака легкого, анализ Framingham Heart Study показал, что риск рака легких остается более чем в 3 раза выше у лиц, которые ранее курили. Поэтому NCCN решил убрать данные ограничения по скринингу и рекомендует проводить низкодозную КТ и пациентам, которые бросили курить, если они подходят под ключевые критерии. Рисунок 1. Рекомендации NCCN Ver.1.2025 в отношении скрининга рака легкого • Не подлежат скринингу некурящие лица в возрасте <50 лет и/или с историей курения менее 20 лет. Их NCCN относит к низкому риску, поскольку вероятность выявления рака легких составляет <1%, а риски, связанные с обследованием, перевешивают преимущества скрининга. является выявление заболевания на ранней стадии, когда оно не вызывает симптомов и когда лечение будет наиболее успешным.
Рисунок 1.
Рекомендации NCCN Ver.1.2025 в отношении
скрининга рака легкого.
Идеальный скрининг:
- должен улучшать результаты выживаемости;
- быть научно обоснованным (например, иметь приемлемые уровни чувствительности и специфичности) с низкой частотой ложноположительных результатов, предотвращая ненужное дополнительное тестирование;
- быть малорискованным, воспроизводимым, доступным и рентабельным. В обновленных рекомендациях [2] NCCN расширил критерии высокого риска для определения показаний к скринингу (рис.1):
- Скринингу подлежат лица ≥50 лет с историей курения сигарет более 20 лет (которые либо курили в настоящее время, либо бросили курить) и имевшие по крайней мере один дополнительный фактор риска, такой как профессиональное воздействие канцерогенов.
Важно учесть, что, согласно предыдущим рекомендациям, скрининг рекомендовался лицам от 55 до 74 лет, со стажем курения более 30 лет. А в рекомендациях USPSTF и CMS скринингу не подлежали лица, которые не курят уже 15 лет. Хоть отказ от курения и снижает риск развития рака легкого, анализ Framingham Heart Study показал, что риск рака легких остается более чем в 3 раза выше у лиц, которые ранее курили. Поэтому NCCN решил убрать данные ограничения по скринингу и рекомендует проводить низкодозную КТ и пациентам, которые бросили курить, если они подходят под ключевые критерии.
- Не подлежат скринингу некурящие лица в возрасте <50 лет и/или с историей курения менее 20 лет. Их NCCN относит к низкому риску, поскольку вероятность выявления рака легких составляет <1%, а риски, связанные с обследованием, перевешивают преимущества скрининга.
Источники:
- Harry J. de Koning, et al. Reduced Lung-Cancer Mortality with Volume CT Screening in a Randomized Trial. N Engl J Med. 2020; 382: 503-513. DOI:10.1056/NEJMoa1911793.
- Lung Cancer Screening. NCCN Guidelines, Version 1.2025.
УГОЛОК РАДИОТЕРАПЕВТА / SBRT: ЦЕЛЬ – ГОРТАНЬ
Автор: Деньгина Наталья Владимировна
Заведующая радиологическим отделением ГУЗ «Областной клинический онкологический диспансер»,
директор Центра лучевой терапии «R-Spei», член правления RUSSCO, главный редактор Газеты RUSSCO
и сайта RosOncoWeb, кандидат медицинских наук, Ульяновск
Можно себе представить негодование хирургов: какая еще SBRT при маленькой, легко досягаемой скальпелем опухоли голосовых связок?? Тем не менее, радиационных онкологов остановить сложно, и уже немалое количество успехов, достигнутых при использовании метода стереотаксической лучевой терапии (SBRT) в лечении опухолей различных локализаций, будет стимулировать проведение дальнейших исследований. В фокусе для итальянских авторов оказались опухоли складочного отдела гортани минимального размера – Т1a-b. Результаты первого проспективного исследования I/ II фазы были опубликованы в январском номере журнала IJROBP, и многие специалисты расценили их как революционные – хотя и требующие дальнейшей доработки.
Исследования были начаты еще в 2017 году, авторы постепенно разрабатывали наиболее оптимальный подход к максимально точному облучению самой опухоли голосовой связки всего за 3 фракции, хотя в настоящее время наиболее принято гипофракционированное облучение всего связочного отдела гортани при начальной стадии процесса. В исследование включались всесторонне обследованные пациенты с плоскоклеточным раком Т1a и Т1b, ранее не получавшие ни хирургического, ни лучевого лечения. Во время КТ-топометрии и последующего лечения пациентам было запрещено делать глотательные движения. Каждая истинная голосовая складка была разделена на трети вдоль аксиальной плоскости, и та часть (или части), которая содержала в себе подтвержденную злокачественную опухоль, получала 36 Гр за 3 фракции (CTV36), тогда как прилегающие участки в каждом направлении (передний и задний) – 30 Гр за те же 3 фракции (CTV30). Лечение проводилось методом SBRT через день. Передняя комиссура считалась отдельным сегментом. Она факультативно получала 30 Гр в случаях, если опухоли располагались в передней трети складки, хотя при наличии макроскопической опухоли в области комиссуры эта зона получала 36 Гр, тогда как незатронутая передняя треть – 30 Гр. Щитовидный и перстневидный хрящи, а также воздушная полость гортани всегда исключались из любого CTV. Расширение до соответствующего целевого объема планирования (PTV) подразумевало 3 мм латеро-латерально и передне-задне и 5 мм кранио-каудально.
Оценка результатов проводилась через 2 недели и 1, 2 и 6 месяцев после SBRT, а затем каждые 6 месяцев. При каждом последующем наблюдении пациент проходил фиброларингоскопию; токсичность оценивалась врачом в соответствии со шкалой общих терминологических критериев для нежелательных явлений, версия 5.0.
Что касается результатов, репортируемых пациентами: анкета Voice Handicap Index (VHI) заполнялась на исходном уровне до начала лечения и через 1, 2 и 6 месяцев после SBRT, а затем ежегодно.
Первичной конечной точкой исследования был локальный рецидив, определяемый как наличие персистирующей/рецидивной опухоли в голосовой щели. Вторичными конечными точками были частота осложнений и качество голоса после SBRT
С мая 2017 года по март 2021 года было включено 33 пациента (23 – с Т1а, 10 – с Т1b). Ни один из них не был исключен по причине дозиметрических данных при планировании, и, таким образом, все были пролечены по предложенной схеме. Однако набор был прекращен, когда второй случай хондронекроза был зарегистрирован в марте 2021 года. Медиана наблюдения составила 51,5 мес. (47,9-61 мес.).
При последнем наблюдении все пациенты были живы и без признаков заболевания, кроме 2 больных, которые умерли через 61,5 и 21,3 мес. после SBRT по интеркуррентным причинам. Таким образом, четырехлетняя общая выживаемость составляет 97,0% (95% ДИ 91,1-100%), при этом локальный контроль за 4 года составил 100%.
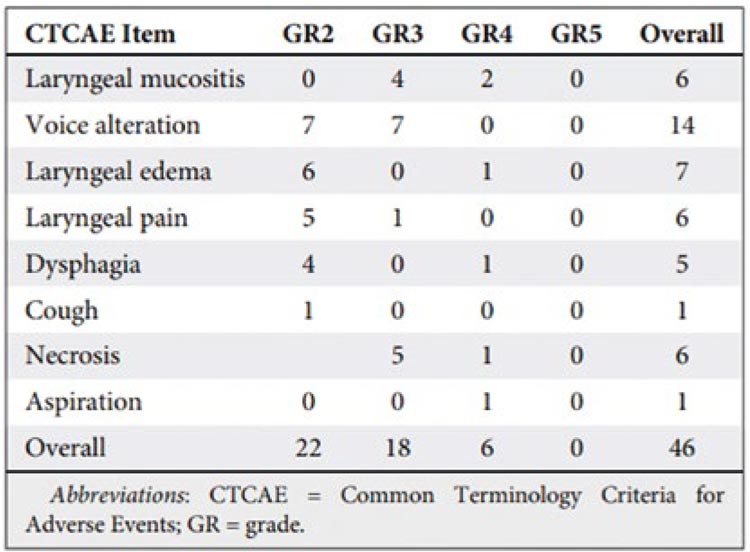
Наиболее важным моментом исследования, игнорировать который невозможно, стала токсичность. Практически у всех пациентов отмечена токсичность 2 степени и выше (рис.1).
Рисунок 1.
Частота возникновения и виды
токсичности Grade2+ в исследовании.
У шести пациентов (18,2%) развился некроз мягких тканей (N=4) или некроз хряща (N=2) по прошествии среднего промежутка времени 14,9 мес. от SBRT. Пять из шести некрозов наблюдались у пациентов, которые продолжали курить и/или недавно перенесли инфекцию COVID. Все 4 мягкотканных некроза благополучно разрешились с помощью консервативной терапии.
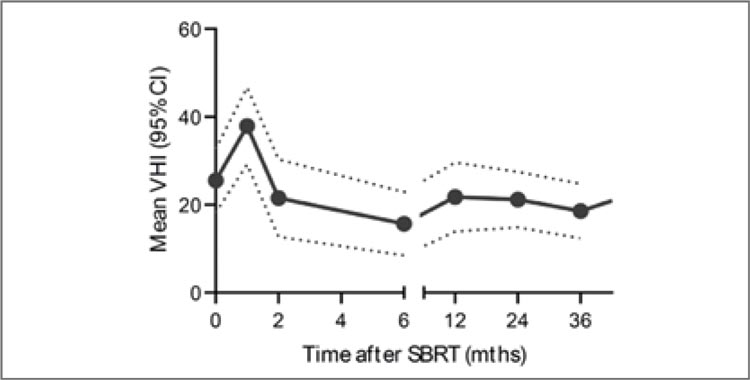
Что касается качества голосовой функции, после первоначального ухудшения средний балл индекса нарушения голоса значительно улучшился спустя 6 месяцев по сравнению с исходным уровнем (рис.2).
Рисунок 2.
Изменения качества голоса
(согласно данным репортирования пациентов).
Это исследование показывает, что SBRT в дозе 36 Гр за 3 фракции на область непосредственной опухоли голосовой связки является высокоэффективной терапевтической опцией при T1N0, хотя токсичность, в частности, некрозы, вызывает беспокойство и требует дальнейших разработок. Будущие направления включают исследование дозиметрических факторов и сопутствующих негативных факторов прогноза поздней токсичности. С учетом высокого локального контроля над опухолью, но неприемлемых показателей поздних осложнений, возможным решением является небольшое снижение предписанной дозы для макроскопической опухоли. Поэтому в настоящее время проводится новое исследование, в котором доза снижена до 30 Гр за 3 фракции на PTV и 27 Гр на зоны субклинического распространения. Возможно, отбор пациентов (с предпочтением некурящих) также будет иметь значение во избежание столь негативных последствий, как некроз.
Источник:
Sanguineti G, D'Urso P, Bottero M, Farneti A, Goanta L, Giannarelli D, Landoni V. Stereotactic Radiation Therapy in 3 Fractions for T1 Glottic Cancer. Int J Radiat Oncol Biol Phys. 2025 Jan 1; 121(1): 145-152. doi: 10.1016/j.ijrobp.2024.09.051.
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / АДЕНОКАРЦИНОМА ЛЕГКОГО С МУЦИНОЗНЫМ КОМПОНЕНТОМ: ХАРАКТЕРИСТИКА И ВОЗМОЖНОСТИ ЛЕЧЕНИЯ
Среди всех железистых форм немелкоклеточного рака легкого на долю аденокарциномы с муцинозным компонентом приходится не более 3-10%. Данный морфологический подтип представлен бокаловидными или столбчатыми клетками с активной продукцией муцина, характеризуется слабой или негативной экспрессией TTF1 и высокой распространенностью драйверных мутаций KRAS, а также чаще выявляется у некурящих пациентов [1-2]. У ряда больных на момент манифестации заболевания рентгенологически определяются множественные очаги в одном или обоих легких, что отчасти объясняется преобладанием внутрилегочной диссеминации над отдаленным метастазированием в другие органы [3]. Однако, несмотря на достаточное количество молекулярно-генетических и морфологических исследований, популяционный анализ эффективности классических вариантов лечения и прогноза таких пациентов остается крайне затруднительным из-за небольшого количества больных.
В декабре 2024 года Di Federico и соавторы представили в журнале Annals of Oncology результаты собственной многоцентровой работы, включившей ретроспективные данные 4082 пациентов с аденокарциномой легкого, среди которых у 9,9% (n=404) определялся муцинозный компонент [4]. Задачей исследования служило прямое сравнение клинико-морфологических, молекулярно-генетических и прогностических характеристик, а также непосредственных и отдаленных результатов лечения у пациентов в группах с или без муцинозного компонента.
Авторы показали, что у пациентов с муцинозной аденокарциномой были достоверно ниже медиана стажа курения (15 против 20 пачка/лет; p=0,008), экспрессия PD-L1 TPS (0% против 5%; p<0,0001) и мутационная нагрузка (6,8 против 8,5 мутаций на мегабазу; p<0,0001). Помимо этого, различался и мутационный профиль заболевания: при муцинозной аденокарциноме достоверно чаще определялись мутации KRAS, NKX2-1 (TTF-1), STK11, SMARCA4, GNAS и ALK, а при аденокарциноме без муцинозного компонента – TP53, EGFR, BRAF и MET. Также была выявлена гетерогенность между группами по пораженным органам-мишеням при IV стадии НМРЛ – у пациентов с муцинозным подтипом чаще поражалось противоположное легкое (55,2% против 36,9%; p<0,0001) и реже головной мозг (23,3% против 41,9%; p<0,0001).
Анализ результатов лечения выявил достоверно меньшую чувствительность аденокарциномы с муцинозным компонентом к ингибиторам контрольных точек. Среди 112 пациентов с муцинозной аденокарциномой и 1511 пациентов с аденокарциномой без муцинозного компонента проведение иммунотерапии в первой линии ассоциировалось с достижением объективного ответа у 8,4% и 25,9% (p<0,0001). Медиана безрецидивной и общей выживаемости составили соответственно 2,6 против 3,9 мес. (p<0,0001) и 9,9 против 17,2 мес. (p<0,0001).
Аналогичные результаты были получены и при оценке эффективности KRAS-ингибиторов (n=18 и n=150 соответственно). Частота объективного ответа и медиана выживаемости без прогрессирования были нумерически ниже в группе муцинозной аденокарциномы (16,7% и 4,6 мес.) по сравнению с классическим вариантом (34,9% и 5,6 мес.), однако различия не достигли статистической достоверности (p=0,12 и p=0,17). Показатель общей выживаемости был достоверно ниже в группе муцинозной аденокарциномы (6,8 против 10,8 мес., p=0,018).
Таким образом, авторы приходят к выводу, что муцинозный подтип при аденокарциноме легкого является более агрессивным и менее благоприятным вариантом заболевания, характеризующимся достоверно меньшей эффективностью имеющихся вариантов противоопухолевой терапии, и требует активной разработки новых направлений для лечения.
Источники:
- Yang SR, Chang JC, Leduc C, et al. Invasive Mucinous Adenocarcinomas With Spatially Separate Lung Lesions: Analysis of Clonal Relationship by Comparative Molecular Profiling. J Thorac Oncol. 2021 Jul; 16(7): 1188- 1199. doi: 10.1016/j.jtho.2021.03.023. Epub 2021 Apr 8. PMID: 33839364; PMCID: PMC8240964.
- Buettner R. Invasive mucinous adenocarcinoma: genetic insights into a lung cancer entity with distinct clinical behavior and genomic features. Mod Pathol. 2022 Feb; 35(2): 138-139. doi: 10.1038/s41379-021-00945-0. Epub 2021 Nov 19. PMID: 34795416; PMCID: PMC8786656.
- Shim HS, Kenudson M, Zheng Z, et al. Unique Genetic and Survival Characteristics of Invasive Mucinous Adenocarcinoma of the Lung. J Thorac Oncol. 2015 Aug; 10(8): 1156-62. doi: 10.1097/JTO.0000000000000579. PMID: 26200269.
- Di Federico A, Hong L, Elkrief A, et al. Lung adenocarcinomas with mucinous histology: clinical, genomic, and immune microenvironment characterization and outcomes to immunotherapy-based treatments and KRASG12C inhibitors. Ann Oncol. 2024 Dec 3. S0923-7534(24)04951-2. doi: 10.1016/j.annonc.2024.11.014. Epub ahead of print. PMID: 39637943.
Материал подготовил
И.М. Боровков
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / 2 ЛИНИЯ ТЕРАПИИ EGFR-МУТИРОВАННОГО НЕМЕЛКОКЛЕТОЧНОГО РАКА ЛЕГКОГО: ОБНОВЛЕННЫЕ ДАННЫЕ
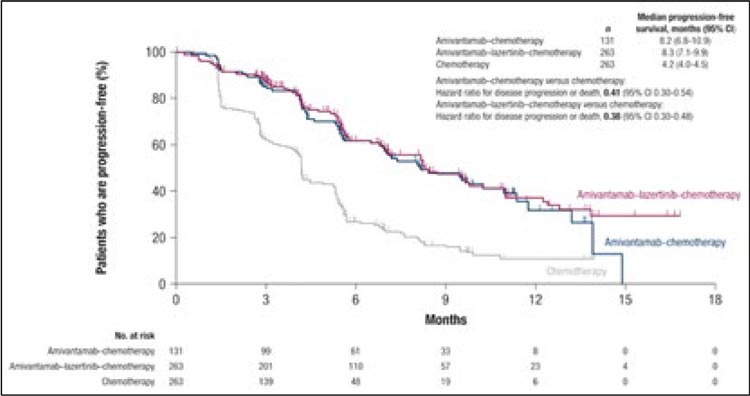
Исследования, изучающие возможности лечения пациентов с EGFR-мутантным НМРЛ, прогрессирующих на фоне терапии осимертинибом, несколько меркнут на фоне более успешных и заметных работ по 1 линии, таких как, например, FLAURA, FLAURA2 и MARIPOSA. Длительное время «стандартом» 2 линии считалось назначение квадриплета ABCP (атезолизумаб, бевацизумаб, карбоплатин, паклитаксел), показавшего определенную эффективность в исследованиях Impower150 и ATTLAS [1-2]. Квадриплет обеспечивал достоверное увеличение медианы выживаемости без прогрессирования (ВБП) до 8,5-9,7 мес., но неоднозначно влиял на общую выживаемость и демонстрировал высокую распространенность нежелательных явлений 3-4 степени (55,7%). Помимо этого, данные работы включали большое количество пациентов, ранее получавших ингибиторы тирозинкиназы I поколения, что также несколько ограничивало возможности трансляции полученных результатов на популяцию больных, получавших только осимертиниб [3]. Новым этапом стала публикация в 2024 году результатов исследования MARIPOSA-2. Авторы показали, что комбинация MEK-ингибитора амивантамаба и платиносодержащей химиотерапии ассоциируется с достоверным увеличением ВБП до 8,2 мес. по сравнению с 8,3 мес. в группе амивантамаб + лазертиниб + ХТ (ОР 0,44; p<0,001) и 4,2 мес. в группе ХТ (ОР 0,48; p<0,001), но сопровождается выраженной токсичностью (частота НЯ 3-4 ст. 72%) (рис.1) [4]. Однако, несмотря на эффективность и регистрацию FDA, применение амивантамаба по-прежнему ограничено его высокой стоимостью, что невольно поднимает вопрос, остаются ли равноэффективные альтернативы данному препарату?
Рисунок 1.
Выживаемость без прогрессирования в MARIPOSA-2 (investigator-assessed).
Определенную популярность в последнее время стали приобретать работы по продолжению терапии осимертинибом после прогрессирования. Ранее мы уже упоминали публикацию Natalie F. и соавт., которые показали, что реинтродукция осимертиниба у тяжело предлеченных пациентов, получавших ингибиторы EGFR 3 поколения, обеспечивала контроль заболевания (частичный ответ – 13%, стабилизация – 38%) в течение 7,5 мес. [4]. Однако медиана длительности интервала от прекращения осимертиниба до его возобновления в исследовании составила 13,8 мес., что не позволяет ответить на вопрос, есть ли смысл в продолжении терапии непосредственно после прогрессирования.
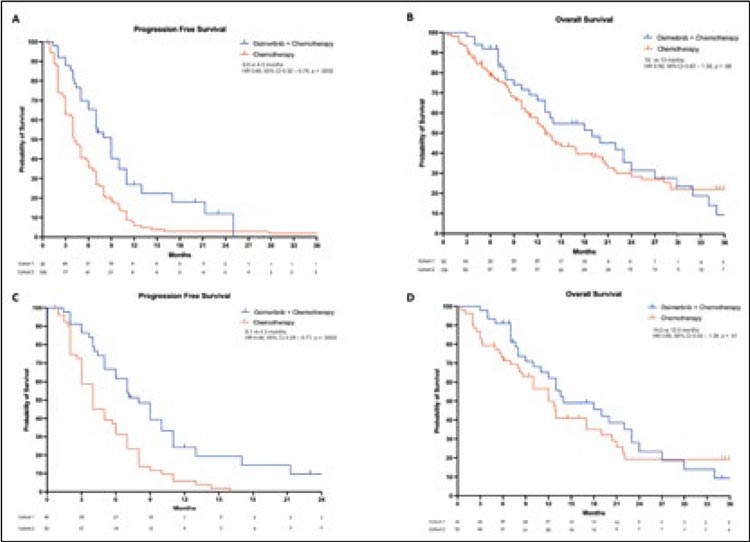
Возможное решение было представлено в ретроспективном анализе Patil T. в декабре 2024 года [5]. Авторы включили пациентов, прогрессирующих на фоне 1 или 2 (T790M+) линии терапии осимертинибом, и разделили их на «экспериментальную» (продолжение осимертиниба с началом пеметрексед-содержащей химиотерапии, n=50) и «контрольную» завершение осимертиниба, начало ХТ с пеметрекседом, n=109) группы. При медиане наблюдения в 30 мес. рентгенологическое подтверждение прогрессирования заболевания было выявлено у 139 пациентов, а медиана выживаемости без прогрессирования составила 9,0 и 4,5 мес. в экспериментальной и контрольной группах соответственно (ОР 0,49; 95% ДИ 0,32-0,74; p=0,0032). Однако около 30% в группе проведения химиотерапии ранее получали бевацизумаб или ингибиторы контрольных точек, в связи с чем был проведен дополнительный анализ, исключающий таких пациентов. Были получены схожие данные: среди 98 пациентов медиана ВБП в двух группах составила 8,0 и 4,0 мес. соответственно (ОР 0,46; 95% ДИ 0,29-0,71; p<0,0001). Улучшение показателя ВБП сохранялось при продолжении осимертиниба даже после исключения всех пациентов, получавших осимертиниб во 2+ линиях (n=55, 11,0 против 6,2 мес.; ОР 0,41, 95% ДИ 0,25-0,73, p=0,002). Отдельного внимания заслуживает оценка ВБП в ЦНС. При анализе пациентов без метастазов в головном мозге на момент прогрессирования было выявлено, что продолжение осимертиниба с добавлением ХТ ассоциировалось с достоверным увеличением медианы ВБП в ЦНС до 7,0 мес. по сравнению с 4,1 мес. в группе ХТ (ОР 0,47; 95% ДИ 0,48-0,98; p=0,01). Значимых различий по показателю общей выживаемости как в общей выборке, так и в подгрупповых анализах выявлено не было, однако отмечалось нумерическое увеличение медианы ОВ до 19 мес. по сравнению с 13 мес. при продолжении терапии осимертинибом (ОР 0,92; 95% ДИ 0,60-1,39; p=0,68) (рис.2). Авторы заключают, что описанный подход является перспективным направлением для дальнейшего изучения в рамках рандомизированных работ, обеспечивает достоверный контроль заболевания при прогрессировании и предлагает новую опцию лечения, заслуживающую рассмотрения в общей популяции больных.
Рисунок 2.
Безрецидивная и общая выживаемость
в исследовании Patil T. А – ВБП в общей выборке пациентов;
B – ОВ в общей выборке пациентов; C – ВБП в подгруппе
пациентов, не получавших бевацизумаб и ингибиторы
контрольных точек; D – ОВ в подгруппе пациентов, не
получавших бевацизумаб и ингибиторы контрольных точек.
Другой вариант лечения при прогрессировании был предложен на ESMO Asia 2024 [6]. Авторы представили объединенный анализ TROPION-Lung05 и -01, включивший 96 пациентов, получавших ранее осимертиниб (1 линия – 40,2%, 2 линия – 29,1%, медиана количества линий – 3). Применение датопотомаба дерукстекана ассоциировалось с достижением объективного ответа у 44,8% пациентов, среди которых у 4,2% определялся полный ответ, у 40,6% – частичный ответ и у 38,5% – стабилизация, а медиана длительности ответа составила 6,9 мес. Медиана общей и безрецидивной выживаемости в данной группе составила 14,7 и 5,7 мес. соответственно. Данные по токсичности терапии соответствовали таковым в оригинальных исследованиях, а частота нежелательных явлений 3-4 ст. не превышала 23%. На основании представленного прессрелиза FDA присвоил данному протоколу «прорывной» статус. Однако, учитывая предыдущий скромный «опыт» датопотамаба дерукстекана и наличие альтернатив, предлагающих по меньшей мере аналогичные (или даже лучшие) отдаленные результаты лечения, представляется сомнительным, что данный препарат займет прочные позиции в терапии EGFR-мутированного НМРЛ в широкой популяции больных.
Источники:
- Socinski MA, Jotte RM, Cappuzzo F. et al; IMpower150 Study Group. Atezolizumab for First-Line Treatment of Metastatic Nonsquamous NSCLC. N Engl J Med. 2018 Jun 14; 378(24): 2288-2301. doi: 10.1056/NEJMoa1716948. Epub 2018 Jun 4. PMID: 29863955.
- Park S, Kim TM, Han JY, et al. Phase III, Randomized Study of Atezolizumab Plus Bevacizumab and Chemotherapy in Patients With EGFR- or ALK-Mutated Non-SmallCell Lung Cancer (ATTLAS, KCSGLU19-04). J Clin Oncol. 2024 Apr 10; 42(11): 1241-1251. doi: 10.1200/ JCO.23.01891. Epub 2023 Oct 20. Erratum in: J Clin Oncol. 2024 Aug 1; 42(22): 2725. doi: 10.1200/ JCO.24.01092. PMID: 37861993; PMCID: PMC11095857.
- www.rosoncoweb.ru/news/ oncology/2024/10/31/.
- Natalie F. Uy, et al. Osimertinib rechallenge in advanced EGFR nonsmall cell lung cancer patients. JCO. 2023; 41: e21196-e21196. doi: 10.1200/ JCO.2023.41.16_suppl.e21196.
- Patil T, Gao D, Watson A, et al. The efficacy of continuing osimertinib with platinum pemetrexed chemotherapy upon progression in patients with metastatic non-small cell lung cancer harboring sensitizing EGFR mutations. Lung Cancer. 2024 Nov 25; 199: 108040. doi: 10.1016/j. lungcan.2024.108040. Epub ahead of print. PMID: 39615411.
- www.daiichisankyo.com/files/news/pressrelease/pdf/202412/20241206_E. pdf.
Материал подготовил
И.М. Боровков
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / НИВОЛУМАБ И ИПИЛИМУМАБ В НЕОАДЪЮВАНТНОМ РЕЖИМЕ ПРИ НЕМЕЛКОКЛЕТОЧНОМ РАКЕ ЛЕГКОГО: ОБНОВЛЕННЫЕ РЕЗУЛЬТАТЫ CHECKMATE 816
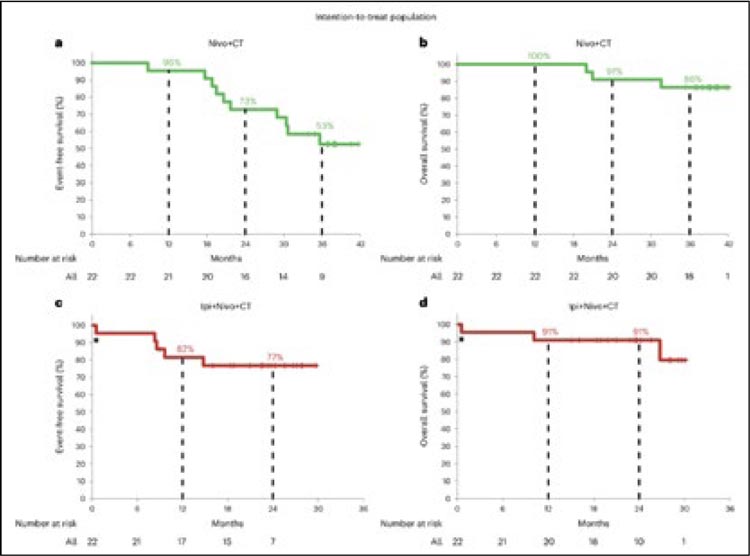
8 января 2025 года в JCO были представлены обновленные результаты эксплораторного анализа исследования CheckMate 816, сравнившего эффективность платиносодержащей химиотерапии и комбинации ниволумаба и ипилимумаба без ХТ при неоадъювантном лечении местнораспространенного немелкоклеточного рака легкого (НМРЛ) [1]. Оригинальное исследование CM816 было опубликовано еще в 2022 году и стало прародителем целого направления работ по применению ингибиторов контрольных точек (ИКТ) в сочетании с химиотерапией в лечении операбельного НМРЛ, показав достоверное увеличение в экспериментальной группе бессобытийной выживаемости (3-летняя EFS – 57% против 43%, ОР 0,68) и частоты полных патоморфологических ответов (pCR – 24% против 2,2%, ОШ 13,94). В последующие годы роль ИКТ была детально изучена, а их назначение стало неотъемлемой частью современного комбинированного лечения местнораспространенного рака легкого. Однако большинство работ акцентировали внимание исключительно на сочетании одного иммунологического препарата (ниволумаб, пембролизумаб, дурвалумаб и др.) с ХТ, в то время как роль двойной иммунной блокады у данных больных была изучена гораздо меньше. Одним из наиболее значимых стало исследование II фазы NEOSTAR, авторы которого сравнили 2 группы – ниволумаб + ипилимумаб + ХТ (n=22) и ниволумаб + ХТ (n=22) [2]. Было показано, что группы достоверно не различались по частоте полных патоморфологических ответов (18,2%), а медиана бессобытийной выживаемости не была достигнута ни в одной из групп (2-летняя EFS – 77% и 73% соответственно) (рис.1). В то же время в группе двойной блокады определялся значительно меньший процент жизнеспособных клеток по результатам гистологического исследования (4,5% против 50,5%) и меньший риск внутрилегочного прогрессирования среди пациентов с MPR/pCR (9% и 0% против 42% и 25%). Тем не менее, отсутствие достоверного влияния на отдаленные результаты лечения, малая выборка и высокая стоимость подобной терапии не позволили двойной блокаде приобрести большую популярность.
Рисунок 1.
Отдаленные результаты лечения в NEOSTAR.
Но открытым оставался вопрос, можно ли отказаться при назначении двойной иммунной блокады от химиотерапии. В дополнительных рукавах CheckMate 816 пациенты были разделены на экспериментальную (ниволумаб + ипилимумаб, n=113) и контрольную (платиносодержащая химиотерапия, n=108) группы, а первичные конечные точки включили частоту полных патоморфологических ответов (pCR) и показатель 4-летней бессобытийной выживаемости (EFS). Группы были хорошо сбалансированы между собой с преобладанием пациентов с IIIa ст. (63% и 61%) и стажем курения (88% и 90%). Полный объем лекарственного лечения был проведен у 91% и 86% пациентов, хирургическое вмешательство выполнено у 73% и 76%, а частота выполнения пневмонэктомии составила 11% и 21% в двух группах соответственно. При этом ведущей причиной отказа от операции служило прогрессирование заболевание (16% и 8%), выявляемое вдвое чаще у пациентов, получавших двойную иммунотерапию.
Рисунок 2.
Бессобытийная выживаемость и частота pCR/MPR
в общей выборке больных, CheckMate 816.
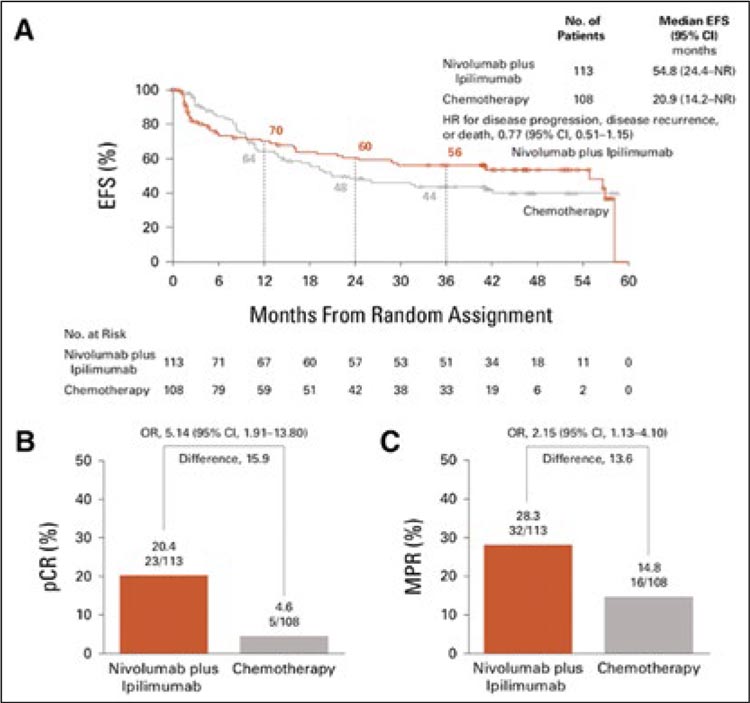
Аналогично предыдущим исследованиям, проведение иммунотерапии ассоциировалось с достоверным увеличением бессобытийной выживаемости и частоты полных патоморфологических ответов. Так, при медиане наблюдения в 49,2 мес. показатель 3-летней EFS составил 56% и 44% (медиана EFS в экспериментальной группе не достигнута, в контрольной – 20,9 мес.; ОР 0,77), а частоты pCR – 20,4% и 4,6% (рис.2А-С). Однако также было отмечено пересечение кривых EFS на отметке в 9 месяцев, что соотносится с данными о большей частоте прогрессирования на предоперационном этапе в экспериментальной группе и говорит о недостаточном контроле заболевания при отказе от цитотоксических агентов. Помимо этого, с высоким риском раннего прогрессирования коррелировала экспрессия PD-L1<1%, а экспрессия PD-L1>1% (n=118), напротив, сопровождалась большей бессобытийной выживаемостью (ОР 0,47). Стадия НМРЛ не влияла на эффективность лечения по данным подгруппового анализа.
Как и в исследовании NEOSTAR, двойная иммунная блокада сопровождалась большей глубиной ответа и лучшим локорегиональным контролем – медиана доли резидуальных опухолевых клеток в двух группах составила 10% и 60% (4,5% и 50,5% в NEOSTAR), а частота внутрилегочного прогрессирования – 16% и 24%. Данные по общей выживаемости на момент публикации не достигли статистической зрелости, однако уже сейчас могут быть предварительно трактованы в пользу иммунной терапии – 3-летняя ОВ в экспериментальной и контрольной группах составила 73% и 61% (ОР 0,73). Также интерес вызывает анализ циркулирующей опухолевой ДНК (цоДНК) и ее клиренса (n=66). Авторы показали, что именно химиотерапия обеспечивала наиболее быстрый и выраженный клиренс уже после 1 курса лечения, а полная ликвидация цоДНК была отмечена у 11% (4/36) в экспериментальной и 33% (10/30) в контрольной группах (рис.3). Подобные различия, также как и данные о раннем прогрессировании, свидетельствуют о том, что именно химиотерапия обеспечивает контроль заболевания на начальных этапах лечения, а для полной реализации эффекта ингибиторов контрольных точек требуется более длительное время, достигающее, согласно разным авторам, 1,5-3 месяцев [3-4].
Рисунок 3.
Клиренс циркулирующей опухолевой ДНК.
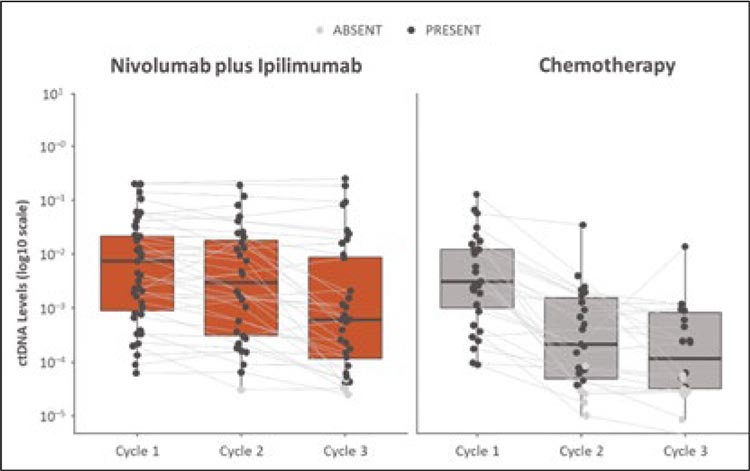
Лечение характеризовалось удовлетворительным профилем безопасности – нежелательные явления 3-4 степени были выявлены у 14% пациентов в группе ниволумаб + ипилимумаб против 36% пациентов в группе ХТ и служили непосредственной причиной прекращения терапии у 5% и 7% соответственно. Структура и частота послеоперационных осложнений между группами клинически значимо не различались (15% и 14%). Подводя итог, можем ли мы сказать, что отказ от ХТ в пользу двойной иммунотерапии обеспечивает такие же результаты лечения? С одной стороны, мы видим аналогичные оригинальному CM816 показатели 3-летней EFS – 56% (ниво+ипи) и 57% (ниво+ХТ), а также схожую глубину ответа c достижением pCR – 20,4% (ниво+ипи) и 24% (ниво+ХТ). С другой же стороны, двойная иммунная блокада с отказом от ХТ характеризовалось ранним прогрессированием у 16% пациентов по сравнению с 6,7% у пациентов, получавших комбинацию ИКТ и ХТ в оригинальном CM816, что наравне с низким клиренсом цоДНК сигнализирует о недостаточном контроле заболевания на начальных этапах лечения. Конечно, для формулировки окончательных выводов требуется тщательная дифференциация истинного прогрессирования и явлений псевдопрогрессии, что в настоящей работе не приводится и только упоминается самими авторами, но представленные результаты дают мало аргументов в пользу изменения имеющихся парадигм комбинированного лечения НМРЛ. В то же время, могут ли быть пациенты, которые выиграют от назначения комбинации ингибиторов PD/-L1 и CTLA-4? По данным ряда работ, наличие мутации в гене KRAS с некоторыми ко-мутациями (например, TP53, STK11/LKB1 и KEAP1) ассоциируется с достоверным увеличением эффективности ингибиторов контрольных точек канцерогенеза, что в теории может говорить о вероятности улучшения отдаленных результатов лечения при интенсификации иммунной терапии [5-6]. Однако для этого, несомненно, потребуется проведение более узконаправленных исследований, сравнивающих одно- и двухкомпонентную иммунную блокаду и, вероятнее всего, добавление платиносодержащей химиотерапии для предотвращения раннего прогрессирования заболевания. А до тех пор стандартом остается применение схем, описанных в таких исследованиях, как CheckMate 816 (ниволумаб + ХТ), Keynote671, AEGEAN и др.
Источники:
- Awad MM, Forde PM, Girard N, et al. Neoadjuvant Nivolumab Plus Ipilimumab Versus Chemotherapy in Resectable Lung Cancer. J Clin Oncol. 2025 Jan 8. JCO2402239. doi: 10.1200/JCO-24-02239. Epub ahead of print. PMID: 39778121.
- Cascone T, Leung CH, Weissferdt A, et al. Neoadjuvant chemotherapy plus nivolumab with or without ipilimumab in operable non-small cell lung cancer: the phase 2 platform NEOSTAR trial. Nat Med. 2023 Mar; 29(3): 593-604. doi: 10.1038/ s41591-022-02189-0. Epub 2023 Mar 16. PMID: 36928818; PMCID: PMC10033402.
- Berz AM, Dromain C, Vietti-Violi N, Boughdad S, Duran R. Tumor response assessment on imaging following immunotherapy. Front Oncol. 2022 Oct 25; 12: 982983. doi: 10.3389/fonc.2022.982983. Erratum in: Front Oncol. 2023 Mar 07; 13: 1175321. doi: 10.3389/ fonc.2023.1175321. PMID: 36387133; PMCID: PMC9641095.
- Borcoman E, Nandikolla A, Long G, Goel S, Le Tourneau C. Patterns of Response and Progression to Immunotherapy. Am Soc Clin Oncol Educ Book. 2018 May 23; 38: 169-178. doi: 10.1200/EDBK_200643. PMID: 30231380.
- Laktionov KK, Kazakov AM, Sarantseva KA, Scherbo DS, Koval AP. Mutation in the kras gene as a predictor of the effectiveness of immunotherapy for non-small cell lung cancer. Siberian journal of oncology. 2022; 21(1): 115-121. (In Russ.) https://doi.org/10.21294/1814- 4861-2022-21-1-115-121.
- Uprety D, Remon J, Peters S. First-Line Dual Immunotherapy, a Treatment Option in First-Line Metastatic Non-Small-Cell Lung Cancer: Are We Ready to Use It? J Clin Oncol. 2024 Feb 1; 42(4): 378-382. doi: 10.1200/JCO.23.01524. Epub 2023 Nov 30. PMID: 38033277.
Материал подготовил
И.М. Боровков
ПРОЧТИ ОБ ЭТОМ РАНЬШЕ, ЧЕМ ТВОЙ ПАЦИЕНТ / ОЦЕНКА ЧАСТОТЫ КОСТНЫХ ПЕРЕЛОМОВ В ИССЛЕДОВАНИИ PEACE-3 (223-RA + ЭНЗАЛУТАМИД VS ЭНЗАЛУТАМИД)
На ESMO 2024 было представлено исследование PEACE-3 [1], в котором сравнивалась комбинация 223-радия и энзалутамида с монотерапией энзалутамидом среди мало- и асимптомных пациентов с мКРРПЖ и костными метастазами. Исследование является позитивным по своей первичной конечной точке: рВБП – 19,4 мес. против 16,4 мес. соответственно (ОР 0,69; 95% ДИ 0,54-0,87; р=0,0009). Ранее в исследовании ERA-223 [2] комбинация абиратерона ацетата (АА) и радия продемонстрировала высокую частоту костных событий (29% против 11% в группе монотерапии АА), что послужило поводом к запрету на использование данной комбинации Европейским медицинским агентством [3]. Причиной подобных результатов послужил тот факт, что только ≈40% пациентов в каждой из групп получили остеомодифицирующие агенты (ОМА).
После представления результатов ERA-223 исследователи протокола PEACE-3 приняли решение о срочном начале использования ОМА в марте 2018 года (ежемесячная терапия золедроновой кислотой или деносумабом) [4]. Сто пятнадцать пациентов из 251 больного, доступного для оценки эффективности и безопасности, были включены до получения срочного извещения. Среди 115 пациентов 53 (46,1%) получили ОМА согласно решению лечащего врача до перелома. Суммарно в данной работе 184 (73%) больных получили ОМА.
После 1 года терапии кумулятивный риск переломов без ОМА в группах энзалутамида и комбинации составил 15,6% и 37,1% соответственно. После внедрения ОМА вышеуказанный показатель значительно снизился: 2,6% и 2,7% в группах монотерапии и комбинации соответственно (рис.1).
Рисунок 1.
Частота костных переломов согласно группе
лечения и использованию ОМА.
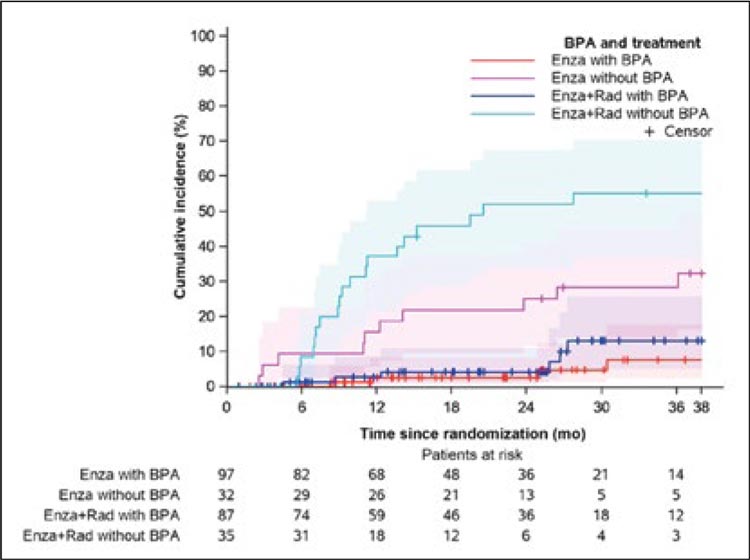
Удивительно, как сопутствующая терапия может влиять на судьбу рандомизированных исследований и изучаемых экспериментальных режимов. Подводя краткий итог, хочется повторить, что остеомодифицирующая терапия является обязательной для пациентов с мКРРПЖ и костными метастазами вне зависимости от проводимой противоопухолевой терапии. А пока что мы ждем финальных результатов PEACE-3 с данными по ОВ.
Источники:
- ESMO Congress 2024. OncologyPRO. Accessed: Jan. 19, 2025 [online].
- Smith M, et al. Addition of radium-223 to abiraterone acetate and prednisone or prednisolone in patients with castration-resistant prostate cancer and bone metastases (ERA 223): a randomised, doubleНачало на стр. 12 blind, placebo-controlled, phase 3 trial. Lancet Oncol. Mar. 2019; Vol.20, no.3, P.408-419. doi: 10.1016/S1470- 2045(18)30860-X.
- Gourd E. EMA guidance on radium-223 dichloride in prostate cancer. Lancet Oncol. Apr. 2018; Vol.19, no.4, P.e190, doi: 10.1016/ S1470-2045(18)30216-X.
- Gillessen S, et al. Decrease in Fracture Rate with Mandatory Bone-protecting Agents in the EORTC 1333/PEACE-3 Trial Comparing Radium-223 Combined with Enzalutamide Versus Enzalutamide Alone: A Safety Analysis. Eur Urol. Jan. 2025. doi: 10.1016/J.EURURO.2024.11.027.
Материал подготовил
Э.Р. Исраелян
НОВОСТИ ОНКОЛОГИИ / ОЛИГОПРОГРЕССИРУЮЩИЙ МЕТАСТАТИЧЕСКИЙ УРОТЕЛИАЛЬНЫЙ РАК – ВЫБОР ТАКТИКИ ПО МНЕНИЮ РОССИЙСКИХ ОНКОЛОГОВ
Авторы: Тимофеев Илья Валерьевич
Директор Бюро по изучению рака (Россия), член Международного комитета ASCO (США),
член научного комитета Колледжа Европейской Школы Онкологии (ESCO)
Тимофеев Илья Валерьевич
Заведующая радиологическим отделением ГУЗ «Областной клинический онкологический диспансер»,
директор Центра лучевой терапии «R-Spei», кандидат медицинских наук, Ульяновск
В отличие от других опухолей, концепция олигометастатического и, тем более, олигопрогрессирующего метастатического уротелиального рака не сформирована. В ретроспективных исследованиях и описаниях клинических случаев приводятся различные критерии и термины для этих состояний [1-5]. Если попытаться обобщить эти данные, то авторы дают следующие определения. Олигометастатический уротелиальный рак – состояние, при котором выявляется первичная опухоль и синхронные метастазы в количестве, по разным данным, до 3 или 5 очагов. В трех исследованиях выявление метастазов в печени было критерием исключения, независимо от их числа и размеров. Под олигорецидивом понимается появление олигометастазов после радикального/ условно-радикального лечения первичной опухоли. И, наконец, олигопрогрессирование описывается как прогрессирование болезни за счет появления новых или значимого увеличения имеющихся метастазов в количестве до 3-5 при условии, что все остальные очаги стабильны на фоне лекарственного или локального лечения.
В 2025 году в случае множественных метастазов уротелиального рака предпочтительным стандартом первой линии является химиотерапия на основе препаратов платины с поддерживающей терапией авелумабом [6, 7] или монотерапия ингибиторами контрольных точек в случае непереносимости цисплатина и карбоплатина [6, 8]. Такие подходы обеспечивают медиану выживаемости без прогрессирования в 5,5 и 2,2 месяца соответственно [9, 10]. Результаты российских исследований реальной практики подтверждают эти цифры [11, 12]. Далее у половины пациентов отмечается прогрессирование болезни, требующее согласно существующим рекомендациям перехода на вторую линию [6]. Суммарно медиана общей выживаемости составляет 23,8 месяца у пациентов, получивших химиотерапию с последующим авелумабом, и 11,3 месяца при монотерапии пембролизумабом [9, 10]. Можно ли увеличить продолжительность жизни пациентов с олигопрогрессированием на фоне первой линии терапии путем локального лечения прогрессирующих очагов с сохранением первой линии? Как часто в практике встречается олигопрогрессирование уротелиального рака? Какие варианты рассматривают российские онкологи в такой ситуации? Бюро по изучению рака (Россия) провело электронный опрос в период с 20 по 26 декабря 2024 года, в котором приняли участие 72 специалиста в области лечения рака мочевого пузыря (химиотерапевты – 43%, хирурги – 28%, радиотерапевты – 26%, организаторы здравоохранения – 3%) [13]. Ежемесячно 71% респондентов ведут более 5 пациентов с уротелиальным раком. Олигопрогрессированием в данном опросе считаете появление <5 новых метастазов и/ или увеличение в размерах <5 метастазов (суммарно). Результаты представлены ниже.
Во-первых, ожидаемо, что большинство онкологов предпочитают использовать химиотерапию с поддерживающей терапией авелумабом в первой линии лечения метастатического уротелиального рака.
Во-вторых, 70% онкологов наблюдают олигопрогрессирование у этих пациентов часто или очень часто.
В-третьих, и это представляется наиболее важным, 71% онкологов считают стереотаксис на очаги олигопрогрессирования с продолжением той же самой первой линии терапии основной опцией ведения таких пациентов. Действительно, несмотря на отсутствие проспективных рандомизированных исследований, такой подход описывается в сериях нескольких наблюдений [2].
И, наконец, 79,4% онкологов считают целесообразным проРисунок 1 ведение проспективного рандомизированного исследования у пациентов с олигопрогрессированием для оценки тактики лечения.
Рисунок 1.
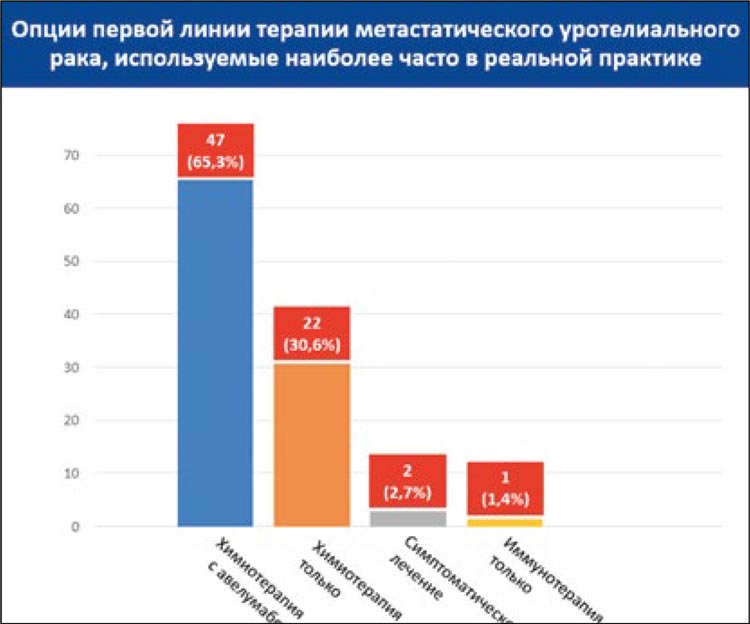
Рисунок 2.
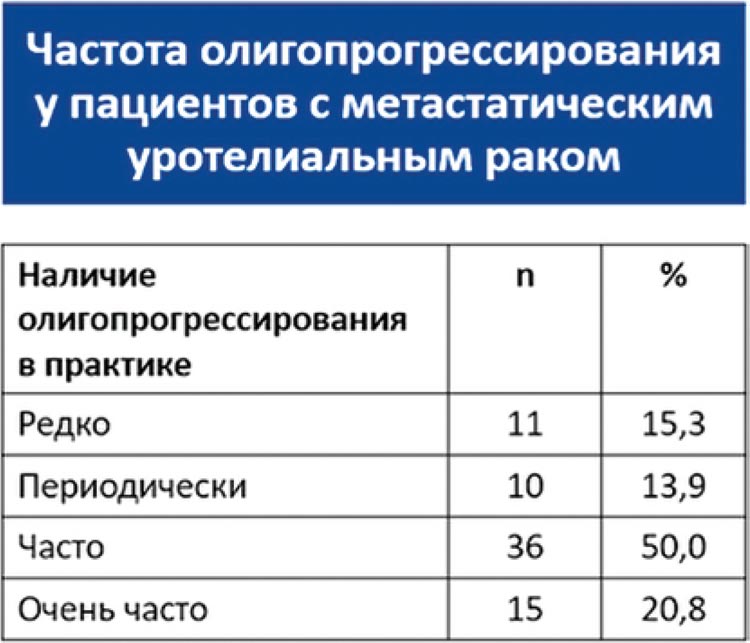
Рисунок 3.
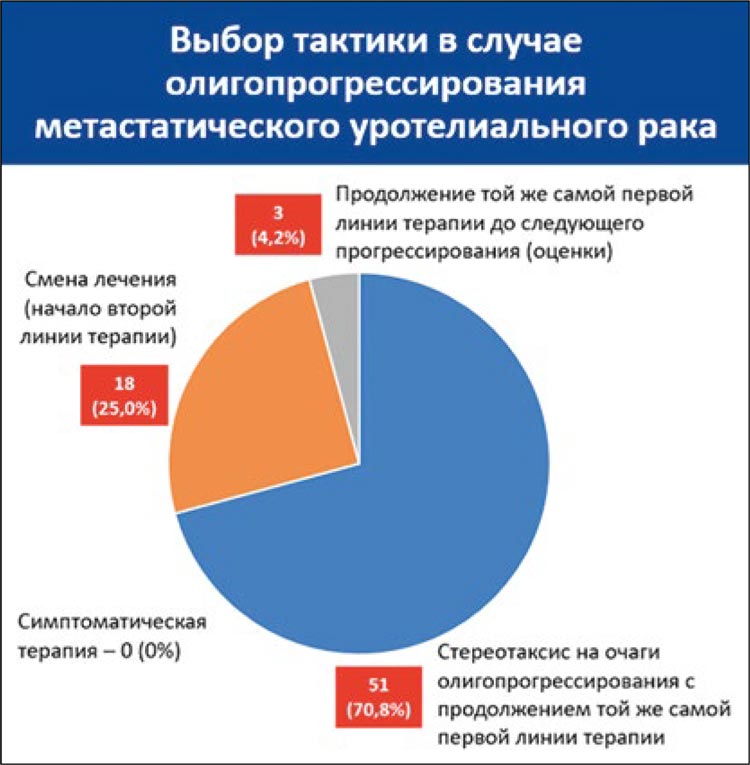
На основании результатов данного опроса Бюро по изучению рака планирует проведение многоцентрового рандомизированного исследования 2 фазы (Volga 2), оценивающего эффективность и безопасность стереотаксической лучевой терапии и продолжение терапии первой линии по сравнению с переходом на вторую линию у пациентов с олигопрогрессированием на поддерживающей терапии авелумабом. Первичной конечной точкой в исследовании будет общая выживаемость.
Источники:
- Francolini G, Desideri I, Detti B, et al. Stereotactic radiotherapy in oligoprogressive and oligorecurrent urothelial cancer patients: A retrospective experience. Cancer Treat Res Commun. 2019; 19: 100124.
- Bamias A, Stenzl A, Zagouri F, Andrikopoulou A, Hoskin P. Defining Oligometastatic Bladder Cancer: A Systematic Review. Eur Urol Open Sci. 2023 Aug 22; 55: 28-37.
- Franzese C, Francolini G, Nicosia L, Alongi F, Livi L, Scorsetti M. Stereotactic Body Radiation Therapy in the Management of Oligometastatic and Oligoprogressive Bladder Cancer and Other Urothelial Malignancies. Clin Oncol (R Coll Radiol). 2021 Jan; 33(1): 50-56.
- Shatkovskaya O, Kaidarova D, Ongarbayev B, et al. Five-year overall survival of patients with advanced bladder cancer in Kazakhstan: OSURK registry study. Am J Clin Exp Urol. 2023 Dec 15; 11(6): 542-548.
- Berghen C, Joniau S, Vulsteke C, et al. Metastasis-directed therapy for oligometastatic urological tumours: still no second-hand news. eCancer. 2020; 14: 1036.
- Румянцев А.А., Булычкин П.В., Волкова М.И. и соавт. Рак мочевого пузыря. Практические рекомендации RUSSCO, часть 1.2. Злокачественные опухоли. 2024; 14(3s2): 221-241.
- Grivas P, Grande E, Davis ID, et al. Avelumab first-line maintenance treatment for advanced urothelial carcinoma: review of evidence to guide clinical practice. ESMO Open. 2023 Dec; 8(6): 102050.
- Tsimafeyeu I, Tjulandin S. Firstline checkpoint inhibitors in PDL1-positive patients with advanced urothelial carcinoma. BJU Int. 2019 Apr; 123(4): 563-565.
- Powles T, Park SH, Caserta C, et al. Avelumab First-Line Maintenance for Advanced Urothelial Carcinoma: Results From the JAVELIN Bladder 100 Trial After ≥2 Years of FollowUp. J Clin Oncol. 2023 Jul 1; 41(19): 3486-3492.
- Vuky J, Balar AV, Castellano D, et al. Long-Term Outcomes in KEYNOTE-052: Phase II Study Investigating First-Line Pembrolizumab in CisplatinIneligible Patients With Locally Advanced or Metastatic Urothelial Cancer. J Clin Oncol. 2020 Aug 10; 38(23): 2658-2666.
- Petkau V, Alekseeva G, Zukov R, et al. The association of access to systemic therapy and overall survival in metastatic bladder cancer in Russia: An analysis of URRU register. J Clin Oncol. 2021; 39 (suppl 28), abstr 88.
- Gridneva Y, Sultanbaev A, Anzhiganova Yu, et al. Maintenance therapy with avelumab as the first-line treatment in patients with metastatic urothelial carcinoma: A real-world, ambispective RAVE-Bladder study. JCO. 2024; 42: e16569-e16569. DOI: 10.1200/JCO.2024.42.16_suppl. e16569.
- Веб-сайт Бюро по изучению рака (БИР): https://www.rosrak.ru/